+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of dodecameric RdrB cage | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Cryoelectron microscopy / adenosine deaminase / IMMUNE SYSTEM | |||||||||
| 機能・相同性 | deaminase activity / Adenosine/adenine deaminase / Metal-dependent hydrolase / Adenosine deaminase 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.58 Å | |||||||||
 データ登録者 データ登録者 | Gao Y | |||||||||
| 資金援助 |  中国, 1件 中国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Cell / 年: 2023 ジャーナル: Cell / 年: 2023タイトル: Molecular basis of RADAR anti-phage supramolecular assemblies. 著者: Yina Gao / Xiu Luo / Peipei Li / Zhaolong Li / Feng Ye / Songqing Liu / Pu Gao /  要旨: Adenosine-to-inosine RNA editing has been proposed to be involved in a bacterial anti-phage defense system called RADAR. RADAR contains an adenosine triphosphatase (RdrA) and an adenosine deaminase ...Adenosine-to-inosine RNA editing has been proposed to be involved in a bacterial anti-phage defense system called RADAR. RADAR contains an adenosine triphosphatase (RdrA) and an adenosine deaminase (RdrB). Here, we report cryo-EM structures of RdrA, RdrB, and currently identified RdrA-RdrB complexes in the presence or absence of RNA and ATP. RdrB assembles into a dodecameric cage with catalytic pockets facing outward, while RdrA adopts both autoinhibited tetradecameric and activation-competent heptameric rings. Structural and functional data suggest a model in which RNA is loaded through the bottom section of the RdrA ring and translocated along its inner channel, a process likely coupled with ATP-binding status. Intriguingly, up to twelve RdrA rings can dock one RdrB cage with precise alignments between deaminase catalytic pockets and RNA-translocation channels, indicative of enzymatic coupling of RNA translocation and deamination. Our data uncover an interesting mechanism of enzymatic coupling and anti-phage defense through supramolecular assemblies. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_34967.map.gz emd_34967.map.gz | 227.8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-34967-v30.xml emd-34967-v30.xml emd-34967.xml emd-34967.xml | 13.4 KB 13.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_34967.png emd_34967.png | 96.8 KB | ||
| その他 |  emd_34967_half_map_1.map.gz emd_34967_half_map_1.map.gz emd_34967_half_map_2.map.gz emd_34967_half_map_2.map.gz | 191.4 MB 191.1 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-34967 http://ftp.pdbj.org/pub/emdb/structures/EMD-34967 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-34967 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-34967 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_34967_validation.pdf.gz emd_34967_validation.pdf.gz | 906.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_34967_full_validation.pdf.gz emd_34967_full_validation.pdf.gz | 905.7 KB | 表示 | |
| XML形式データ |  emd_34967_validation.xml.gz emd_34967_validation.xml.gz | 15.8 KB | 表示 | |
| CIF形式データ |  emd_34967_validation.cif.gz emd_34967_validation.cif.gz | 18.6 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34967 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34967 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34967 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34967 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_34967.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_34967.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 1.04 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #1
| ファイル | emd_34967_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
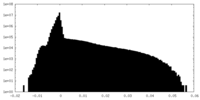
| 投影像・断面図 |
| ||||||||||||
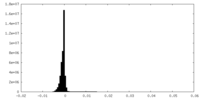
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_34967_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
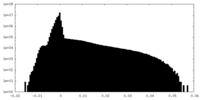
| 投影像・断面図 |
| ||||||||||||
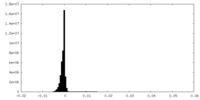
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : RdrB
| 全体 | 名称: RdrB |
|---|---|
| 要素 |
|
-超分子 #1: RdrB
| 超分子 | 名称: RdrB / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  |
-分子 #1: Adenosine deaminase
| 分子 | 名称: Adenosine deaminase / タイプ: protein_or_peptide / ID: 1 / コピー数: 12 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 92.216953 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MERFLLNSTV LLYRLSTVSL DEVSLDERVE SSVFLAQYEQ ARSLPDHVAK SAWSYLVQQI KQRNMKLGPV AILRLIAEKF IKNEKGGPK IDLPMFSEWQ TLMSRVSCLP IIACHQVFNP GPASQEYSFR WPLYPYHPTV EDYITRECLH ETHQHLNGST S AEECWLDA ...文字列: MERFLLNSTV LLYRLSTVSL DEVSLDERVE SSVFLAQYEQ ARSLPDHVAK SAWSYLVQQI KQRNMKLGPV AILRLIAEKF IKNEKGGPK IDLPMFSEWQ TLMSRVSCLP IIACHQVFNP GPASQEYSFR WPLYPYHPTV EDYITRECLH ETHQHLNGST S AEECWLDA LKHPEACLRD FEKGWASQEM KQLCAQIDPS LTPRIFKDRL QIACNIREIL CRVAQGVELP EWIASMQNPQ QL ANSTILH NGREYGFATV WPIDDKYSQE SEFCWLTGLL EKWRFNAPEG LERLLWIYLL IQNQYLTLLV QRDDFFGFEQ FQN YTMTEL REETEKSYLS RFKHAHGAGV YSQVRYLEGR FAPKSDPNKM QKLLFSVLRG YWEYLSAHMS MEWVHEKPLT ISQV LDNLE LVEPHGKCVE LALVPHFIKR KPKNGEAYPH ALLFKDLKNQ AAILMDMLKS EPRLTGWIRG VDAAANEMHA PPELF CPLF RVLAKSGIAH FTYHVGEDFP HLISGIRSID DALRFLPLRN GDRLGHCTAI GITPSIWKRS LPLSLSMTKE TRLLDL VFI WRELRSHPEL LRYASDAAIE AVRLAHKVFS LEEEVSITTL DQVFEMRGLL AESEGLLSEL NEPLKPKSLW LEEYERA RE LVKTTGMKRP LKLYKQWLTS DNVRKQRAEY VEVALEYLPD EAVVALQQAV MAKMADRNIA IECPPTSNTR ISQYRNVS E HHIFRWMGLP GEAIEGDVPM SICLGSDDPG IFAADLKSEF YHLFVVLTRK FGLSPADALR KVAEVNENGR IYRFHDVS UniProtKB: Adenosine deaminase |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 60.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 1.5 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期モデル | モデルのタイプ: NONE |
|---|---|
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 2.58 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 373491 |
| 初期 角度割当 | タイプ: PROJECTION MATCHING |
| 最終 角度割当 | タイプ: PROJECTION MATCHING |
 ムービー
ムービー コントローラー
コントローラー




















 Z
Z Y
Y X
X