+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-30537 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM map of Omono River virus (Strain: LZ) full capsid with its fiber-like protrusion anchored at the five-fold vertex. | |||||||||
 マップデータ マップデータ | To show each element of the virus, maps are shown at different counter levels. The major capsid shell: 4%u03C3; Subvolume of the protrusion: 0.65%u03C3. | |||||||||
 試料 試料 | Major capsid dimer of OmRV-LZ (with protrusion) != Omono River virus Major capsid dimer of OmRV-LZ (with protrusion)
| |||||||||
 キーワード キーワード | Totiviridae / major capsid / virus | |||||||||
| 機能・相同性 | Double-stranded RNA binding motif / Double-stranded RNA binding motif / Double stranded RNA-binding domain (dsRBD) profile. / Double-stranded RNA-binding domain / RNA binding / Main capsid protein 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  Omono River virus (ウイルス) Omono River virus (ウイルス) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.79 Å | |||||||||
 データ登録者 データ登録者 | Shao Q / Jia X | |||||||||
| 資金援助 |  中国, 1件 中国, 1件
| |||||||||
 引用 引用 |  ジャーナル: PLoS Pathog / 年: 2021 ジャーナル: PLoS Pathog / 年: 2021タイトル: Cryo-EM reveals a previously unrecognized structural protein of a dsRNA virus implicated in its extracellular transmission. 著者: Qianqian Shao / Xudong Jia / Yuanzhu Gao / Zhe Liu / Huan Zhang / Qiqi Tan / Xin Zhang / Huiqiong Zhou / Yinyin Li / De Wu / Qinfen Zhang /  要旨: Mosquito viruses cause unpredictable outbreaks of disease. Recently, several unassigned viruses isolated from mosquitoes, including the Omono River virus (OmRV), were identified as totivirus-like ...Mosquito viruses cause unpredictable outbreaks of disease. Recently, several unassigned viruses isolated from mosquitoes, including the Omono River virus (OmRV), were identified as totivirus-like viruses, with features similar to those of the Totiviridae family. Most reported members of this family infect fungi or protozoans and lack an extracellular life cycle stage. Here, we identified a new strain of OmRV and determined high-resolution structures for this virus using single-particle cryo-electron microscopy. The structures feature an unexpected protrusion at the five-fold vertex of the capsid. Disassociation of the protrusion could result in several conformational changes in the major capsid. All these structures, together with some biological results, suggest the protrusions' associations with the extracellular transmission of OmRV. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_30537.map.gz emd_30537.map.gz | 771.5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-30537-v30.xml emd-30537-v30.xml emd-30537.xml emd-30537.xml | 13.8 KB 13.8 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
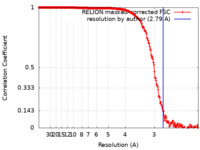
| FSC (解像度算出) |  emd_30537_fsc.xml emd_30537_fsc.xml | 21.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_30537.png emd_30537.png | 239.4 KB | ||
| Filedesc metadata |  emd-30537.cif.gz emd-30537.cif.gz | 6.1 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-30537 http://ftp.pdbj.org/pub/emdb/structures/EMD-30537 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-30537 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-30537 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_30537_validation.pdf.gz emd_30537_validation.pdf.gz | 758.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_30537_full_validation.pdf.gz emd_30537_full_validation.pdf.gz | 757.8 KB | 表示 | |
| XML形式データ |  emd_30537_validation.xml.gz emd_30537_validation.xml.gz | 18.1 KB | 表示 | |
| CIF形式データ |  emd_30537_validation.cif.gz emd_30537_validation.cif.gz | 25.1 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-30537 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-30537 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-30537 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-30537 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_30537.map.gz / 形式: CCP4 / 大きさ: 824 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_30537.map.gz / 形式: CCP4 / 大きさ: 824 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | To show each element of the virus, maps are shown at different counter levels. The major capsid shell: 4%u03C3; Subvolume of the protrusion: 0.65%u03C3. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.09 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Major capsid dimer of OmRV-LZ (with protrusion)
| 全体 | 名称: Major capsid dimer of OmRV-LZ (with protrusion) |
|---|---|
| 要素 |
|
-超分子 #1: Omono River virus
| 超分子 | 名称: Omono River virus / タイプ: virus / ID: 1 / 親要素: 0 / 含まれる分子: all / NCBI-ID: 753758 / 生物種: Omono River virus / Sci species strain: LZ / ウイルスタイプ: VIRION / ウイルス・単離状態: STRAIN / ウイルス・エンベロープ: No / ウイルス・中空状態: No |
|---|---|
| 宿主 | 生物種:  Culex quinquefasciatus (カ) Culex quinquefasciatus (カ) |
| ウイルス殻 | Shell ID: 1 / 名称: Major capsid / 直径: 450.0 Å / T番号(三角分割数): 1 |
-分子 #1: Capsid protein
| 分子 | 名称: Capsid protein / タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Omono River virus (ウイルス) / 株: LZ Omono River virus (ウイルス) / 株: LZ |
| 分子量 | 理論値: 96.860992 KDa |
| 配列 | 文字列: PISADFSEVE NAPSFLSLAE NTDEVLKPYT GLEIQTIITN IVGDANPNQS RIFDQDRLRG NQYSAGGLVT QNAVSAIPFT NLIPRTIRV GNILVNSANR LQITETNVSE YYSNPIIATK LSEMISDQVK NNQFSTWRRD NTSLQGFNAF DIATINTAIL P NGLSLESM ...文字列: PISADFSEVE NAPSFLSLAE NTDEVLKPYT GLEIQTIITN IVGDANPNQS RIFDQDRLRG NQYSAGGLVT QNAVSAIPFT NLIPRTIRV GNILVNSANR LQITETNVSE YYSNPIIATK LSEMISDQVK NNQFSTWRRD NTSLQGFNAF DIATINTAIL P NGLSLESM LLKLSLLHSI KAMNVDAASI NRSQYQVIDH NTVPTIGAPA VVGVNNSPVF GEDCGGNNPV YPFGGGTGAI AF HVTLQTV PDERKSYAIF VPPAILQATS DANEALALFA LSMSEWPHAL YTVTKQTTDL AGANAGQQVF IPTQSTIHIG GRR VLDLII PRREIAPNPT TLVAANAMCM VRPQAGPDAT AGAIPLAAGQ LFNMNFIGAP AFEEWPMTSY LYSWAGRFDI TTIR QYMGR LATMVGVKDA YWAAHELNVA LSQVAPKMTT AAGGWAAQAA NSAQQSDVCY SSLLTVTRSA ANFPLANQPA ADMRV YDTD PATWNKVALG LATAANLVPE QSMDVPFVVG DARASFWERL QAIPMCIAWT MYYHSRGITT LAWDNAYTDN TNKWLQ KMV RNTFSTTQSV GTIIPARYGK IVCNLYKNMF HRAPAYVATS VGGKELHITH FERWLPGGTY ANVYSGAGAV VNCFSPV LI PDIWCQYFTA KLPLFAGAFP PAQGQNSTKG FNSKQGLMIH RNQNNNLVAP YLEKFADNSS YFPVGQGPEI NDMATWNG R LWMTTGNVQY LDYSGAAIVE AVPPAGELPV GKQIPLLAGE NAPIELTNAA TTCVPRYSND GRRIFTYLTT AQSVIPVQA CNRAANLARS CWLLSNVYAE PALQALGDEV EDAFDTLTNS SFLDVAKSVA ESAGEVPATK ALTDLQAVDV SSLPSTSDPS NVLSQPAPL MSPPTSSS |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 構成要素:
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY | |||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: COUNTING / 平均電子線量: 39.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 75000 |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL |
|---|---|
| 得られたモデル |  PDB-7d0k: |
 ムービー
ムービー コントローラー
コントローラー

















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)