+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Human Dis3L2 in complex with hairpin A-GCU14 | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | 3'-5' exonuclease / human exonuclease / RNA BINDING PROTEIN-RNA complex | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報polyuridylation-dependent mRNA catabolic process / miRNA catabolic process / mitotic sister chromatid separation / : / Z-decay: degradation of maternal mRNAs by zygotically expressed factors / poly(U) RNA binding / stem cell population maintenance / : / mRNA catabolic process / RNA nuclease activity ...polyuridylation-dependent mRNA catabolic process / miRNA catabolic process / mitotic sister chromatid separation / : / Z-decay: degradation of maternal mRNAs by zygotically expressed factors / poly(U) RNA binding / stem cell population maintenance / : / mRNA catabolic process / RNA nuclease activity / P-body / mitotic cell cycle / 加水分解酵素; エステル加水分解酵素; 5'-リン酸モノエステル産生エキソリボヌクレアーゼ / 3'-5'-RNA exonuclease activity / negative regulation of cell population proliferation / cell division / magnesium ion binding / cytoplasm / cytosol 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) / synthetic construct (人工物) Homo sapiens (ヒト) / synthetic construct (人工物) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.1 Å | |||||||||
 データ登録者 データ登録者 | Meze K / Thomas DR / Joshua-Tor L | |||||||||
| 資金援助 |  米国, 2件 米国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nat Struct Mol Biol / 年: 2023 ジャーナル: Nat Struct Mol Biol / 年: 2023タイトル: A shape-shifting nuclease unravels structured RNA. 著者: Katarina Meze / Armend Axhemi / Dennis R Thomas / Ahmet Doymaz / Leemor Joshua-Tor /  要旨: RNA turnover pathways ensure appropriate gene expression levels by eliminating unwanted transcripts. Dis3-like 2 (Dis3L2) is a 3'-5' exoribonuclease that plays a critical role in human development. ...RNA turnover pathways ensure appropriate gene expression levels by eliminating unwanted transcripts. Dis3-like 2 (Dis3L2) is a 3'-5' exoribonuclease that plays a critical role in human development. Dis3L2 independently degrades structured substrates, including coding and noncoding 3' uridylated RNAs. While the basis for Dis3L2's substrate recognition has been well characterized, the mechanism of structured RNA degradation by this family of enzymes is unknown. We characterized the discrete steps of the degradation cycle by determining cryogenic electron microscopy structures representing snapshots along the RNA turnover pathway and measuring kinetic parameters for RNA processing. We discovered a dramatic conformational change that is triggered by double-stranded RNA (dsRNA), repositioning two cold shock domains by 70 Å. This movement exposes a trihelix linker region, which acts as a wedge to separate the two RNA strands. Furthermore, we show that the trihelix linker is critical for dsRNA, but not single-stranded RNA, degradation. These findings reveal the conformational plasticity of Dis3L2 and detail a mechanism of structured RNA degradation. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_27828.map.gz emd_27828.map.gz | 96.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-27828-v30.xml emd-27828-v30.xml emd-27828.xml emd-27828.xml | 20.7 KB 20.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_27828.png emd_27828.png | 47.2 KB | ||
| Filedesc metadata |  emd-27828.cif.gz emd-27828.cif.gz | 6.9 KB | ||
| その他 |  emd_27828_half_map_1.map.gz emd_27828_half_map_1.map.gz emd_27828_half_map_2.map.gz emd_27828_half_map_2.map.gz | 80.7 MB 80.7 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-27828 http://ftp.pdbj.org/pub/emdb/structures/EMD-27828 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-27828 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-27828 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_27828_validation.pdf.gz emd_27828_validation.pdf.gz | 1018.1 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_27828_full_validation.pdf.gz emd_27828_full_validation.pdf.gz | 1017.7 KB | 表示 | |
| XML形式データ |  emd_27828_validation.xml.gz emd_27828_validation.xml.gz | 13.1 KB | 表示 | |
| CIF形式データ |  emd_27828_validation.cif.gz emd_27828_validation.cif.gz | 15.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27828 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27828 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27828 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27828 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_27828.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_27828.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 0.66 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #1
| ファイル | emd_27828_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
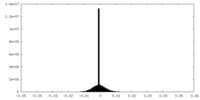
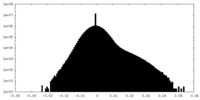
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_27828_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Inactive HsDis3L2 (D391N) in complex with a short hairpin with a ...
| 全体 | 名称: Inactive HsDis3L2 (D391N) in complex with a short hairpin with a 16-nucleotide 3' overhang |
|---|---|
| 要素 |
|
-超分子 #1: Inactive HsDis3L2 (D391N) in complex with a short hairpin with a ...
| 超分子 | 名称: Inactive HsDis3L2 (D391N) in complex with a short hairpin with a 16-nucleotide 3' overhang タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 100 KDa |
-分子 #1: DIS3-like exonuclease 2
| 分子 | 名称: DIS3-like exonuclease 2 / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 96.54332 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MSHPDYRMNL RPLGTPRGVS AVAGPHDIGA SPGDKKSKNR STRGKKKSIF ETYMSKEDVS EGLKRGTLIQ GVLRINPKKF HEAFIPSPD GDRDIFIDGV VARNRALNGD LVVVKLLPEE HWKVVKPESN DKETEAAYES DIPEELCGHH LPQQSLKSYN D SPDVIVEA ...文字列: MSHPDYRMNL RPLGTPRGVS AVAGPHDIGA SPGDKKSKNR STRGKKKSIF ETYMSKEDVS EGLKRGTLIQ GVLRINPKKF HEAFIPSPD GDRDIFIDGV VARNRALNGD LVVVKLLPEE HWKVVKPESN DKETEAAYES DIPEELCGHH LPQQSLKSYN D SPDVIVEA QFDGSDSEDG HGITQNVLVD GVKKLSVCVS EKGREDGDAP VTKDETTCIS QDTRALSEKS LQRSAKVVYI LE KKHSRAA TGFLKLLADK NSELFRKYAL FSPSDHRVPR IYVPLKDCPQ DFVARPKDYA NTLFICRIVD WKEDCNFALG QLA KSLGQA GEIEPETEGI LTEYGVDFSD FSSEVLECLP QGLPWTIPPE EFSKRRDLRK DCIFTIDPST ARDLNDALSC KPLA DGNFK VGVHIADVSY FVPEGSDLDK VAAERATSVY LVQKVVPMLP RLLCEELCSL NPMSDKLTFS VIWTLTPEGK ILDEW FGRT IIRSCTKLSY EHAQSMIESP TEKIPAKELP PISPEHSSEE VHQAVLNLHG IAKQLRQQRF VDGALRLDQL KLAFTL DHE TGLPQGCHIY EYRESNKLVE EFMLLANMAV AHKIHRAFPE QALLRRHPPP QTRMLSDLVE FCDQMGLPVD FSSAGAL NK SLTQTFGDDK YSLARKEVLT NMCSRPMQMA LYFCSGLLQD PAQFRHYALN VPLYTHFTSP IRRFADVLVH RLLAAALG Y RERLDMAPDT LQKQADHCND RRMASKRVQE LSTSLFFAVL VKESGPLESE AMVMGILKQA FDVLVLRYGV QKRIYCNAL ALRSHHFQKV GKKPELTLVW EPEDMEQEPA QQVITIFSLV EVVLQAESTA LKYSAILK UniProtKB: DIS3-like exonuclease 2 |
-分子 #2: RNA hairpin A-GCU14
| 分子 | 名称: RNA hairpin A-GCU14 / タイプ: rna / ID: 2 / コピー数: 1 |
|---|---|
| 由来(天然) | 生物種: synthetic construct (人工物) |
| 分子量 | 理論値: 10.678133 KDa |
| 配列 | 文字列: GAGGCCUUUC GAGGCCUUGC UUUUUUUUUU UUUU |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.3 mg/mL | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
| ||||||||||||
| グリッド | モデル: UltrAuFoil R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 支持フィルム - 材質: GOLD / 支持フィルム - トポロジー: HOLEY ARRAY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 30 sec. / 前処理 - 雰囲気: AIR / 前処理 - 気圧: 0.042 kPa | ||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 90 % / チャンバー内温度: 295 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 温度 | 最低: 80.0 K / 最高: 80.0 K |
| 撮影 | フィルム・検出器のモデル: GATAN K2 QUANTUM (4k x 4k) 検出モード: COUNTING / デジタル化 - サイズ - 横: 3840 pixel / デジタル化 - サイズ - 縦: 3712 pixel / デジタル化 - 画像ごとのフレーム数: 1-25 / 撮影したグリッド数: 1 / 実像数: 9654 / 平均露光時間: 5.0 sec. / 平均電子線量: 51.75 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm 最大 デフォーカス(補正後): 2.8000000000000003 µm 最小 デフォーカス(補正後): 0.5 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.6 µm 最小 デフォーカス(公称値): 0.7000000000000001 µm 倍率(公称値): 160000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | PDB ID: Chain - Chain ID: C / Chain - Source name: PDB / Chain - Initial model type: experimental model |
|---|---|
| 詳細 | The model of Homo Sapiens Dis3L2 was used as a starting reference for the protein and the nucleic acid was used from PDB 4PMW. All manual building was done in Coot. The models were fit into the maps and then refined using PHENIX. |
| 精密化 | 空間: REAL / プロトコル: FLEXIBLE FIT |
| 得られたモデル |  PDB-8e28: |
 ムービー
ムービー コントローラー
コントローラー









 Z
Z Y
Y X
X