+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of human Kidney Betaine-Homocysteine Methyltransferase | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | betaine-homocysteine methyltransferase / BHSMT / HYDROLASE | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報regulation of homocysteine metabolic process / betaine-homocysteine S-methyltransferase / amino-acid betaine metabolic process / betaine-homocysteine S-methyltransferase activity / L-methionine salvage / amino-acid betaine catabolic process / Sulfur amino acid metabolism / Choline catabolism / 'de novo' L-methionine biosynthetic process / protein methylation ...regulation of homocysteine metabolic process / betaine-homocysteine S-methyltransferase / amino-acid betaine metabolic process / betaine-homocysteine S-methyltransferase activity / L-methionine salvage / amino-acid betaine catabolic process / Sulfur amino acid metabolism / Choline catabolism / 'de novo' L-methionine biosynthetic process / protein methylation / extracellular exosome / zinc ion binding / nucleus / cytosol 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
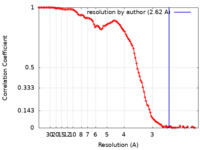
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.62 Å | |||||||||
 データ登録者 データ登録者 | Lyu M / Yu EW | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: To Be Published ジャーナル: To Be Publishedタイトル: Cryo-EM structure of human Kidney Betaine-Homocysteine Methyltransferase 著者: Lyu M / Yu EW | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_27175.map.gz emd_27175.map.gz | 97.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-27175-v30.xml emd-27175-v30.xml emd-27175.xml emd-27175.xml | 15.1 KB 15.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_27175_fsc.xml emd_27175_fsc.xml | 13.7 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_27175.png emd_27175.png | 92.8 KB | ||
| Filedesc metadata |  emd-27175.cif.gz emd-27175.cif.gz | 5.5 KB | ||
| その他 |  emd_27175_half_map_1.map.gz emd_27175_half_map_1.map.gz emd_27175_half_map_2.map.gz emd_27175_half_map_2.map.gz | 95.6 MB 95.6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-27175 http://ftp.pdbj.org/pub/emdb/structures/EMD-27175 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-27175 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-27175 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_27175_validation.pdf.gz emd_27175_validation.pdf.gz | 745.3 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_27175_full_validation.pdf.gz emd_27175_full_validation.pdf.gz | 744.9 KB | 表示 | |
| XML形式データ |  emd_27175_validation.xml.gz emd_27175_validation.xml.gz | 17.6 KB | 表示 | |
| CIF形式データ |  emd_27175_validation.cif.gz emd_27175_validation.cif.gz | 23.5 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27175 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27175 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27175 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27175 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8d45MC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_27175.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_27175.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.07 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #2
| ファイル | emd_27175_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_27175_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Betaine-Homocysteine Methyltransferase
| 全体 | 名称: Betaine-Homocysteine Methyltransferase |
|---|---|
| 要素 |
|
-超分子 #1: Betaine-Homocysteine Methyltransferase
| 超分子 | 名称: Betaine-Homocysteine Methyltransferase / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: Betaine--homocysteine S-methyltransferase 1
| 分子 | 名称: Betaine--homocysteine S-methyltransferase 1 / タイプ: protein_or_peptide / ID: 1 / コピー数: 4 / 光学異性体: LEVO / EC番号: betaine-homocysteine S-methyltransferase |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 45.059441 KDa |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: MPPVGGKKAK KGILERLNAG EIVIGDGGFV FALEKRGYVK AGPWTPEAAV EHPEAVRQLH REFLRAGSNV MQTFTFYASE DKLENRGNY VLEKISGQEV NEAACDIARQ VADEGDALVA GGVSQTPSYL SCKSETEVKK VFLQQLEVFM KKNVDFLIAE Y FEHVEEAV ...文字列: MPPVGGKKAK KGILERLNAG EIVIGDGGFV FALEKRGYVK AGPWTPEAAV EHPEAVRQLH REFLRAGSNV MQTFTFYASE DKLENRGNY VLEKISGQEV NEAACDIARQ VADEGDALVA GGVSQTPSYL SCKSETEVKK VFLQQLEVFM KKNVDFLIAE Y FEHVEEAV WAVETLIASG KPVAATMCIG PEGDLHGVPP GECAVRLVKA GASIIGVNCH FDPTISLKTV KLMKEGLEAA RL KAHLMSQ PLAYHTPDCN KQGFIDLPEF PFGLEPRVAT RWDIQKYARE AYNLGVRYIG GCCGFEPYHI RAIAEELAPE RGF LPPASE KHGSWGSGLD MHTKPWVRAR ARKEYWENLR IASGRPYNPS MSKPDGWGVT KGTAELMQQK EATTEQQLKE LFEK QKFKS Q UniProtKB: Betaine--homocysteine S-methyltransferase 1 |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 平均電子線量: 38.75 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 1.0 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー



 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)