+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | CRYO-EM STRUCTURE OF HUMAN 15-PGDH IN COMPLEX WITH SMALL MOLECULE SW222746 | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード |  DEHYDROGENASE (脱水素酵素) / DEHYDROGENASE (脱水素酵素) /  INHIBITOR (酵素阻害剤) / INHIBITOR (酵素阻害剤) /  OXIDOREDUCTASE (酸化還元酵素) / OXIDOREDUCTASE-INHIBITOR complex OXIDOREDUCTASE (酸化還元酵素) / OXIDOREDUCTASE-INHIBITOR complex | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 15-ヒドロキシプロスタグランジンデヒドロゲナーゼ (NAD+) / 15-ヒドロキシプロスタグランジンデヒドロゲナーゼ (NAD+) /  15-ヒドロキシイコサテトラエン酸デヒドロゲナーゼ / regulation of prostaglandin catabolic process / ductus arteriosus closure / thrombin-activated receptor signaling pathway / 15-ヒドロキシイコサテトラエン酸デヒドロゲナーゼ / regulation of prostaglandin catabolic process / ductus arteriosus closure / thrombin-activated receptor signaling pathway /  排卵 / 排卵 /  prostaglandin E receptor activity / prostaglandin E receptor activity /  15-hydroxyprostaglandin dehydrogenase (NAD+) activity / Synthesis of Lipoxins (LX) / 15-hydroxyprostaglandin dehydrogenase (NAD+) activity / Synthesis of Lipoxins (LX) /  出産 ... 出産 ... 15-ヒドロキシプロスタグランジンデヒドロゲナーゼ (NAD+) / 15-ヒドロキシプロスタグランジンデヒドロゲナーゼ (NAD+) /  15-ヒドロキシイコサテトラエン酸デヒドロゲナーゼ / regulation of prostaglandin catabolic process / ductus arteriosus closure / thrombin-activated receptor signaling pathway / 15-ヒドロキシイコサテトラエン酸デヒドロゲナーゼ / regulation of prostaglandin catabolic process / ductus arteriosus closure / thrombin-activated receptor signaling pathway /  排卵 / 排卵 /  prostaglandin E receptor activity / prostaglandin E receptor activity /  15-hydroxyprostaglandin dehydrogenase (NAD+) activity / Synthesis of Lipoxins (LX) / 15-hydroxyprostaglandin dehydrogenase (NAD+) activity / Synthesis of Lipoxins (LX) /  出産 / lipoxygenase pathway / Biosynthesis of D-series resolvins / Biosynthesis of E-series 18(S)-resolvins / Synthesis of Prostaglandins (PG) and Thromboxanes (TX) / 出産 / lipoxygenase pathway / Biosynthesis of D-series resolvins / Biosynthesis of E-series 18(S)-resolvins / Synthesis of Prostaglandins (PG) and Thromboxanes (TX) /  酸化還元酵素; CH-OHの結合に対し酸化酵素として働く; NAD又はNADPを用いる / oxidoreductase activity, acting on the CH-OH group of donors, NAD or NADP as acceptor / prostaglandin metabolic process / negative regulation of cell cycle / 酸化還元酵素; CH-OHの結合に対し酸化酵素として働く; NAD又はNADPを用いる / oxidoreductase activity, acting on the CH-OH group of donors, NAD or NADP as acceptor / prostaglandin metabolic process / negative regulation of cell cycle /  NAD+ binding / positive regulation of vascular associated smooth muscle cell proliferation / transforming growth factor beta receptor signaling pathway / NAD+ binding / positive regulation of vascular associated smooth muscle cell proliferation / transforming growth factor beta receptor signaling pathway /  kidney development / female pregnancy / NAD binding / response to estradiol / basolateral plasma membrane / response to ethanol / response to lipopolysaccharide / positive regulation of apoptotic process / extracellular exosome / kidney development / female pregnancy / NAD binding / response to estradiol / basolateral plasma membrane / response to ethanol / response to lipopolysaccharide / positive regulation of apoptotic process / extracellular exosome /  核質 / identical protein binding / 核質 / identical protein binding /  細胞質基質 / 細胞質基質 /  細胞質 細胞質類似検索 - 分子機能 | |||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 2.9 Å クライオ電子顕微鏡法 / 解像度: 2.9 Å | |||||||||
 データ登録者 データ登録者 | Huang W / Taylor DJ | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2023 ジャーナル: Nat Commun / 年: 2023タイトル: Small molecule inhibitors of 15-PGDH exploit a physiologic induced-fit closing system. 著者: Wei Huang / Hongyun Li / Janna Kiselar / Stephen P Fink / Sagar Regmi / Alexander Day / Yiyuan Yuan / Mark Chance / Joseph M Ready / Sanford D Markowitz / Derek J Taylor /  要旨: 15-prostaglandin dehydrogenase (15-PGDH) is a negative regulator of tissue stem cells that acts via enzymatic activity of oxidizing and degrading PGE2, and related eicosanoids, that support stem ...15-prostaglandin dehydrogenase (15-PGDH) is a negative regulator of tissue stem cells that acts via enzymatic activity of oxidizing and degrading PGE2, and related eicosanoids, that support stem cells during tissue repair. Indeed, inhibiting 15-PGDH markedly accelerates tissue repair in multiple organs. Here we have used cryo-electron microscopy to solve the solution structure of native 15-PGDH and of 15-PGDH individually complexed with two distinct chemical inhibitors. These structures identify key 15-PGDH residues that mediate binding to both classes of inhibitors. Moreover, we identify a dynamic 15-PGDH lid domain that closes around the inhibitors, and that is likely fundamental to the physiologic 15-PGDH enzymatic mechanism. We furthermore identify two key residues, F185 and Y217, that act as hinges to regulate lid closing, and which both inhibitors exploit to capture the lid in the closed conformation, thus explaining their sub-nanomolar binding affinities. These findings provide the basis for further development of 15-PGDH targeted drugs as therapeutics for regenerative medicine. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_27025.map.gz emd_27025.map.gz | 32.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-27025-v30.xml emd-27025-v30.xml emd-27025.xml emd-27025.xml | 15.3 KB 15.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_27025.png emd_27025.png | 104.4 KB | ||
| Filedesc metadata |  emd-27025.cif.gz emd-27025.cif.gz | 5.5 KB | ||
| その他 |  emd_27025_half_map_1.map.gz emd_27025_half_map_1.map.gz emd_27025_half_map_2.map.gz emd_27025_half_map_2.map.gz | 59.5 MB 59.5 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-27025 http://ftp.pdbj.org/pub/emdb/structures/EMD-27025 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-27025 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-27025 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_27025.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_27025.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 1.02 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #2
| ファイル | emd_27025_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_27025_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : HUMAN 15-PGDH IN COMPLEX WITH INHIBITOR
| 全体 | 名称: HUMAN 15-PGDH IN COMPLEX WITH INHIBITOR |
|---|---|
| 要素 |
|
-超分子 #1: HUMAN 15-PGDH IN COMPLEX WITH INHIBITOR
| 超分子 | 名称: HUMAN 15-PGDH IN COMPLEX WITH INHIBITOR / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: 15-hydroxyprostaglandin dehydrogenase [NAD(+)]
| 分子 | 名称: 15-hydroxyprostaglandin dehydrogenase [NAD(+)] / タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 光学異性体: LEVO EC番号:  15-ヒドロキシプロスタグランジンデヒドロゲナーゼ (NAD+) 15-ヒドロキシプロスタグランジンデヒドロゲナーゼ (NAD+) |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 27.747906 KDa |
| 組換発現 | 生物種:   Escherichia coli (大腸菌) Escherichia coli (大腸菌) |
| 配列 | 文字列: MVNGKVALVT GAAQGIGRAF AEALLLKGAK VALVDWNLEA GVQCKAALDE QFEPQKTLFI QCDVADQQQL RDTFRKVVDH FGRLDILVN NAGVNNEKNW EKTLQINLVS VISGTYLGLD YMSKQNGGEG GIIINMSSLA GLMPVAQQPV YCASKHGIVG F TRSAALAA ...文字列: MVNGKVALVT GAAQGIGRAF AEALLLKGAK VALVDWNLEA GVQCKAALDE QFEPQKTLFI QCDVADQQQL RDTFRKVVDH FGRLDILVN NAGVNNEKNW EKTLQINLVS VISGTYLGLD YMSKQNGGEG GIIINMSSLA GLMPVAQQPV YCASKHGIVG F TRSAALAA NLMNSGVRLN AICPGFVNTA ILESIEKEEN MGQYIEYKDH IKDMIKYYGI LDPPLIANGL ITLIEDDALN GA IMKITTS KGIHFQDY UniProtKB: 15-hydroxyprostaglandin dehydrogenase [NAD(+)] |
-分子 #2: 1,4-DIHYDRONICOTINAMIDE ADENINE DINUCLEOTIDE
| 分子 | 名称: 1,4-DIHYDRONICOTINAMIDE ADENINE DINUCLEOTIDE / タイプ: ligand / ID: 2 / コピー数: 2 / 式: NAI |
|---|---|
| 分子量 | 理論値: 665.441 Da |
| Chemical component information | 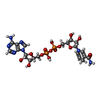 ChemComp-NAI: |
-分子 #3: 2-methyl-6-[7-(piperidine-1-carbonyl)quinoxalin-2-yl]isoquinolin-...
| 分子 | 名称: 2-methyl-6-[7-(piperidine-1-carbonyl)quinoxalin-2-yl]isoquinolin-1(2H)-one タイプ: ligand / ID: 3 / コピー数: 2 / 式: RLD |
|---|---|
| 分子量 | 理論値: 398.457 Da |
| Chemical component information | 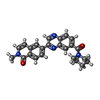 ChemComp-RLD: |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 0.25 µm Bright-field microscopy / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 0.25 µm |
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 平均電子線量: 1.08 e/Å2 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析 #1
画像解析 #1
| 初期モデル | モデルのタイプ: NONE |
|---|---|
| 初期 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
| 最終 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 2.9 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 361366 |
| Image processing ID | 1 |
- 画像解析 #2
画像解析 #2
| 初期モデル | モデルのタイプ: NONE |
|---|---|
| 初期 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
| 最終 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 2.9 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 361366 |
| Image processing ID | 2 |
 ムービー
ムービー コントローラー
コントローラー













 Z
Z Y
Y X
X