+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
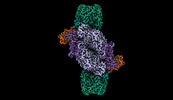
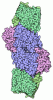
| タイトル | Iron Nitrogenase Complex from Rhodobacter capsulatus | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | nitrogen fixation / Fe nitrogenase / OXIDOREDUCTASE | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報nitrogenase / : / nitrogenase activity / nitrogen fixation / iron-sulfur cluster binding / 4 iron, 4 sulfur cluster binding / iron ion binding / ATP binding / metal ion binding 類似検索 - 分子機能 | |||||||||
| 生物種 |  Rhodobacter capsulatus SB 1003 (バクテリア) Rhodobacter capsulatus SB 1003 (バクテリア) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.35 Å | |||||||||
 データ登録者 データ登録者 | Schmidt FV / Schulz L / Zarzycki J / Prinz S / Erb TJ / Rebelein JG | |||||||||
| 資金援助 |  ドイツ, 2件 ドイツ, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nat Struct Mol Biol / 年: 2024 ジャーナル: Nat Struct Mol Biol / 年: 2024タイトル: Structural insights into the iron nitrogenase complex. 著者: Frederik V Schmidt / Luca Schulz / Jan Zarzycki / Simone Prinz / Niels N Oehlmann / Tobias J Erb / Johannes G Rebelein /  要旨: Nitrogenases are best known for catalyzing the reduction of dinitrogen to ammonia at a complex metallic cofactor. Recently, nitrogenases were shown to reduce carbon dioxide (CO) and carbon monoxide ...Nitrogenases are best known for catalyzing the reduction of dinitrogen to ammonia at a complex metallic cofactor. Recently, nitrogenases were shown to reduce carbon dioxide (CO) and carbon monoxide to hydrocarbons, offering a pathway to recycle carbon waste into hydrocarbon products. Among the three nitrogenase isozymes, the iron nitrogenase has the highest wild-type activity for the reduction of CO, but the molecular architecture facilitating these activities has remained unknown. Here, we report a 2.35-Å cryogenic electron microscopy structure of the ADP·AlF-stabilized iron nitrogenase complex from Rhodobacter capsulatus, revealing an [FeSC-(R)-homocitrate] cluster in the active site. The enzyme complex suggests that the iron nitrogenase G subunit is involved in cluster stabilization and substrate channeling and confers specificity between nitrogenase reductase and catalytic component proteins. Moreover, the structure highlights a different interface between the two catalytic halves of the iron and the molybdenum nitrogenase, potentially influencing the intrasubunit 'communication' and thus the nitrogenase mechanism. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_16890.map.gz emd_16890.map.gz | 108 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-16890-v30.xml emd-16890-v30.xml emd-16890.xml emd-16890.xml | 22.4 KB 22.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_16890_fsc.xml emd_16890_fsc.xml | 12.5 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_16890.png emd_16890.png | 45.1 KB | ||
| Filedesc metadata |  emd-16890.cif.gz emd-16890.cif.gz | 6.9 KB | ||
| その他 |  emd_16890_half_map_1.map.gz emd_16890_half_map_1.map.gz emd_16890_half_map_2.map.gz emd_16890_half_map_2.map.gz | 193.8 MB 193.8 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-16890 http://ftp.pdbj.org/pub/emdb/structures/EMD-16890 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-16890 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-16890 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_16890_validation.pdf.gz emd_16890_validation.pdf.gz | 994.4 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_16890_full_validation.pdf.gz emd_16890_full_validation.pdf.gz | 994 KB | 表示 | |
| XML形式データ |  emd_16890_validation.xml.gz emd_16890_validation.xml.gz | 21.6 KB | 表示 | |
| CIF形式データ |  emd_16890_validation.cif.gz emd_16890_validation.cif.gz | 28 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-16890 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-16890 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-16890 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-16890 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8oieMC  8pbbC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_16890.map.gz / 形式: CCP4 / 大きさ: 209.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_16890.map.gz / 形式: CCP4 / 大きさ: 209.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 0.837 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #1
| ファイル | emd_16890_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_16890_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
+全体 : Iron Nitrogenase Complex from Rhodobacter capsulatus
+超分子 #1: Iron Nitrogenase Complex from Rhodobacter capsulatus
+分子 #1: Nitrogenase protein alpha chain
+分子 #2: Nitrogenase iron-iron protein delta chain
+分子 #3: Nitrogenase iron-iron protein, beta subunit
+分子 #4: Nitrogenase iron protein
+分子 #5: FeFe cofactor
+分子 #6: 3-HYDROXY-3-CARBOXY-ADIPIC ACID
+分子 #7: FE(8)-S(7) CLUSTER
+分子 #8: ADENOSINE-5'-DIPHOSPHATE
+分子 #9: MAGNESIUM ION
+分子 #10: ALUMINUM FLUORIDE
+分子 #11: IRON/SULFUR CLUSTER
+分子 #12: water
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.8 詳細: 50 mM TRIS (pH = 7.8) 200 mM NaCl 5 mM sodium dithionite |
|---|---|
| グリッド | モデル: Quantifoil R2/1 / 材質: COPPER / メッシュ: 300 / 前処理 - タイプ: GLOW DISCHARGE |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 90 % / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 0.5 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー




 Z
Z Y
Y X
X