+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of the Human SHMT1-RNA complex | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Riboregulation / Metabolism / 1 carbon metablism / Moonlighting protein / RNA BINDING PROTEIN / TRANSFERASE | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報cellular response to tetrahydrofolate / Carnitine synthesis / carnitine biosynthetic process / purine nucleobase biosynthetic process / serine binding / aldehyde-lyase activity / L-serine metabolic process / L-serine catabolic process / glycine metabolic process / glycine hydroxymethyltransferase ...cellular response to tetrahydrofolate / Carnitine synthesis / carnitine biosynthetic process / purine nucleobase biosynthetic process / serine binding / aldehyde-lyase activity / L-serine metabolic process / L-serine catabolic process / glycine metabolic process / glycine hydroxymethyltransferase / glycine hydroxymethyltransferase activity / glycine biosynthetic process from serine / Metabolism of folate and pterines / tetrahydrofolate metabolic process / tetrahydrofolate interconversion / dTMP biosynthetic process / small molecule binding / folic acid metabolic process / mRNA regulatory element binding translation repressor activity / cellular response to leukemia inhibitory factor / mRNA 5'-UTR binding / pyridoxal phosphate binding / protein homotetramerization / negative regulation of translation / protein homodimerization activity / mitochondrion / extracellular exosome / nucleoplasm / identical protein binding / nucleus / cytosol / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
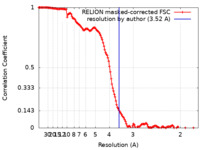
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.52 Å | |||||||||
 データ登録者 データ登録者 | Spizzichino S / Marabelli C / Bharadwaj A / Jakobi AJ / Chaves-Sanjuan A / Giardina G / Bolognesi M / Cutruzzola F | |||||||||
| 資金援助 |  イタリア, 2件 イタリア, 2件
| |||||||||
 引用 引用 |  ジャーナル: Mol Cell / 年: 2024 ジャーナル: Mol Cell / 年: 2024タイトル: Structure-based mechanism of riboregulation of the metabolic enzyme SHMT1. 著者: Sharon Spizzichino / Federica Di Fonzo / Chiara Marabelli / Angela Tramonti / Antonio Chaves-Sanjuan / Alessia Parroni / Giovanna Boumis / Francesca Romana Liberati / Alessio Paone / Linda ...著者: Sharon Spizzichino / Federica Di Fonzo / Chiara Marabelli / Angela Tramonti / Antonio Chaves-Sanjuan / Alessia Parroni / Giovanna Boumis / Francesca Romana Liberati / Alessio Paone / Linda Celeste Montemiglio / Matteo Ardini / Arjen J Jakobi / Alok Bharadwaj / Paolo Swuec / Gian Gaetano Tartaglia / Alessandro Paiardini / Roberto Contestabile / Antonello Mai / Dante Rotili / Francesco Fiorentino / Alberto Macone / Alessandra Giorgi / Giancarlo Tria / Serena Rinaldo / Martino Bolognesi / Giorgio Giardina / Francesca Cutruzzolà /   要旨: RNA can directly control protein activity in a process called riboregulation; only a few mechanisms of riboregulation have been described in detail, none of which have been characterized on ...RNA can directly control protein activity in a process called riboregulation; only a few mechanisms of riboregulation have been described in detail, none of which have been characterized on structural grounds. Here, we present a comprehensive structural, functional, and phylogenetic analysis of riboregulation of cytosolic serine hydroxymethyltransferase (SHMT1), the enzyme interconverting serine and glycine in one-carbon metabolism. We have determined the cryoelectron microscopy (cryo-EM) structure of human SHMT1 in its free- and RNA-bound states, and we show that the RNA modulator competes with polyglutamylated folates and acts as an allosteric switch, selectively altering the enzyme's reactivity vs. serine. In addition, we identify the tetrameric assembly and a flap structural motif as key structural elements necessary for binding of RNA to eukaryotic SHMT1. The results presented here suggest that riboregulation may have played a role in evolution of eukaryotic SHMT1 and in compartmentalization of one-carbon metabolism. Our findings provide insights for RNA-based therapeutic strategies targeting this cancer-linked metabolic pathway. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_15065.map.gz emd_15065.map.gz | 2.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-15065-v30.xml emd-15065-v30.xml emd-15065.xml emd-15065.xml | 20 KB 20 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_15065_fsc.xml emd_15065_fsc.xml | 14.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_15065.png emd_15065.png | 144.4 KB | ||
| Filedesc metadata |  emd-15065.cif.gz emd-15065.cif.gz | 6.8 KB | ||
| その他 |  emd_15065_half_map_1.map.gz emd_15065_half_map_1.map.gz emd_15065_half_map_2.map.gz emd_15065_half_map_2.map.gz | 194.7 MB 194.8 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-15065 http://ftp.pdbj.org/pub/emdb/structures/EMD-15065 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-15065 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-15065 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_15065_validation.pdf.gz emd_15065_validation.pdf.gz | 673.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_15065_full_validation.pdf.gz emd_15065_full_validation.pdf.gz | 672.8 KB | 表示 | |
| XML形式データ |  emd_15065_validation.xml.gz emd_15065_validation.xml.gz | 22.2 KB | 表示 | |
| CIF形式データ |  emd_15065_validation.cif.gz emd_15065_validation.cif.gz | 28.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15065 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15065 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15065 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15065 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8a11MC  8r7hC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_15065.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_15065.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.889 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #2
| ファイル | emd_15065_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_15065_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : human SHMT1 in complex with RNA (SHMT2 5' UTR 1-50)
| 全体 | 名称: human SHMT1 in complex with RNA (SHMT2 5' UTR 1-50) |
|---|---|
| 要素 |
|
-超分子 #1: human SHMT1 in complex with RNA (SHMT2 5' UTR 1-50)
| 超分子 | 名称: human SHMT1 in complex with RNA (SHMT2 5' UTR 1-50) / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 / 詳細: SHMT1= homotetramer of 53kDa subunits |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 53 kDa/nm |
-分子 #1: Serine hydroxymethyltransferase, cytosolic
| 分子 | 名称: Serine hydroxymethyltransferase, cytosolic / タイプ: protein_or_peptide / ID: 1 詳細: first 3 N-ter residues come from removal of His-tag. Sequence numbering starts from first M residue. K257 is covalently bound to PLP forming an internal aldimine (LLP) コピー数: 4 / 光学異性体: LEVO / EC番号: glycine hydroxymethyltransferase |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 53.434797 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: GSHMTMPVNG AHKDADLWSS HDKMLAQPLK DSDVEVYNII KKESNRQRVG LELIASENFA SRAVLEALGS CLNNKYSEGY PGQRYYGGT EFIDELETLC QKRALQAYKL DPQCWGVNVQ PYSGSPANFA VYTALVEPHG RIMGLDLPDG GHLTHGFMTD K KKISATSI ...文字列: GSHMTMPVNG AHKDADLWSS HDKMLAQPLK DSDVEVYNII KKESNRQRVG LELIASENFA SRAVLEALGS CLNNKYSEGY PGQRYYGGT EFIDELETLC QKRALQAYKL DPQCWGVNVQ PYSGSPANFA VYTALVEPHG RIMGLDLPDG GHLTHGFMTD K KKISATSI FFESMPYKVN PDTGYINYDQ LEENARLFHP KLIIAGTSCY SRNLEYARLR KIADENGAYL MADMAHISGL VA AGVVPSP FEHCHVVTTT THKTLRGCRA GMIFYRKGVK SVDPKTGKEI LYNLESLINS AVFPGLQGGP HNHAIAGVAV ALK QAMTLE FKVYQHQVVA NCRALSEALT ELGYKIVTGG SDNHLILVDL RSKGTDGGRA EKVLEACSIA CNKNTCPGDR SALR PSGLR LGTPALTSRG LLEKDFQKVA HFIHRGIELT LQIQSDTGVR ATLKEFKERL AGDKYQAAVQ ALREEVESFA SLFPL PGLP DF UniProtKB: Serine hydroxymethyltransferase, cytosolic |
-分子 #2: PYRIDOXAL-5'-PHOSPHATE
| 分子 | 名称: PYRIDOXAL-5'-PHOSPHATE / タイプ: ligand / ID: 2 / コピー数: 3 / 式: PLP |
|---|---|
| 分子量 | 理論値: 247.142 Da |
| Chemical component information |  ChemComp-PLP: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.3 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.2 構成要素:
| |||||||||
| グリッド | モデル: Quantifoil / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 30 sec. / 前処理 - 雰囲気: AIR | |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV / 詳細: blotted for 4 seconds before plunging. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TALOS ARCTICA |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: COUNTING / 撮影したグリッド数: 1 / 実像数: 5450 / 平均電子線量: 40.0 e/Å2 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 0.5 µm / 倍率(公称値): 120000 |
| 試料ステージ | 試料ホルダーモデル: OTHER / ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー





 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)