+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of yeast SWR1C subunit Swc5 bound to the nucleosome, 3D class 0 | |||||||||||||||
 マップデータ マップデータ | Map of 3D class 0 (Fig. 6B, S1E) | |||||||||||||||
 試料 試料 |
| |||||||||||||||
 キーワード キーワード | Chromatin / Remodeler / Complex / Histone / GENE REGULATION | |||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報HATs acetylate histones / Condensation of Prophase Chromosomes / SIRT1 negatively regulates rRNA expression / Activated PKN1 stimulates transcription of AR (androgen receptor) regulated genes KLK2 and KLK3 / Assembly of the ORC complex at the origin of replication / Swr1 complex / HDACs deacetylate histones / Recruitment and ATM-mediated phosphorylation of repair and signaling proteins at DNA double strand breaks / replication fork protection complex / Oxidative Stress Induced Senescence ...HATs acetylate histones / Condensation of Prophase Chromosomes / SIRT1 negatively regulates rRNA expression / Activated PKN1 stimulates transcription of AR (androgen receptor) regulated genes KLK2 and KLK3 / Assembly of the ORC complex at the origin of replication / Swr1 complex / HDACs deacetylate histones / Recruitment and ATM-mediated phosphorylation of repair and signaling proteins at DNA double strand breaks / replication fork protection complex / Oxidative Stress Induced Senescence / RMTs methylate histone arginines / postreplication repair / RNA Polymerase I Promoter Escape / Estrogen-dependent gene expression / heterochromatin organization / Ub-specific processing proteases / nucleosomal DNA binding / structural constituent of chromatin / nucleosome / nucleosome assembly / chromatin organization / chromatin remodeling / protein heterodimerization activity / DNA repair / regulation of DNA-templated transcription / chromatin / negative regulation of transcription by RNA polymerase II / DNA binding / nucleoplasm / nucleus / cytosol 類似検索 - 分子機能 | |||||||||||||||
| 生物種 |  | |||||||||||||||
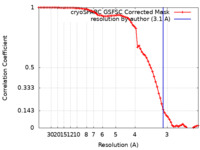
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.1 Å | |||||||||||||||
 データ登録者 データ登録者 | Eek P / Tan S | |||||||||||||||
| 資金援助 |  米国, 米国,  Estonia, 4件 Estonia, 4件
| |||||||||||||||
 引用 引用 |  ジャーナル: Elife / 年: 2024 ジャーナル: Elife / 年: 2024タイトル: Dual engagement of the nucleosomal acidic patches is essential for deposition of histone H2A.Z by SWR1C. 著者: Alexander S Baier / Nathan Gioacchini / Priit Eek / Erik M Leith / Song Tan / Craig L Peterson /   要旨: The yeast SWR1C chromatin remodeling enzyme catalyzes the ATP-dependent exchange of nucleosomal histone H2A for the histone variant H2A.Z, a key variant involved in a multitude of nuclear functions. ...The yeast SWR1C chromatin remodeling enzyme catalyzes the ATP-dependent exchange of nucleosomal histone H2A for the histone variant H2A.Z, a key variant involved in a multitude of nuclear functions. How the 14-subunit SWR1C engages the nucleosomal substrate remains largely unknown. Studies on the ISWI, CHD1, and SWI/SNF families of chromatin remodeling enzymes have demonstrated key roles for the nucleosomal acidic patch for remodeling activity, however a role for this nucleosomal epitope in nucleosome editing by SWR1C has not been tested. Here, we employ a variety of biochemical assays to demonstrate an essential role for the acidic patch in the H2A.Z exchange reaction. Utilizing asymmetrically assembled nucleosomes, we demonstrate that the acidic patches on each face of the nucleosome are required for SWR1C-mediated dimer exchange, suggesting SWR1C engages the nucleosome in a 'pincer-like' conformation, engaging both patches simultaneously. Loss of a single acidic patch results in loss of high affinity nucleosome binding and nucleosomal stimulation of ATPase activity. We identify a conserved arginine-rich motif within the Swc5 subunit that binds the acidic patch and is key for dimer exchange activity. In addition, our cryoEM structure of a Swc5-nucleosome complex suggests that promoter proximal, histone H2B ubiquitylation may regulate H2A.Z deposition. Together these findings provide new insights into how SWR1C engages its nucleosomal substrate to promote efficient H2A.Z deposition. #1:  ジャーナル: Elife / 年: 2024 ジャーナル: Elife / 年: 2024タイトル: Dual engagement of the nucleosomal acidic patches is essential for deposition of histone H2A.Z by SWR1C 著者: Baier AS / Gioacchini N / Eek P / Leith EM / Song T / Peterson CL | |||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_41839.map.gz emd_41839.map.gz | 19.5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-41839-v30.xml emd-41839-v30.xml emd-41839.xml emd-41839.xml | 25.3 KB 25.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_41839_fsc.xml emd_41839_fsc.xml | 7.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_41839.png emd_41839.png | 180.4 KB | ||
| マスクデータ |  emd_41839_msk_1.map emd_41839_msk_1.map | 38.4 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-41839.cif.gz emd-41839.cif.gz | 6.3 KB | ||
| その他 |  emd_41839_half_map_1.map.gz emd_41839_half_map_1.map.gz emd_41839_half_map_2.map.gz emd_41839_half_map_2.map.gz | 35.7 MB 35.7 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-41839 http://ftp.pdbj.org/pub/emdb/structures/EMD-41839 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-41839 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-41839 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_41839_validation.pdf.gz emd_41839_validation.pdf.gz | 931.4 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_41839_full_validation.pdf.gz emd_41839_full_validation.pdf.gz | 931 KB | 表示 | |
| XML形式データ |  emd_41839_validation.xml.gz emd_41839_validation.xml.gz | 14.5 KB | 表示 | |
| CIF形式データ |  emd_41839_validation.cif.gz emd_41839_validation.cif.gz | 18.9 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-41839 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-41839 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-41839 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-41839 | HTTPS FTP |
-関連構造データ
| 関連構造データ | C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_41839.map.gz / 形式: CCP4 / 大きさ: 38.4 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_41839.map.gz / 形式: CCP4 / 大きさ: 38.4 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Map of 3D class 0 (Fig. 6B, S1E) | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.182 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_41839_msk_1.map emd_41839_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Half map B of class 0
| ファイル | emd_41839_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map B of class 0 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Half map A of class 0
| ファイル | emd_41839_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map A of class 0 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Swc5 in complex with nucleosome core particle
| 全体 | 名称: Swc5 in complex with nucleosome core particle |
|---|---|
| 要素 |
|
-超分子 #1: Swc5 in complex with nucleosome core particle
| 超分子 | 名称: Swc5 in complex with nucleosome core particle / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種: |
-分子 #1: Histone H3.2
| 分子 | 名称: Histone H3.2 / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種: |
| 組換発現 | 生物種:  |
| 配列 | 文字列: ARTKQTARKS TGGKAPRKQL ATKAARKSAP ATGGVKKPHR YRPGTVALRE IRRYQKSTEL LIRKLPFQRL VREIAQDFKT DLRFQSSAVM ALQEASEAYL VALFEDTNLC AIHAKRVTIM PKDIQLARRI RGERA UniProtKB: Histone H3.2 |
-分子 #2: Histone H4
| 分子 | 名称: Histone H4 / タイプ: protein_or_peptide / ID: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種: |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MSGRGKGGKG LGKGGAKRHR KVLRDNIQGI TKPAIRRLAR RGGVKRISGL IYEETRGVLK VFLENVIRDA VTYTEHAKRK TVTAMDVVYA LKRQGRTLYG FGG UniProtKB: Histone H4 |
-分子 #3: Histone H2A.1
| 分子 | 名称: Histone H2A.1 / タイプ: protein_or_peptide / ID: 3 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
| 配列 | 文字列: SGGKGGKAGS AAKASQSRSA KAGLTFPVGR VHRLLRRGNY AQRIGSGAPV YLTAVLEYLA AEILELAGNA ARDNKKTRII PRHLQLAIRN DDELNKLLGN VTIAQGGVLP NIHQNLLPKK SAKATKASQE L UniProtKB: Histone H2A.1 |
-分子 #4: Histone H2B.1
| 分子 | 名称: Histone H2B.1 / タイプ: protein_or_peptide / ID: 4 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
| 配列 | 文字列: SAKAEKKPAS KAPAEKKPAA KKTSTSTDGK KRSKARKETY SSYIYKVLKQ THPDTGISQK SMSILNSFVN DIFERIATEA SKLAAYNKKS TISAREIQTA VRLILPGELA KHAVSEGTRA VTKYSSSTQA UniProtKB: Histone H2B.1 |
-分子 #5: SWR1-complex protein 5
| 分子 | 名称: SWR1-complex protein 5 / タイプ: protein_or_peptide / ID: 5 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
| 配列 | 文字列: RGSHHHHHHG SKTRRARQAE EEYAKTHKYE SLTVESIPAK VNSIWEELQE ASKNRLLSSS GKVGSVLDGS KEARSTTAAQ QEDKILIERN YKFAGETVHE KKWVSRSSAE GQEYLNSLKF KQQAPAAPVQ LEKAVRTKSN ESRQHLRRPL KRPPLLEQII SGGLRPKLTT ...文字列: RGSHHHHHHG SKTRRARQAE EEYAKTHKYE SLTVESIPAK VNSIWEELQE ASKNRLLSSS GKVGSVLDGS KEARSTTAAQ QEDKILIERN YKFAGETVHE KKWVSRSSAE GQEYLNSLKF KQQAPAAPVQ LEKAVRTKSN ESRQHLRRPL KRPPLLEQII SGGLRPKLTT LEKSQLDWAS YVDRAGLNDE LVLHNKDGFL ARQEFLQRVG SAEDERYKEL RRQQLAQQLQ QDNEAS UniProtKB: SWR1-complex protein 5 |
-分子 #6: Widom 601 forward DNA
| 分子 | 名称: Widom 601 forward DNA / タイプ: dna / ID: 6 / 分類: DNA |
|---|---|
| 由来(天然) | 生物種: synthetic construct (人工物) |
| 配列 | 文字列: ATCGAGAATC CCGGTGCCGA GGCCGCTCAA TTGGTCGTAG ACAGCTCTAG CACCGCTTAA ACGCACGTAC GCGCTGTCCC CCGCGTTTTA ACCGCCAAGG GGATTACTCC CTAGTCTCCA GGCACGTGTC AGATATATAC ATCCGAT |
-分子 #7: Widom 601 reverse DNA
| 分子 | 名称: Widom 601 reverse DNA / タイプ: dna / ID: 7 / 分類: DNA |
|---|---|
| 由来(天然) | 生物種: synthetic construct (人工物) |
| 配列 | 文字列: ATCGGATGTA TATATCTGAC ACGTGCCTGG AGACTAGGGA GTAATCCCCT TGGCGGTTAA AACGCGGGGG ACAGCGCGTA CGTGCGTTTA AGCGGTGCTA GAGCTGTCTA CGACCAATTG AGCGGCCTCG GCACCGGGAT TCTCGAT |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.9 mg/mL | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
| |||||||||||||||
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 45 sec. / 前処理 - 雰囲気: AIR / 詳細: 15 mA with PELCO easiGlow | |||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV | |||||||||||||||
| 詳細 | Chemically cross-linked with glutaraldehyde using the GraFix method. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 撮影したグリッド数: 1 / 実像数: 13855 / 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm 最大 デフォーカス(公称値): 2.8000000000000003 µm 最小 デフォーカス(公称値): 0.8 µm / 倍率(公称値): 29000 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー
















 Z
Z Y
Y X
X