+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 7no1 | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
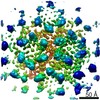
| タイトル | Structure of the mature RSV CA lattice: T=3 CA icosahedron | |||||||||||||||
 要素 要素 | Capsid protein p27, alternate cleaved 1 | |||||||||||||||
 キーワード キーワード | VIRAL PROTEIN / Retrovirus / Rous sarcoma virus / capsid protein / IP6 | |||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報host cell nucleoplasm / viral procapsid maturation / host cell nucleolus / 加水分解酵素; プロテアーゼ; ペプチド結合加水分解酵素; アスパラギン酸プロテアーゼ / viral capsid / nucleic acid binding / structural constituent of virion / aspartic-type endopeptidase activity / host cell plasma membrane / proteolysis ...host cell nucleoplasm / viral procapsid maturation / host cell nucleolus / 加水分解酵素; プロテアーゼ; ペプチド結合加水分解酵素; アスパラギン酸プロテアーゼ / viral capsid / nucleic acid binding / structural constituent of virion / aspartic-type endopeptidase activity / host cell plasma membrane / proteolysis / zinc ion binding / membrane 類似検索 - 分子機能 | |||||||||||||||
| 生物種 |  Rous sarcoma virus (ラウス肉腫ウイルス) Rous sarcoma virus (ラウス肉腫ウイルス) | |||||||||||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 7.6 Å | |||||||||||||||
 データ登録者 データ登録者 | Obr, M. / Ricana, C.L. / Nikulin, N. / Feathers, J.-P.R. / Klanschnig, M. / Thader, A. / Johnson, M.C. / Vogt, V.M. / Schur, F.K.M. / Dick, R.A. | |||||||||||||||
| 資金援助 |  オーストリア, オーストリア,  米国, 4件 米国, 4件
| |||||||||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2021 ジャーナル: Nat Commun / 年: 2021タイトル: Structure of the mature Rous sarcoma virus lattice reveals a role for IP6 in the formation of the capsid hexamer. 著者: Martin Obr / Clifton L Ricana / Nadia Nikulin / Jon-Philip R Feathers / Marco Klanschnig / Andreas Thader / Marc C Johnson / Volker M Vogt / Florian K M Schur / Robert A Dick /   要旨: Inositol hexakisphosphate (IP6) is an assembly cofactor for HIV-1. We report here that IP6 is also used for assembly of Rous sarcoma virus (RSV), a retrovirus from a different genus. IP6 is ~100-fold ...Inositol hexakisphosphate (IP6) is an assembly cofactor for HIV-1. We report here that IP6 is also used for assembly of Rous sarcoma virus (RSV), a retrovirus from a different genus. IP6 is ~100-fold more potent at promoting RSV mature capsid protein (CA) assembly than observed for HIV-1 and removal of IP6 in cells reduces infectivity by 100-fold. Here, visualized by cryo-electron tomography and subtomogram averaging, mature capsid-like particles show an IP6-like density in the CA hexamer, coordinated by rings of six lysines and six arginines. Phosphate and IP6 have opposing effects on CA in vitro assembly, inducing formation of T = 1 icosahedrons and tubes, respectively, implying that phosphate promotes pentamer and IP6 hexamer formation. Subtomogram averaging and classification optimized for analysis of pleomorphic retrovirus particles reveal that the heterogeneity of mature RSV CA polyhedrons results from an unexpected, intrinsic CA hexamer flexibility. In contrast, the CA pentamer forms rigid units organizing the local architecture. These different features of hexamers and pentamers determine the structural mechanism to form CA polyhedrons of variable shape in mature RSV particles. | |||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  7no1.cif.gz 7no1.cif.gz | 90.3 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb7no1.ent.gz pdb7no1.ent.gz | 55 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  7no1.json.gz 7no1.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  7no1_validation.pdf.gz 7no1_validation.pdf.gz | 791 KB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  7no1_full_validation.pdf.gz 7no1_full_validation.pdf.gz | 790.6 KB | 表示 | |
| XML形式データ |  7no1_validation.xml.gz 7no1_validation.xml.gz | 20.5 KB | 表示 | |
| CIF形式データ |  7no1_validation.cif.gz 7no1_validation.cif.gz | 30.5 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/no/7no1 https://data.pdbj.org/pub/pdb/validation_reports/no/7no1 ftp://data.pdbj.org/pub/pdb/validation_reports/no/7no1 ftp://data.pdbj.org/pub/pdb/validation_reports/no/7no1 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  12486MC  7no0C  7no2C  7no3C  7no4C  7no5C  7no6C  7no7C  7no8C  7no9C  7noaC  7nobC  7nocC  7nodC  7noeC  7nofC  7nogC  7nohC  7noiC  7nojC  7nokC  7nolC  7nomC  7nonC  7nooC  7nopC  7noqC M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 | x 60
|
- 要素
要素
| #1: タンパク質 | 分子量: 24773.594 Da / 分子数: 3 / 由来タイプ: 組換発現 由来: (組換発現)  Rous sarcoma virus (strain Prague C) (ラウス肉腫ウイルス) Rous sarcoma virus (strain Prague C) (ラウス肉腫ウイルス)株: Prague C / 遺伝子: gag / 発現宿主:  |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: Rous sarcoma virus - Prague C / タイプ: VIRUS / Entity ID: all / 由来: RECOMBINANT |
|---|---|
| 分子量 | 実験値: NO |
| 由来(天然) | 生物種:  Rous sarcoma virus - Prague C (ラウス肉腫ウイルス) Rous sarcoma virus - Prague C (ラウス肉腫ウイルス) |
| 由来(組換発現) | 生物種:  |
| ウイルスについての詳細 | 中空か: YES / エンベロープを持つか: NO / 単離: OTHER / タイプ: VIRUS-LIKE PARTICLE |
| ウイルス殻 | 名称: T=3 icosahedron |
| 緩衝液 | pH: 8 |
| 緩衝液成分 | 濃度: 1 M / 名称: sodium phosphate / 式: NaPi |
| 試料 | 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES |
| 試料支持 | グリッドの材料: COPPER / グリッドのサイズ: 300 divisions/in. / グリッドのタイプ: C-flat-2/2 |
| 急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE / 湿度: 95 % / 凍結前の試料温度: 277 K / 詳細: blot time = 2.5s blot force = 0 |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TECNAI ARCTICA |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 200 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 200 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 倍率(公称値): 63000 X / 最大 デフォーカス(公称値): 1500 nm / 最小 デフォーカス(公称値): 800 nm / Cs: 2.7 mm / C2レンズ絞り径: 50 µm |
| 試料ホルダ | 凍結剤: NITROGEN 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 撮影 | 平均露光時間: 3 sec. / 電子線照射量: 50 e/Å2 フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 実像数: 2394 |
| 電子光学装置 | エネルギーフィルター名称: GIF Bioquantum / エネルギーフィルタースリット幅: 20 eV |
| 画像スキャン | 横: 5760 / 縦: 4092 |
- 解析
解析
| EMソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||||||||||||||||||
| 粒子像の選択 | 選択した粒子像数: 2309 / 詳細: Three rounds of auto-picking and 2D classification | ||||||||||||||||||||||||||||||||||||||||
| 対称性 | 点対称性: I (正20面体型対称) | ||||||||||||||||||||||||||||||||||||||||
| 3次元再構成 | 解像度: 7.6 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 406 / 対称性のタイプ: POINT | ||||||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | プロトコル: RIGID BODY FIT | ||||||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | PDB-ID: 7NO0 Accession code: 7NO0 / Source name: PDB / タイプ: experimental model |
 ムービー
ムービー コントローラー
コントローラー






































 PDBj
PDBj