+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-6559 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-electron microscopy structure of ribosome-bound initiation factor 2 70S IC II state | |||||||||
 マップデータ マップデータ | Reconstruction of the 70S-fMet-tRNAiMet-IF2-GDPNP complex, IC II state | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | translation initiation / ribosome / initiation / Initiation Factor 2 / 70S initiation complex / prokaryotes / GTPase / translation GTPAse | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報guanosine tetraphosphate binding / stringent response / transcription antitermination factor activity, RNA binding / ornithine decarboxylase inhibitor activity / ribosomal small subunit binding / misfolded RNA binding / Group I intron splicing / RNA folding / transcriptional attenuation / endoribonuclease inhibitor activity ...guanosine tetraphosphate binding / stringent response / transcription antitermination factor activity, RNA binding / ornithine decarboxylase inhibitor activity / ribosomal small subunit binding / misfolded RNA binding / Group I intron splicing / RNA folding / transcriptional attenuation / endoribonuclease inhibitor activity / positive regulation of ribosome biogenesis / RNA-binding transcription regulator activity / translational termination / four-way junction DNA binding / negative regulation of cytoplasmic translation / DnaA-L2 complex / regulation of mRNA stability / translation initiation factor activity / translation repressor activity / negative regulation of translational initiation / negative regulation of DNA-templated DNA replication initiation / mRNA regulatory element binding translation repressor activity / response to cold / regulation of DNA-templated transcription elongation / positive regulation of RNA splicing / transcription elongation factor complex / cytosolic ribosome assembly / response to reactive oxygen species / ribosome assembly / assembly of large subunit precursor of preribosome / transcription antitermination / DNA endonuclease activity / molecular condensate scaffold activity / translational initiation / regulation of cell growth / response to radiation / DNA-templated transcription termination / maintenance of translational fidelity / mRNA 5'-UTR binding / regulation of translation / large ribosomal subunit / ribosomal small subunit assembly / transferase activity / ribosome biogenesis / protein folding / ribosome binding / ribosomal small subunit biogenesis / 5S rRNA binding / small ribosomal subunit / ribosomal large subunit assembly / small ribosomal subunit rRNA binding / cytosolic small ribosomal subunit / large ribosomal subunit rRNA binding / cytosolic large ribosomal subunit / cytoplasmic translation / tRNA binding / negative regulation of translation / rRNA binding / structural constituent of ribosome / ribosome / translation / response to antibiotic / negative regulation of DNA-templated transcription / hydrolase activity / mRNA binding / GTPase activity / GTP binding / DNA binding / RNA binding / zinc ion binding / membrane / cytoplasm / cytosol 類似検索 - 分子機能 | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.7 Å | |||||||||
 データ登録者 データ登録者 | Sprink T / Ramrath DJF / Yamamoto H / Yamamoto K / Loerke J / Ismer J / Hildebrand PW / Scheerer P / Buerger J / Mielke T / Spahn CMT | |||||||||
 引用 引用 |  ジャーナル: Sci Adv / 年: 2016 ジャーナル: Sci Adv / 年: 2016タイトル: Structures of ribosome-bound initiation factor 2 reveal the mechanism of subunit association. 著者: Thiemo Sprink / David J F Ramrath / Hiroshi Yamamoto / Kaori Yamamoto / Justus Loerke / Jochen Ismer / Peter W Hildebrand / Patrick Scheerer / Jörg Bürger / Thorsten Mielke / Christian M T Spahn /  要旨: Throughout the four phases of protein biosynthesis-initiation, elongation, termination, and recycling-the ribosome is controlled and regulated by at least one specified translational guanosine ...Throughout the four phases of protein biosynthesis-initiation, elongation, termination, and recycling-the ribosome is controlled and regulated by at least one specified translational guanosine triphosphatase (trGTPase). Although the structural basis for trGTPase interaction with the ribosome has been solved for the last three steps of translation, the high-resolution structure for the key initiation trGTPase, initiation factor 2 (IF2), complexed with the ribosome, remains elusive. We determine the structure of IF2 complexed with a nonhydrolyzable guanosine triphosphate analog and initiator fMet-tRNAi (Met) in the context of the Escherichia coli ribosome to 3.7-Å resolution using cryo-electron microscopy. The structural analysis reveals previously unseen intrinsic conformational modes of the 70S initiation complex, establishing the mutual interplay of IF2 and initator transfer RNA (tRNA) with the ribsosome and providing the structural foundation for a mechanistic understanding of the final steps of translation initiation. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_6559.map.gz emd_6559.map.gz | 163.8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-6559-v30.xml emd-6559-v30.xml emd-6559.xml emd-6559.xml | 13.1 KB 13.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_6559.png emd_6559.png | 347 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-6559 http://ftp.pdbj.org/pub/emdb/structures/EMD-6559 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-6559 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-6559 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_6559.map.gz / 形式: CCP4 / 大きさ: 173.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_6559.map.gz / 形式: CCP4 / 大きさ: 173.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Reconstruction of the 70S-fMet-tRNAiMet-IF2-GDPNP complex, IC II state | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.025 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
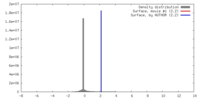
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Escherichia coli Initiation Factor 2 stalled on Escherichia coli ...
| 全体 | 名称: Escherichia coli Initiation Factor 2 stalled on Escherichia coli 70S ribosomes by the non-hydrolysable GTP analogue GDPNP in the presence of fMet-tRNAiMet and mRNA |
|---|---|
| 要素 |
|
-超分子 #1000: Escherichia coli Initiation Factor 2 stalled on Escherichia coli ...
| 超分子 | 名称: Escherichia coli Initiation Factor 2 stalled on Escherichia coli 70S ribosomes by the non-hydrolysable GTP analogue GDPNP in the presence of fMet-tRNAiMet and mRNA タイプ: sample / ID: 1000 / Number unique components: 3 |
|---|---|
| 分子量 | 実験値: 2.5 MDa / 理論値: 2.6 MDa |
-超分子 #1: 70S ribosome
| 超分子 | 名称: 70S ribosome / タイプ: complex / ID: 1 / Name.synonym: 70S / 組換発現: No / データベース: NCBI / Ribosome-details: ribosome-prokaryote: ALL |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 実験値: 2.5 MDa / 理論値: 2.6 MDa |
-分子 #1: fMet-tRNAiMet
| 分子 | 名称: fMet-tRNAiMet / タイプ: rna / ID: 1 / Name.synonym: initiator tRNA / 分類: TRANSFER / Structure: DOUBLE HELIX / Synthetic?: No |
|---|---|
| 由来(天然) | 生物種:  |
-分子 #2: Initiation Factor 2
| 分子 | 名称: Initiation Factor 2 / タイプ: protein_or_peptide / ID: 2 / Name.synonym: IF2 / 詳細: bound to GNPPNP / コピー数: 1 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 実験値: 97 KDa / 理論値: 97 KDa |
| 組換発現 | 生物種:  |
| 配列 | UniProtKB: Translation initiation factor IF-2 |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 詳細: 20 mM HEPES-KOH, pH 7.5, 15 mM magnesium acetate, 150 mM potassium acetate, 4 mM 2-mercapthoethanol, 2 mM spermidine, 0.05 mM spermine |
|---|---|
| グリッド | 詳細: Quantifoil R3-3 Cu 300 mesh with 2 nm carbon support film |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / 装置: FEI VITROBOT MARK I / 手法: Blot for 2-4 seconds before plunging. |
- 電子顕微鏡法 #1
電子顕微鏡法 #1
| Microscopy ID | 1 |
|---|---|
| 顕微鏡 | FEI POLARA 300 |
| 日付 | 2013年8月26日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 実像数: 918 / 平均電子線量: 20 e/Å2 / 詳細: Automated data collection using Leginon |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 39000 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.0 mm / 最大 デフォーカス(公称値): 7.18 µm / 最小 デフォーカス(公称値): 0.64 µm / 倍率(公称値): 31000 |
| 試料ステージ | 試料ホルダーモデル: GATAN LIQUID NITROGEN |
| 実験機器 |  モデル: Tecnai Polara / 画像提供: FEI Company |
- 電子顕微鏡法 #2
電子顕微鏡法 #2
| Microscopy ID | 2 |
|---|---|
| 顕微鏡 | FEI POLARA 300 |
| 日付 | 2015年6月10日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 実像数: 2797 / 平均電子線量: 20 e/Å2 / 詳細: Automated data collection using Leginon |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 39000 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.0 mm / 最大 デフォーカス(公称値): 7.57 µm / 最小 デフォーカス(公称値): 0.19 µm / 倍率(公称値): 31000 |
| 試料ステージ | 試料ホルダーモデル: GATAN LIQUID NITROGEN |
| 実験機器 |  モデル: Tecnai Polara / 画像提供: FEI Company |
- 画像解析
画像解析
| 詳細 | To avoid overfitting, the data was refined in a resolution-limited scheme using SPIDER. |
|---|---|
| CTF補正 | 詳細: CTFFIND4 |
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 3.7 Å / 解像度の算出法: OTHER / ソフトウェア - 名称: EMAN2, CTFFIND4, SPIDER, SPARX 詳細: Final maps were calculated from two combined datasets. To avoid overfitting, the data were refined in a resolution-limited scheme using SPIDER. 使用した粒子像数: 54585 |
 ムービー
ムービー コントローラー
コントローラー




























 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)