+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Mechanistic Insights Revealed by YbtPQ in the Occluded State | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | ABC importer / siderophore / occluded / MEMBRANE PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報加水分解酵素; 酸無水物に作用; 酸無水物に作用・物質の膜輸送を触媒する / ABC-type transporter activity / ATP hydrolysis activity / ATP binding / membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.1 Å | |||||||||
 データ登録者 データ登録者 | Hu W / Parkinson C / Zheng H | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Biomolecules / 年: 2024 ジャーナル: Biomolecules / 年: 2024タイトル: Mechanistic Insights Revealed by YbtPQ in the Occluded State. 著者: Wenxin Hu / Chance Parkinson / Hongjin Zheng /  要旨: Recently, several ATP-binding cassette (ABC) importers have been found to adopt the typical fold of type IV ABC exporters. Presumably, these importers would function under the transport scheme of ...Recently, several ATP-binding cassette (ABC) importers have been found to adopt the typical fold of type IV ABC exporters. Presumably, these importers would function under the transport scheme of "alternating access" like those exporters, cycling through inward-open, occluded, and outward-open conformations. Understanding how the exporter-like importers move substrates in the opposite direction requires structural studies on all the major conformations. To shed light on this, here we report the structure of yersiniabactin importer YbtPQ from uropathogenic in the occluded conformation trapped by ADP-vanadate (ADP-Vi) at a 3.1 Å resolution determined by cryo-electron microscopy. The structure shows unusual local rearrangements in multiple helices and loops in its transmembrane domains (TMDs). In addition, the dimerization of the nucleotide-binding domains (NBDs) promoted by the vanadate trapping is highlighted by the "screwdriver" action at one of the two hinge points. These structural observations are rare and thus provide valuable information to understand the structural plasticity of the exporter-like ABC importers. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_43498.map.gz emd_43498.map.gz | 5.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-43498-v30.xml emd-43498-v30.xml emd-43498.xml emd-43498.xml | 15.4 KB 15.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_43498.png emd_43498.png | 93 KB | ||
| Filedesc metadata |  emd-43498.cif.gz emd-43498.cif.gz | 6.2 KB | ||
| その他 |  emd_43498_half_map_1.map.gz emd_43498_half_map_1.map.gz emd_43498_half_map_2.map.gz emd_43498_half_map_2.map.gz | 115.8 MB 115.8 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-43498 http://ftp.pdbj.org/pub/emdb/structures/EMD-43498 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-43498 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-43498 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8vsiMC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_43498.map.gz / 形式: CCP4 / 大きさ: 5.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_43498.map.gz / 形式: CCP4 / 大きさ: 5.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 0.83 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #1
| ファイル | emd_43498_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
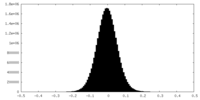
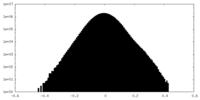
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_43498_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : YbtPQ
| 全体 | 名称: YbtPQ |
|---|---|
| 要素 |
|
-超分子 #1: YbtPQ
| 超分子 | 名称: YbtPQ / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#2 |
|---|---|
| 由来(天然) | 生物種:  |
-分子 #1: ABC transporter ATP-binding protein
| 分子 | 名称: ABC transporter ATP-binding protein / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO EC番号: 加水分解酵素; 酸無水物に作用; 酸無水物に作用・物質の膜輸送を触媒する |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 66.348664 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MSSQSSNTES LSRFPLWQVI TPVRRKVILA MALAGLAALT SLGALLFLAW SLRDIRATPD AIPAWPLGGV IGCVVLTFVL RLQAFNTSH YAAFHLENIL RSRLARKALQ LPPGVLQQMG SGSVAKVMLD DVKSLHIFVA DSTPLYARAI IMPLATIVIL F WLDWRLAI ...文字列: MSSQSSNTES LSRFPLWQVI TPVRRKVILA MALAGLAALT SLGALLFLAW SLRDIRATPD AIPAWPLGGV IGCVVLTFVL RLQAFNTSH YAAFHLENIL RSRLARKALQ LPPGVLQQMG SGSVAKVMLD DVKSLHIFVA DSTPLYARAI IMPLATIVIL F WLDWRLAI ATLGVLAFGS VVLVLARQRS ENMAQRYHKA REQVSAAVIE FVQAMPVVRT FDSGSTSFLR YQRALEEWVD VL KTWYRKA GFSARFSFSI LNPLPTLFVL IWSGYGLLHY GSFDFIAWVA VLLLGSGMAE AVMPMMMLNN LVAQTRLSIQ RIY QVLAMP ELSLPQSDQQ PQEASITFEQ VSFHYPQART GAALQEVSFH VPAGQIVALV GPSGAGKSTV ARLLLRYADP DKGH IRIGG VDLRDMQTDT LMKQLSFVFQ DNFLFADTIA NNIRLGAPDT PLEAVIAAAR VAQAHDFISA LPEGYNTRVG ERGVF LSGG QRQRITIARA LLQDRPILVL DEATAFADPE NEAALIKALA AAMRGRTVIM VAHRLSMVTQ ADVILLFSDG QLREMG NHT QLLAQGGLYQ RLWQHYQQAQ HWVPGGTQEE VVENERQ UniProtKB: ABC transporter ATP-binding protein |
-分子 #2: Permease and ATP-binding protein of yersiniabactin-iron ABC trans...
| 分子 | 名称: Permease and ATP-binding protein of yersiniabactin-iron ABC transporter YbtQ タイプ: protein_or_peptide / ID: 2 / コピー数: 1 / 光学異性体: LEVO EC番号: 加水分解酵素; 酸無水物に作用; 酸無水物に作用・物質の膜輸送を触媒する |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 66.526086 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MKDNNPADNL AWRVIWRQLI SSVGSQARML RRSMLALLLA AFMQGIAFAC LYPIIDALLR GDAPQLLNWA MAFSVAAIVT LVLRWYGLG FEYRGHLAQA THELRLRLGE QLRRVPLEKL QRGRAGEMNA LLLGSVDENL NYVIAIANIL LLTIVTPLTA S LATLWIDW ...文字列: MKDNNPADNL AWRVIWRQLI SSVGSQARML RRSMLALLLA AFMQGIAFAC LYPIIDALLR GDAPQLLNWA MAFSVAAIVT LVLRWYGLG FEYRGHLAQA THELRLRLGE QLRRVPLEKL QRGRAGEMNA LLLGSVDENL NYVIAIANIL LLTIVTPLTA S LATLWIDW RLGLVMLLIF PLLVPFYYWR RPAMRRQMQT LGEAHQRLSG DIVEFAQGMM VLRTCGSDAD KSRALLAHFN AL ENLQTRT HRQGAGATML IASVVELGLQ VVVLSGIVWV VTGTLNLAFL IAAVAMIMRF AEPMAMFISY TSVVELIASA LQR IEQFMA IAPLPVAEQS EMPERYDIRF DNVSYRYEEG DGYALNHVSL TFPAASMSAL VGASGAGKTT VTKLLMRYAD PQQG QISIG GVDIRRLTPE QLNSLISVVF QDVWLFDDTL LANIRIARPQ ATRQEVEEAA RAAQCLEFIS RLPQGWLTPM GEMGG QLSG GERQRISIAR ALLKNAPVVI LDEPTAALDI ESELAVQKAI DNLVHNRTVI IIAHRLSTIA GAGNILVMEE GQVVEQ GTH AQLLSHHGRY QALWQAQMAA RVWRDDGVSA SGEWVHE UniProtKB: Permease and ATP-binding protein of yersiniabactin-iron ABC transporter YbtQ |
-分子 #3: MAGNESIUM ION
| 分子 | 名称: MAGNESIUM ION / タイプ: ligand / ID: 3 / コピー数: 2 / 式: MG |
|---|---|
| 分子量 | 理論値: 24.305 Da |
-分子 #4: ADP ORTHOVANADATE
| 分子 | 名称: ADP ORTHOVANADATE / タイプ: ligand / ID: 4 / コピー数: 2 / 式: AOV |
|---|---|
| 分子量 | 理論値: 544.156 Da |
| Chemical component information | 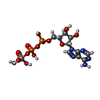 ChemComp-AOV: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 平均電子線量: 60.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 1.0 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期モデル | モデルのタイプ: NONE |
|---|---|
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 3.1 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 340080 |
| 初期 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
| 最終 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
 ムービー
ムービー コントローラー
コントローラー






 Z
Z Y
Y X
X