+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
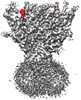
| タイトル | Aplysia californica FaNaC in ligand bound state | |||||||||
 マップデータ マップデータ | ligand bound full map | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | neuropeptide / ion channel / FMRFamide / TRANSPORT PROTEIN | |||||||||
| 機能・相同性 | Epithelial sodium channel / Amiloride-sensitive sodium channel / ligand-gated sodium channel activity / membrane / FMRFamide-gated Na+ channel 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.9 Å | |||||||||
 データ登録者 データ登録者 | Chen QF / Liu FL / Dang Y / Feng H / Zhang Z / Ye S | |||||||||
| 資金援助 |  中国, 2件 中国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nat Chem Biol / 年: 2023 ジャーナル: Nat Chem Biol / 年: 2023タイトル: Structure and mechanism of a neuropeptide-activated channel in the ENaC/DEG superfamily. 著者: Fenglian Liu / Yu Dang / Lu Li / Hao Feng / Jianlin Li / Haowei Wang / Xu Zhang / Zhe Zhang / Sheng Ye / Yutao Tian / Qingfeng Chen /  要旨: Phe-Met-Arg-Phe-amide (FMRFamide)-activated sodium channels (FaNaCs) are a family of channels activated by the neuropeptide FMRFamide, and, to date, the underlying ligand gating mechanism remains ...Phe-Met-Arg-Phe-amide (FMRFamide)-activated sodium channels (FaNaCs) are a family of channels activated by the neuropeptide FMRFamide, and, to date, the underlying ligand gating mechanism remains unknown. Here we present the high-resolution cryo-electron microscopy structures of Aplysia californica FaNaC in both apo and FMRFamide-bound states. AcFaNaC forms a chalice-shaped trimer and possesses several notable features, including two FaNaC-specific insertion regions, a distinct finger domain and non-domain-swapped transmembrane helix 2 in the transmembrane domain (TMD). One FMRFamide binds to each subunit in a cleft located in the top-most region of the extracellular domain, with participation of residues from the neighboring subunit. Bound FMRFamide adopts an extended conformation. FMRFamide binds tightly to A. californica FaNaC in an N terminus-in manner, which causes collapse of the binding cleft and induces large local conformational rearrangements. Such conformational changes are propagated downward toward the TMD via the palm domain, possibly resulting in outward movement of the TMD and dilation of the ion conduction pore. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_34122.map.gz emd_34122.map.gz | 59.9 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-34122-v30.xml emd-34122-v30.xml emd-34122.xml emd-34122.xml | 19 KB 19 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_34122.png emd_34122.png | 161.1 KB | ||
| Filedesc metadata |  emd-34122.cif.gz emd-34122.cif.gz | 6.2 KB | ||
| その他 |  emd_34122_half_map_1.map.gz emd_34122_half_map_1.map.gz emd_34122_half_map_2.map.gz emd_34122_half_map_2.map.gz | 49.7 MB 49.7 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-34122 http://ftp.pdbj.org/pub/emdb/structures/EMD-34122 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-34122 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-34122 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_34122_validation.pdf.gz emd_34122_validation.pdf.gz | 836.9 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_34122_full_validation.pdf.gz emd_34122_full_validation.pdf.gz | 836.5 KB | 表示 | |
| XML形式データ |  emd_34122_validation.xml.gz emd_34122_validation.xml.gz | 12.2 KB | 表示 | |
| CIF形式データ |  emd_34122_validation.cif.gz emd_34122_validation.cif.gz | 14.3 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34122 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34122 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34122 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34122 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7yvbMC  7yvcC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_34122.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_34122.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | ligand bound full map | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.07 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: ligand bound half map 1
| ファイル | emd_34122_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | ligand bound half map 1 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: ligand bound half map 2
| ファイル | emd_34122_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | ligand bound half map 2 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Trimeric FMRFamide activated sodium channel from Aplysia californ...
| 全体 | 名称: Trimeric FMRFamide activated sodium channel from Aplysia californica (AcFaNaC) |
|---|---|
| 要素 |
|
-超分子 #1: Trimeric FMRFamide activated sodium channel from Aplysia californ...
| 超分子 | 名称: Trimeric FMRFamide activated sodium channel from Aplysia californica (AcFaNaC) タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#2 |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 73 KDa |
-分子 #1: FMRFamide-gated Na+ channel
| 分子 | 名称: FMRFamide-gated Na+ channel / タイプ: protein_or_peptide / ID: 1 詳細: Residues 672-679 correspond to the EXPRESSION TAG, whereas resides 660-665 correspond to the thrombin cleavage site, and resides 654-659 and 666-671 correspond to flexible linkers. コピー数: 3 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 76.638312 KDa |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: MLGRGERIKP YHFRDSSADH MKYTSVSAKS GMVPEHRYTM VRSRHHGRHH HHHSYQEYNT QRSAISLIAE LGSESNAHGL AKIVTSRDT KRKVIWALMV IIGFTAATLQ LSLLVRKYLQ FQVVELSEIK DSMPVEYPSV TICNIEPISL RKIRKAYNKN E SQNLKDWL ...文字列: MLGRGERIKP YHFRDSSADH MKYTSVSAKS GMVPEHRYTM VRSRHHGRHH HHHSYQEYNT QRSAISLIAE LGSESNAHGL AKIVTSRDT KRKVIWALMV IIGFTAATLQ LSLLVRKYLQ FQVVELSEIK DSMPVEYPSV TICNIEPISL RKIRKAYNKN E SQNLKDWL NFTQTFHFKD MSFMNSIRAF YENLGSDAKK ISHDLRDLLI HCRFNREECT TENFTSSFDG NYFNCFTFNG GQ LRDQLQM HATGPENGLS LIISIEKDEP LPGTYGVYNF ENNILHSAGV RVVVHAPGSM PSPVDHGFDI PPGYSSSVGL KAL LHTRLS EPYGNCTEDS LEGIQTYRNT FFACLQLCKQ RRLIRECKCK SSALPDLSVE NITFCGVIPD WKDIRRNVTG EYKM NQTIP TISLACEARV QKQLNNDRSY ETECGCYQPC SETSYLKSVS LSYWPLEFYQ LSALERFFSQ KNPTDQQHFM KIAQD FLSR LAHPQQQALA RNNSHDKDIL TTSYSLSEKE MAKEASDLIR QNLLRLNIYL EDLSVVEYRQ LPAYGLADLF ADIGGT LGL WMGISVLTIM ELMELIIRLF ALIFNAEREV PKAPVHSSNN GGGGGGDGQH NFANGDVEHE RDTHFPDLGS SDFDFRR GG GIGAESPVNV EGGSSGGLVP RGSGGSSGGH HHHHHHH UniProtKB: FMRFamide-gated Na+ channel |
-分子 #2: Phe-Met-Arg-Phe-amide
| 分子 | 名称: Phe-Met-Arg-Phe-amide / タイプ: protein_or_peptide / ID: 2 / コピー数: 3 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種: synthetic construct (人工物) |
| 分子量 | 理論値: 599.767 Da |
| 配列 | 文字列: FMR(NFA) |
-分子 #4: 2-acetamido-2-deoxy-beta-D-glucopyranose
| 分子 | 名称: 2-acetamido-2-deoxy-beta-D-glucopyranose / タイプ: ligand / ID: 4 / コピー数: 6 / 式: NAG |
|---|---|
| 分子量 | 理論値: 221.208 Da |
| Chemical component information |  ChemComp-NAG: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 4.00 mg/mL |
|---|---|
| 緩衝液 | pH: 8 |
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | #0 - Image recording ID: 1 #0 - フィルム・検出器のモデル: GATAN K3 (6k x 4k) #0 - 平均電子線量: 60.0 e/Å2 / #1 - Image recording ID: 2 #1 - フィルム・検出器のモデル: GATAN K3 (6k x 4k) #1 - 平均電子線量: 60.0 e/Å2 / #2 - Image recording ID: 3 #2 - フィルム・検出器のモデル: GATAN K3 (6k x 4k) #2 - 平均電子線量: 60.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 1.0 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析 #1
画像解析 #1
+ 画像解析 #2
画像解析 #2
+ 画像解析 #3
画像解析 #3
+ 画像解析 #4
画像解析 #4
-原子モデル構築 1
| 精密化 | プロトコル: AB INITIO MODEL |
|---|---|
| 得られたモデル |  PDB-7yvb: |
 ムービー
ムービー コントローラー
コントローラー




 Z
Z Y
Y X
X