+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-3345 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Hexadecameric structure of an invertebrate gap junction channel | |||||||||
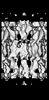
 マップデータ マップデータ | This is a map showing a single INX-6 gap junction channel with P2 crystallographic symmetry | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | innexin / gap junction channel / cryo-electron crystallography / three-dimensional reconstruction / two-dimensional crystal | |||||||||
| 生物種 |  | |||||||||
| 手法 | 電子線結晶学 / クライオ電子顕微鏡法 / 解像度: 10.0 Å | |||||||||
 データ登録者 データ登録者 | Oshima A / Matsuzawa T / Murata K / Tani K / Fujiyoshi Y | |||||||||
 引用 引用 |  ジャーナル: J Mol Biol / 年: 2016 ジャーナル: J Mol Biol / 年: 2016タイトル: Hexadecameric structure of an invertebrate gap junction channel. 著者: Atsunori Oshima / Tomohiro Matsuzawa / Kazuyoshi Murata / Kazutoshi Tani / Yoshinori Fujiyoshi /  要旨: Innexins are invertebrate-specific gap junction proteins with four transmembrane helices. These proteins oligomerize to constitute intercellular channels that allow for the passage of small signaling ...Innexins are invertebrate-specific gap junction proteins with four transmembrane helices. These proteins oligomerize to constitute intercellular channels that allow for the passage of small signaling molecules associated with neural and muscular electrical activity. In contrast to the large number of structural and functional studies of connexin gap junction channels, few structural studies of recombinant innexin channels are reported. Here we show the three-dimensional structure of two-dimensionally crystallized Caenorhabditis elegans innexin-6 (INX-6) gap junction channels. The N-terminal deleted INX-6 proteins are crystallized in lipid bilayers. The three-dimensional reconstruction determined by cryo-electron crystallography reveals that a single INX-6 gap junction channel comprises 16 subunits, a hexadecamer, in contrast to chordate connexin channels, which comprise 12 subunits. The channel pore diameters at the cytoplasmic entrance and extracellular gap region are larger than those of connexin26. Two bulb densities are observed in each hemichannel, one in the pore and the other at the cytoplasmic side of the hemichannel in the channel pore pathway. These findings imply a structural diversity of gap junction channels among multicellular organisms. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_3345.map.gz emd_3345.map.gz | 809 KB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-3345-v30.xml emd-3345-v30.xml emd-3345.xml emd-3345.xml | 10.8 KB 10.8 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  EMD-3345.tif EMD-3345.tif | 168.1 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-3345 http://ftp.pdbj.org/pub/emdb/structures/EMD-3345 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3345 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3345 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_3345_validation.pdf.gz emd_3345_validation.pdf.gz | 199.8 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_3345_full_validation.pdf.gz emd_3345_full_validation.pdf.gz | 198.9 KB | 表示 | |
| XML形式データ |  emd_3345_validation.xml.gz emd_3345_validation.xml.gz | 4.5 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3345 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3345 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3345 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3345 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_3345.map.gz / 形式: CCP4 / 大きさ: 2.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_3345.map.gz / 形式: CCP4 / 大きさ: 2.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | This is a map showing a single INX-6 gap junction channel with P2 crystallographic symmetry | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 これらの図は立方格子座標系で作成されたものです | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X: 2.4397 Å / Y: 2.5177 Å / Z: 2.5 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
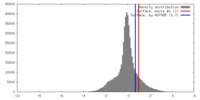
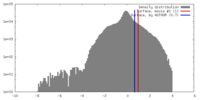
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : The N-terminal deleted C. elegans innexin-6
| 全体 | 名称: The N-terminal deleted C. elegans innexin-6 |
|---|---|
| 要素 |
|
-超分子 #1000: The N-terminal deleted C. elegans innexin-6
| 超分子 | 名称: The N-terminal deleted C. elegans innexin-6 / タイプ: sample / ID: 1000 / 詳細: The sample was reconstituted in lipid bilayers. / 集合状態: hexadecamer / Number unique components: 1 |
|---|---|
| 分子量 | 実験値: 700 KDa / 理論値: 700 KDa / 手法: MALDI-TOF |
-分子 #1: innexin-6
| 分子 | 名称: innexin-6 / タイプ: protein_or_peptide / ID: 1 / Name.synonym: INX-6 / コピー数: 16 / 集合状態: 16 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 実験値: 700 KDa / 理論値: 700 KDa |
| 組換発現 | 生物種:  組換細胞: Sf9 / 組換プラスミド: pFastbac |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 電子線結晶学 |
| 試料の集合状態 | 2D array |
- 試料調製
試料調製
| 濃度 | 0.5 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 / 詳細: 10 mM Tris (pH 7.5), 500 mM NaCl, and 1 mM EDTA |
| 凍結 | 凍結剤: ETHANE / チャンバー内温度: 120 K / 装置: FEI VITROBOT MARK IV / 手法: Blot for 30 seconds before plunging |
| 詳細 | Dialysis |
| 結晶化 | 詳細: Dialysis |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | JEOL KYOTO-3000SFF |
|---|---|
| 温度 | 最低: 4 K / 最高: 20 K / 平均: 4 K |
| 日付 | 2014年7月26日 |
| 撮影 | カテゴリ: FILM / フィルム・検出器のモデル: KODAK SO-163 FILM / デジタル化 - スキャナー: ZEISS SCAI / デジタル化 - サンプリング間隔: 7 µm / 実像数: 249 / 平均電子線量: 20 e/Å2 / カメラ長: 2000 / ビット/ピクセル: 8 |
| Tilt angle min | 0 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 38210 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 1.6 mm / 最大 デフォーカス(公称値): 3.459 µm / 最小 デフォーカス(公称値): 0.66 µm / 倍率(公称値): 40000 |
| 試料ステージ | 試料ホルダーモデル: JEOL / Tilt angle max: 45 / Tilt series - Axis1 - Min angle: 0 ° / Tilt series - Axis1 - Max angle: 45 ° |
- 画像解析
画像解析
| 詳細 | Images were processed with the MRC 2D crystal processing package. |
|---|---|
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 10.0 Å / 解像度の算出法: DIFFRACTION PATTERN/LAYERLINES / ソフトウェア - 名称: MRC |
| 結晶パラメータ | 単位格子 - A: 118.5 Å / 単位格子 - B: 111.5 Å / 単位格子 - C: 320 Å / 単位格子 - γ: 121.7 ° / 単位格子 - α: 90.0 ° / 単位格子 - β: 90.0 ° / 面群: P 2 |
| CTF補正 | 詳細: Each micrograph |
 ムービー
ムービー コントローラー
コントローラー





 Z (Sec.)
Z (Sec.) X (Row.)
X (Row.) Y (Col.)
Y (Col.)