+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure and mechanism of a mitochondrial AAA+ disaggregase CLPB | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / ネガティブ染色法 / 解像度: 6.8 Å | |||||||||
 データ登録者 データ登録者 | Wu D / Liu Y / Dai Y / Wang G / Lu G / Chen Y / Li N / Lin J / Gao N | |||||||||
| 資金援助 |  中国, 1件 中国, 1件
| |||||||||
 引用 引用 |  ジャーナル: PLoS Biol / 年: 2023 ジャーナル: PLoS Biol / 年: 2023タイトル: Comprehensive structural characterization of the human AAA+ disaggregase CLPB in the apo- and substrate-bound states reveals a unique mode of action driven by oligomerization. 著者: Damu Wu / Yan Liu / Yuhao Dai / Guopeng Wang / Guoliang Lu / Yan Chen / Ningning Li / Jinzhong Lin / Ning Gao /  要旨: The human AAA+ ATPase CLPB (SKD3) is a protein disaggregase in the mitochondrial intermembrane space (IMS) and functions to promote the solubilization of various mitochondrial proteins. Loss-of- ...The human AAA+ ATPase CLPB (SKD3) is a protein disaggregase in the mitochondrial intermembrane space (IMS) and functions to promote the solubilization of various mitochondrial proteins. Loss-of-function CLPB mutations are associated with a few human diseases with neutropenia and neurological disorders. Unlike canonical AAA+ proteins, CLPB contains a unique ankyrin repeat domain (ANK) at its N-terminus. How CLPB functions as a disaggregase and the role of its ANK domain are currently unclear. Herein, we report a comprehensive structural characterization of human CLPB in both the apo- and substrate-bound states. CLPB assembles into homo-tetradecamers in apo-state and is remodeled into homo-dodecamers upon substrate binding. Conserved pore-loops (PLs) on the ATPase domains form a spiral staircase to grip and translocate the substrate in a step-size of 2 amino acid residues. The ANK domain is not only responsible for maintaining the higher-order assembly but also essential for the disaggregase activity. Interactome analysis suggests that the ANK domain may directly interact with a variety of mitochondrial substrates. These results reveal unique properties of CLPB as a general disaggregase in mitochondria and highlight its potential as a target for the treatment of various mitochondria-related diseases. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_33105.map.gz emd_33105.map.gz | 9.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-33105-v30.xml emd-33105-v30.xml emd-33105.xml emd-33105.xml | 13.3 KB 13.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_33105.png emd_33105.png | 56 KB | ||
| その他 |  emd_33105_half_map_1.map.gz emd_33105_half_map_1.map.gz emd_33105_half_map_2.map.gz emd_33105_half_map_2.map.gz | 80.7 MB 80.7 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-33105 http://ftp.pdbj.org/pub/emdb/structures/EMD-33105 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-33105 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-33105 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_33105_validation.pdf.gz emd_33105_validation.pdf.gz | 658.1 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_33105_full_validation.pdf.gz emd_33105_full_validation.pdf.gz | 657.6 KB | 表示 | |
| XML形式データ |  emd_33105_validation.xml.gz emd_33105_validation.xml.gz | 13.2 KB | 表示 | |
| CIF形式データ |  emd_33105_validation.cif.gz emd_33105_validation.cif.gz | 15.6 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-33105 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-33105 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-33105 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-33105 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_33105.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_33105.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.07 Å | ||||||||||||||||||||||||||||||||||||
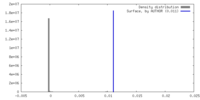
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #1
| ファイル | emd_33105_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
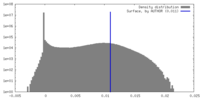
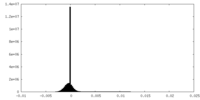
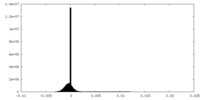
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_33105_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
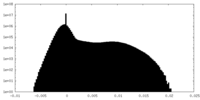
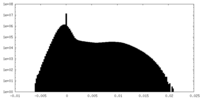
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : cryo-EM structure of CLPB in apo-state
| 全体 | 名称: cryo-EM structure of CLPB in apo-state |
|---|---|
| 要素 |
|
-超分子 #1: cryo-EM structure of CLPB in apo-state
| 超分子 | 名称: cryo-EM structure of CLPB in apo-state / タイプ: complex / ID: 1 / キメラ: Yes / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: CLPB
| 分子 | 名称: CLPB / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MLGSLVLRRK ALAPRLLLRL LRSPTLRGHG GASGRNVTTG SLGEPQWLRV ATGGRPGTSP ALFSGRGAA TGGRQGGRFD TKCLAAATWG RLPGPEETLP GQDSWNGVPS RAGLGMCALA A ALVVHCYS KSPSNKDAAL LEAARANNMQ EVSRLLSEGA DVNAKHRLGW ...文字列: MLGSLVLRRK ALAPRLLLRL LRSPTLRGHG GASGRNVTTG SLGEPQWLRV ATGGRPGTSP ALFSGRGAA TGGRQGGRFD TKCLAAATWG RLPGPEETLP GQDSWNGVPS RAGLGMCALA A ALVVHCYS KSPSNKDAAL LEAARANNMQ EVSRLLSEGA DVNAKHRLGW TALMVAAINR NN SVVQVLL AAGADPNLGD DFSSVYKTAK EQGIHSLEVL ITREDDFNNR LNNRASFKGC TAL HYAVLA DDYRTVKELL DGGANPLQRN EMGHTPLDYA REGEVMKLLR TSEAKYQEKQ RKRE AEERR RFPLEQRLKE HIIGQESAIA TVGAAIRRKE NGWYDEEHPL VFLFLGSSGI GKTEL AKQT AKYMHKDAKK GFIRLDMSEF QERHEVAKFI GSPPGYVGHE EGGQLTKKLK QCPNAV VLF DEVDKAHPDV LTIMLQLFDE GRLTDGKGKT IDCKDAIFIM TSNVASDEIA QHALQLR QE ALEMSRNRIA ENLGDVQISD KITISKNFKE NVIRPILKAH FRRDEFLGRI NEIVYFLP F CHSELIQLVN KELNFWAKRA KQRHNITLLW DREVADVLVD GYNVHYGARS IKHEVERRV VNQLAAAYEQ DLLPGGCTLR ITVEDSDKQL LKSPELPSPQ AEKRLPKLRL EIIDKDSKTR RLDIRAPLH PEKVCNTI |
-実験情報
-構造解析
| 手法 | ネガティブ染色法, クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | cell |
- 試料調製
試料調製
| 緩衝液 | pH: 6.8 |
|---|---|
| 染色 | タイプ: NEGATIVE / 材質: Uranyl Acetate |
| 凍結 | 凍結剤: NITROGEN |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 60.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: SPOT SCAN / 撮影モード: DARK FIELD / 最大 デフォーカス(公称値): 5.0 µm / 最小 デフォーカス(公称値): 1.2 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 6.8 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 153005 |
|---|---|
| 初期 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
| 最終 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
 ムービー
ムービー コントローラー
コントローラー










 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)