+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-3280 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Biochemical and structural characterization of the yeast Sdo1p suggests a surveillance role in the 60S ribosomal subunit maturation | |||||||||
 マップデータ マップデータ | Reconstruction of 60S-Sdo1p complex. | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Ribosome biogenesis / SBDS / SDS / Sdo1 / cryo-electron microscopy (cryo-EM) | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 14.0 Å | |||||||||
 データ登録者 データ登録者 | Ma CY / Yan KG / Tan D / Li NN / Zhang YX / Yuan Y / Li ZF / Dong MQ / Lei JL / Gao N | |||||||||
 引用 引用 |  ジャーナル: Protein Cell / 年: 2016 ジャーナル: Protein Cell / 年: 2016タイトル: Structural dynamics of the yeast Shwachman-Diamond syndrome protein (Sdo1) on the ribosome and its implication in the 60S subunit maturation. 著者: Chengying Ma / Kaige Yan / Dan Tan / Ningning Li / Yixiao Zhang / Yi Yuan / Zhifei Li / Meng-Qiu Dong / Jianlin Lei / Ning Gao /  要旨: The human Shwachman-Diamond syndrome (SDS) is an autosomal recessive disease caused by mutations in a highly conserved ribosome assembly factor SBDS. The functional role of SBDS is to cooperate with ...The human Shwachman-Diamond syndrome (SDS) is an autosomal recessive disease caused by mutations in a highly conserved ribosome assembly factor SBDS. The functional role of SBDS is to cooperate with another assembly factor, elongation factor 1-like (Efl1), to promote the release of eukaryotic initiation factor 6 (eIF6) from the late-stage cytoplasmic 60S precursors. In the present work, we characterized, both biochemically and structurally, the interaction between the 60S subunit and SBDS protein (Sdo1p) from yeast. Our data show that Sdo1p interacts tightly with the mature 60S subunit in vitro through its domain I and II, and is capable of bridging two 60S subunits to form a stable 2:2 dimer. Structural analysis indicates that Sdo1p bind to the ribosomal P-site, in the proximity of uL16 and uL5, and with direct contact to H69 and H38. The dynamic nature of Sdo1p on the 60S subunit, together with its strategic binding position, suggests a surveillance role of Sdo1p in monitoring the conformational maturation of the ribosomal P-site. Altogether, our data support a conformational signal-relay cascade during late-stage 60S maturation, involving uL16, Sdo1p, and Efl1p, which interrogates the functional P-site to control the departure of the anti-association factor eIF6. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_3280.map.gz emd_3280.map.gz | 16.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-3280-v30.xml emd-3280-v30.xml emd-3280.xml emd-3280.xml | 8.7 KB 8.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_3280_fsc.xml emd_3280_fsc.xml | 6.3 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  EMD-3280_60S-Sdo1p.jpg EMD-3280_60S-Sdo1p.jpg emd_3280.png emd_3280.png | 115.8 KB 104.6 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-3280 http://ftp.pdbj.org/pub/emdb/structures/EMD-3280 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3280 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3280 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_3280_validation.pdf.gz emd_3280_validation.pdf.gz | 257.5 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_3280_full_validation.pdf.gz emd_3280_full_validation.pdf.gz | 256.6 KB | 表示 | |
| XML形式データ |  emd_3280_validation.xml.gz emd_3280_validation.xml.gz | 9.3 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3280 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3280 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3280 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3280 | HTTPS FTP |
-関連構造データ
| 類似構造データ |
|---|
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_3280.map.gz / 形式: CCP4 / 大きさ: 21.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_3280.map.gz / 形式: CCP4 / 大きさ: 21.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Reconstruction of 60S-Sdo1p complex. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 2.76 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
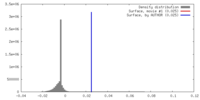
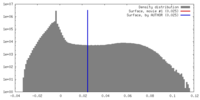
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : The dimeric structure of the yeast 60S ribosomal subunits bound w...
| 全体 | 名称: The dimeric structure of the yeast 60S ribosomal subunits bound with Sdo1p |
|---|---|
| 要素 |
|
-超分子 #1000: The dimeric structure of the yeast 60S ribosomal subunits bound w...
| 超分子 | 名称: The dimeric structure of the yeast 60S ribosomal subunits bound with Sdo1p タイプ: sample / ID: 1000 / 集合状態: two Sdo1p binding to two 60S subunit / Number unique components: 2 |
|---|
-超分子 #1: Sdo1p bound 60S subunit
| 超分子 | 名称: Sdo1p bound 60S subunit / タイプ: complex / ID: 1 / 組換発現: No / Ribosome-details: ribosome-eukaryote: LSU 60S |
|---|---|
| 由来(天然) | 生物種:  |
-分子 #1: Sdo1p
| 分子 | 名称: Sdo1p / タイプ: protein_or_peptide / ID: 1 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 凍結 | 凍結剤: ETHANE / 装置: FEI VITROBOT MARK IV |
|---|
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI F20 |
|---|---|
| 日付 | 2011年12月8日 |
| 撮影 | カテゴリ: CCD / フィルム・検出器のモデル: FEI EAGLE (4k x 4k) |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.0 mm |
| 試料ステージ | 試料ホルダー: Gatan CT3500 / 試料ホルダーモデル: OTHER |
| 実験機器 |  モデル: Tecnai F20 / 画像提供: FEI Company |
- 画像解析
画像解析
| CTF補正 | 詳細: ctfindIII |
|---|---|
| 最終 再構成 | 想定した対称性 - 点群: C2 (2回回転対称) / 解像度のタイプ: BY AUTHOR / 解像度: 14.0 Å / 解像度の算出法: OTHER / ソフトウェア - 名称: Spider, relion / 使用した粒子像数: 13219 |
| FSC曲線 (解像度の算出) |  |
-原子モデル構築 1
| 初期モデル | PDB ID:  3o58 |
|---|---|
| ソフトウェア | 名称:  Chimera Chimera |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT |
 ムービー
ムービー コントローラー
コントローラー







 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)