+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | III2IV2 respiratory supercomplex from Saccharomyces cerevisiae with 4 bound UQ6 | |||||||||
 マップデータ マップデータ | Final Density Map | |||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報: / Complex III assembly / matrix side of mitochondrial inner membrane / protein processing involved in protein targeting to mitochondrion / mitochondrial cytochrome c oxidase assembly / Respiratory electron transport / mitochondrial respirasome assembly / mitochondrial respiratory chain complex III assembly / Mitochondrial protein degradation / : ...: / Complex III assembly / matrix side of mitochondrial inner membrane / protein processing involved in protein targeting to mitochondrion / mitochondrial cytochrome c oxidase assembly / Respiratory electron transport / mitochondrial respirasome assembly / mitochondrial respiratory chain complex III assembly / Mitochondrial protein degradation / : / : / cytochrome-c oxidase / : / quinol-cytochrome-c reductase / ubiquinol-cytochrome-c reductase activity / mitochondrial electron transport, cytochrome c to oxygen / cellular respiration / cytochrome-c oxidase activity / mitochondrial electron transport, ubiquinol to cytochrome c / mitochondrial crista / electron transport coupled proton transport / enzyme regulator activity / ATP synthesis coupled electron transport / aerobic respiration / proton transmembrane transport / nuclear periphery / mitochondrial membrane / mitochondrial intermembrane space / metalloendopeptidase activity / 2 iron, 2 sulfur cluster binding / mitochondrial inner membrane / oxidoreductase activity / copper ion binding / heme binding / mitochondrion / proteolysis / zinc ion binding / membrane / metal ion binding / cytosol 類似検索 - 分子機能 | |||||||||
| 生物種 |   | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.2 Å | |||||||||
 データ登録者 データ登録者 | Hryc CF / Mileykovskaya E / Baker M / Dowhan W | |||||||||
| 資金援助 |  米国, 2件 米国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2023 ジャーナル: Nat Commun / 年: 2023タイトル: Structural insights into cardiolipin replacement by phosphatidylglycerol in a cardiolipin-lacking yeast respiratory supercomplex. 著者: Corey F Hryc / Venkata K P S Mallampalli / Evgeniy I Bovshik / Stavros Azinas / Guizhen Fan / Irina I Serysheva / Genevieve C Sparagna / Matthew L Baker / Eugenia Mileykovskaya / William Dowhan /  要旨: Cardiolipin is a hallmark phospholipid of mitochondrial membranes. Despite established significance of cardiolipin in supporting respiratory supercomplex organization, a mechanistic understanding of ...Cardiolipin is a hallmark phospholipid of mitochondrial membranes. Despite established significance of cardiolipin in supporting respiratory supercomplex organization, a mechanistic understanding of this lipid-protein interaction is still lacking. To address the essential role of cardiolipin in supercomplex organization, we report cryo-EM structures of a wild type supercomplex (IVIIIIV) and a supercomplex (IIIIV) isolated from a cardiolipin-lacking Saccharomyces cerevisiae mutant at 3.2-Å and 3.3-Å resolution, respectively, and demonstrate that phosphatidylglycerol in IIIIV occupies similar positions as cardiolipin in IVIIIIV. Lipid-protein interactions within these complexes differ, which conceivably underlies the reduced level of IVIIIIV and high levels of IIIIV and free III and IV in mutant mitochondria. Here we show that anionic phospholipids interact with positive amino acids and appear to nucleate a phospholipid domain at the interface between the individual complexes, which dampen charge repulsion and further stabilize interaction, respectively, between individual complexes. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_27940.map.gz emd_27940.map.gz | 136.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-27940-v30.xml emd-27940-v30.xml emd-27940.xml emd-27940.xml | 39.4 KB 39.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_27940_fsc.xml emd_27940_fsc.xml | 16.4 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_27940.png emd_27940.png | 168.1 KB | ||
| その他 |  emd_27940_half_map_1.map.gz emd_27940_half_map_1.map.gz emd_27940_half_map_2.map.gz emd_27940_half_map_2.map.gz | 134.1 MB 134.1 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-27940 http://ftp.pdbj.org/pub/emdb/structures/EMD-27940 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-27940 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-27940 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_27940_validation.pdf.gz emd_27940_validation.pdf.gz | 876.1 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_27940_full_validation.pdf.gz emd_27940_full_validation.pdf.gz | 875.6 KB | 表示 | |
| XML形式データ |  emd_27940_validation.xml.gz emd_27940_validation.xml.gz | 20.3 KB | 表示 | |
| CIF形式データ |  emd_27940_validation.cif.gz emd_27940_validation.cif.gz | 26.6 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27940 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27940 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27940 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27940 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8e7sMC  8ec0C M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_27940.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_27940.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Final Density Map | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.07 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: Half map B
| ファイル | emd_27940_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map B | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
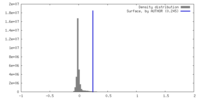
| 密度ヒストグラム |
-ハーフマップ: Half map A
| ファイル | emd_27940_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map A | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
+全体 : III2-IV2 mitochondrial respiratory supercomplex
+超分子 #1: III2-IV2 mitochondrial respiratory supercomplex
+分子 #1: Cytochrome b-c1 complex subunit 1, mitochondrial
+分子 #2: Cytochrome b-c1 complex subunit 2, mitochondrial
+分子 #3: Cytochrome b-c1 complex subunit Rieske, mitochondrial
+分子 #4: Cytochrome b-c1 complex subunit 10, mitochondrial
+分子 #5: Cytochrome b-c1 complex subunit 9, mitochondrial
+分子 #6: Cytochrome b-c1 complex subunit 7, mitochondrial
+分子 #7: Cytochrome b-c1 complex subunit 6, mitochondrial
+分子 #8: Cytochrome b-c1 complex subunit 8, mitochondrial
+分子 #9: Cytochrome b
+分子 #10: Cytochrome c oxidase subunit 1
+分子 #11: Cytochrome c1, heme protein, mitochondrial
+分子 #12: Cytochrome c oxidase subunit 8, mitochondrial
+分子 #13: Cytochrome c oxidase subunit 7, mitochondrial
+分子 #14: Cytochrome c oxidase subunit 3
+分子 #15: Cytochrome c oxidase subunit 2
+分子 #16: Cytochrome c oxidase subunit 6, mitochondrial
+分子 #17: Cytochrome c oxidase subunit 9, mitochondrial
+分子 #18: Cytochrome c oxidase subunit 13, mitochondrial
+分子 #19: Cytochrome c oxidase subunit 4, mitochondrial
+分子 #20: Cytochrome c oxidase subunit 12, mitochondrial
+分子 #21: Cytochrome c oxidase subunit 26, mitochondrial
+分子 #22: Cytochrome c oxidase subunit 5A, mitochondrial
+分子 #23: DI-PALMITOYL-3-SN-PHOSPHATIDYLETHANOLAMINE
+分子 #24: FE2/S2 (INORGANIC) CLUSTER
+分子 #25: CARDIOLIPIN
+分子 #26: 1,2-DIACYL-SN-GLYCERO-3-PHOSHOCHOLINE
+分子 #27: (5S,11R)-5,8,11-trihydroxy-5,11-dioxido-17-oxo-4,6,10,12,16-penta...
+分子 #28: PROTOPORPHYRIN IX CONTAINING FE
+分子 #29: 5-(3,7,11,15,19,23-HEXAMETHYL-TETRACOSA-2,6,10,14,18,22-HEXAENYL)...
+分子 #30: HEME-A
+分子 #31: COPPER (II) ION
+分子 #32: DINUCLEAR COPPER ION
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.2 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / デジタル化 - サイズ - 横: 360 pixel / デジタル化 - サイズ - 縦: 360 pixel / デジタル化 - 画像ごとのフレーム数: 1-35 / 実像数: 20253 / 平均電子線量: 49.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 3.5 µm / 最小 デフォーカス(公称値): 1.5 µm / 倍率(公称値): 130000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー












 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)