+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of monomeric LRRK1 | |||||||||||||||
 マップデータ マップデータ | Sharpened map for LRRK1 monomer | |||||||||||||||
 試料 試料 |
| |||||||||||||||
 キーワード キーワード | monomer / TRANSFERASE | |||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報negative regulation of peptidyl-tyrosine phosphorylation / osteoclast development / positive regulation of intracellular signal transduction / bone resorption / positive regulation of peptidyl-tyrosine phosphorylation / positive regulation of canonical Wnt signaling pathway / phosphorylation / non-specific serine/threonine protein kinase / intracellular signal transduction / protein serine kinase activity ...negative regulation of peptidyl-tyrosine phosphorylation / osteoclast development / positive regulation of intracellular signal transduction / bone resorption / positive regulation of peptidyl-tyrosine phosphorylation / positive regulation of canonical Wnt signaling pathway / phosphorylation / non-specific serine/threonine protein kinase / intracellular signal transduction / protein serine kinase activity / protein serine/threonine kinase activity / GTP binding / mitochondrion / ATP binding / identical protein binding / membrane / metal ion binding / cytosol 類似検索 - 分子機能 | |||||||||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||||||||
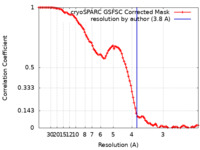
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.8 Å | |||||||||||||||
 データ登録者 データ登録者 | Reimer JM / Mathea S / Chatterjee D / Knapp S / Leschziner AE | |||||||||||||||
| 資金援助 |  米国, 4件 米国, 4件
| |||||||||||||||
 引用 引用 |  ジャーナル: Nat Struct Mol Biol / 年: 2023 ジャーナル: Nat Struct Mol Biol / 年: 2023タイトル: Structure of LRRK1 and mechanisms of autoinhibition and activation. 著者: Janice M Reimer / Andrea M Dickey / Yu Xuan Lin / Robert G Abrisch / Sebastian Mathea / Deep Chatterjee / Elizabeth J Fay / Stefan Knapp / Matthew D Daugherty / Samara L Reck-Peterson / Andres E Leschziner /   要旨: Leucine Rich Repeat Kinase 1 and 2 (LRRK1 and LRRK2) are homologs in the ROCO family of proteins in humans. Despite their shared domain architecture and involvement in intracellular trafficking, ...Leucine Rich Repeat Kinase 1 and 2 (LRRK1 and LRRK2) are homologs in the ROCO family of proteins in humans. Despite their shared domain architecture and involvement in intracellular trafficking, their disease associations are strikingly different: LRRK2 is involved in familial Parkinson's disease while LRRK1 is linked to bone diseases. Furthermore, Parkinson's disease-linked mutations in LRRK2 are typically autosomal dominant gain-of-function while those in LRRK1 are autosomal recessive loss-of-function. Here, to understand these differences, we solved cryo-EM structures of LRRK1 in its monomeric and dimeric forms. Both differ from the corresponding LRRK2 structures. Unlike LRRK2, which is sterically autoinhibited as a monomer, LRRK1 is sterically autoinhibited in a dimer-dependent manner. LRRK1 has an additional level of autoinhibition that prevents activation of the kinase and is absent in LRRK2. Finally, we place the structural signatures of LRRK1 and LRRK2 in the context of the evolution of the LRRK family of proteins. | |||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_27813.map.gz emd_27813.map.gz | 86.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-27813-v30.xml emd-27813-v30.xml emd-27813.xml emd-27813.xml | 17.8 KB 17.8 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_27813_fsc.xml emd_27813_fsc.xml | 10.8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_27813.png emd_27813.png | 68.6 KB | ||
| Filedesc metadata |  emd-27813.cif.gz emd-27813.cif.gz | 6.8 KB | ||
| その他 |  emd_27813_half_map_1.map.gz emd_27813_half_map_1.map.gz emd_27813_half_map_2.map.gz emd_27813_half_map_2.map.gz | 84.6 MB 84.6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-27813 http://ftp.pdbj.org/pub/emdb/structures/EMD-27813 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-27813 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-27813 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_27813_validation.pdf.gz emd_27813_validation.pdf.gz | 922.3 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_27813_full_validation.pdf.gz emd_27813_full_validation.pdf.gz | 921.8 KB | 表示 | |
| XML形式データ |  emd_27813_validation.xml.gz emd_27813_validation.xml.gz | 17.4 KB | 表示 | |
| CIF形式データ |  emd_27813_validation.cif.gz emd_27813_validation.cif.gz | 21.9 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27813 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27813 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27813 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27813 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8e04MC  8e05C  8e06C C: 同じ文献を引用 ( M: このマップから作成された原子モデル |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_27813.map.gz / 形式: CCP4 / 大きさ: 91.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_27813.map.gz / 形式: CCP4 / 大きさ: 91.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Sharpened map for LRRK1 monomer | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.16 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: Half map A for LRRK1 monomer
| ファイル | emd_27813_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map A for LRRK1 monomer | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Half map B for LRRK1 monomer
| ファイル | emd_27813_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map B for LRRK1 monomer | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : LRRK1 20-2015
| 全体 | 名称: LRRK1 20-2015 |
|---|---|
| 要素 |
|
-超分子 #1: LRRK1 20-2015
| 超分子 | 名称: LRRK1 20-2015 / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: Leucine-rich repeat serine/threonine-protein kinase 1
| 分子 | 名称: Leucine-rich repeat serine/threonine-protein kinase 1 タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO / EC番号: non-specific serine/threonine protein kinase |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 223.512703 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: SAVCPERAME TLNGAGDTGG KPSTRGGDPA ARSRRTEGIR AAYRRGDRGG ARDLLEEACD QCASQLEKGQ LLSIPAAYGD LEMVRYLLS KRLVELPTEP TDDNPAVVAA YFGHTAVVQE LLESLPGPCS PQRLLNWMLA LACQRGHLGV VKLLVLTHGA D PESYAVRK ...文字列: SAVCPERAME TLNGAGDTGG KPSTRGGDPA ARSRRTEGIR AAYRRGDRGG ARDLLEEACD QCASQLEKGQ LLSIPAAYGD LEMVRYLLS KRLVELPTEP TDDNPAVVAA YFGHTAVVQE LLESLPGPCS PQRLLNWMLA LACQRGHLGV VKLLVLTHGA D PESYAVRK NEFPVIVRLP LYAAIKSGNE DIAIFLLRHG AYFCSYILLD SPDPSKHLLR KYFIEASPLP SSYPGKTALR VK WSHLRLP WVDLDWLIDI SCQITELDLS ANCLATLPSV IPWGLINLRK LNLSDNHLGE LPGVQSSDEI ICSRLLEIDI SSN KLSHLP PGFLHLSKLQ KLTASKNCLE KLFEEENATN WIGLRKLQEL DISDNKLTEL PALFLHSFKS LNSLNVSRNN LKVF PDPWA CPLKCCKASR NALECLPDKM AVFWKNHLKD VDFSENALKE VPLGLFQLDA LMFLRLQGNQ LAALPPQEKW TCRQL KTLD LSRNQLGKNE DGLKTKRIAF FTTRGRQRSG TEAASVLEFP AFLSESLEVL CLNDNHLDTV PPSVCLLKSL SELYLG NNP GLRELPPELG QLGNLWQLDT EDLTISNVPA EIQKEGPKAM LSYLRAQLRK AEKCKLMKMI IVGPPRQGKS TLLEILQ TG RAPQVVHGEA TIRTTKWELQ RPAGSRAKVE SVEFNVWDIG GPASMATVNQ CFFTDKALYV VVWNLALGEE AVANLQFW L LNIEAKAPNA VVLVVGTHLD LIEAKFRVER IATLRAYVLA LCRSPSGSRA TGFPDITFKH LHEISCKSLE GQEGLRQLI FHVTCSMKDV GSTIGCQRLA GRLIPRSYLS LQEAVLAEQQ RRSRDDDVQY LTDRQLEQLV EQTPDNDIKD YEDLQSAISF LIETGTLLH FPDTSHGLRN LYFLDPIWLS ECLQRIFNIK GSRSVAKNGV IRAEDLRMLL VGTGFTQQTE EQYFQFLAKF E IALPVAND SYLLPHLLPS KPGLDTHGMR HPTANTIQRV FKMSFVPVGF WQRFIARMLI SLAEMDLQLF ENKKNTKSRN RK VTIYSFT GNQRNRCSTF RVKRNQTIYW QEGLLVTFDG GYLSVESSDV NWKKKKSGGM KIVCQSEVRD FSAMAFITDH VNS LIDQWF PALTATESDG TPLMEQYVPC PVCETAWAQH TDPSEKSEDV QYFDMEDCVL TAIERDFISC PRHPDLPVPL QELV PELFM TDFPARLFLE NSKLEHSEDE GSVLGQGGSG TVIYRARYQG QPVAVKRFHI KKFKNFANVP ADTMLRHLRA TDAMK NFSE FRQEASMLHA LQHPCIVALI GISIHPLCFA LELAPLSSLN TVLSENARDS SFIPLGHMLT QKIAYQIASG LAYLHK KNI IFCDLKSDNI LVWSLDVKEH INIKLSDYGI SRQSFHEGAL GVEGTPGYQA PEIRPRIVYD EKVDMFSYGM VLYELLS GQ RPALGHHQLQ IAKKLSKGIR PVLGQPEEVQ FRRLQALMME CWDTKPEKRP LALSVVSQMK DPTFATFMYE LCCGKQTA F FSSQGQEYTV VFWDGKEESR NYTVVNTEKG LMEVQRMCCP GMKVSCQLQV QRSLWTATED QKIYIYTLKG MCPLNTPQQ ALDTPAVVTC FLAVPVIKKN SYLVLAGLAD GLVAVFPVVR GTPKDSCSYL CSHTANRSKF SIADEDARQN PYPVKAMEVV NSGSEVWYS NGPGLLVIDC ASLEICRRLE PYMAPSMVTS VVCSSEGRGE EVVWCLDDKA NSLVMYHSTT YQLCARYFCG V PSPLRDMF PVRPLDTEPP AASHTANPKV PEGDSIADVS IMYSEELGTQ ILIHQESLTD YCSMSSYSSS PPRQAARSPS SL PSSPASS SSVPFSTDCE DSDMLHTPGA ASDRSEHDLT PMDGETFSQH LQAVKILAVR DLIWVPRRGG DVIVIGLEKD SGA QRGRVI AVLKARELTP HGVLVDAAVV AKDTVVCTFE NENTEWCLAV WRGWGAREFD IFYQSYEELG RLEACTRKRR UniProtKB: Leucine-rich repeat serine/threonine-protein kinase 1 |
-分子 #2: GUANOSINE-5'-DIPHOSPHATE
| 分子 | 名称: GUANOSINE-5'-DIPHOSPHATE / タイプ: ligand / ID: 2 / コピー数: 1 / 式: GDP |
|---|---|
| 分子量 | 理論値: 443.201 Da |
| Chemical component information |  ChemComp-GDP: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 詳細: 50 mM HEPES pH 7.4, 150 mM NaCl, 5% glycerol, 0.5 mM TCEP, 20 uM GDP |
|---|---|
| グリッド | モデル: UltrAuFoil R1.2/1.3 / 材質: GOLD / 前処理 - タイプ: PLASMA CLEANING |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TALOS ARCTICA |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 51.0 e/Å2 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.124 µm 最小 デフォーカス(公称値): 1.2630000000000001 µm |
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー














 Z
Z Y
Y X
X