+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of TRPV5 in detergent in the presence of PKA | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Calcium / Ion channel / Kidney / MEMBRANE PROTEIN | |||||||||
| 生物種 |   | |||||||||
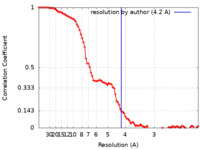
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.2 Å | |||||||||
 データ登録者 データ登録者 | Fluck EC / Yazici AT / Rohacs T / Moiseenkova-Bell VY | |||||||||
| 資金援助 |  米国, 2件 米国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Cell Rep / 年: 2022 ジャーナル: Cell Rep / 年: 2022タイトル: Structural basis of TRPV5 regulation by physiological and pathophysiological modulators. 著者: Edwin C Fluck / Aysenur Torun Yazici / Tibor Rohacs / Vera Y Moiseenkova-Bell /  要旨: Transient receptor potential vanilloid 5 (TRPV5) is a kidney-specific Ca-selective ion channel that plays a key role in Ca homeostasis. The basal activity of TRPV5 is balanced through activation by ...Transient receptor potential vanilloid 5 (TRPV5) is a kidney-specific Ca-selective ion channel that plays a key role in Ca homeostasis. The basal activity of TRPV5 is balanced through activation by phosphatidylinositol 4,5-bisphosphate (PI(4,5)P) and inhibition by Ca-bound calmodulin (CaM). Parathyroid hormone (PTH), the key extrinsic regulator of Ca homeostasis, increases the activity of TRPV5 via protein kinase A (PKA)-mediated phosphorylation. Metabolic acidosis leads to reduced TRPV5 activity independent of PTH, causing hypercalciuria. Using cryoelectron microscopy (cryo-EM), we show that low pH inhibits TRPV5 by precluding PI(4,5)P activation. We capture intermediate conformations at low pH, revealing a transition from open to closed state. In addition, we demonstrate that PI(4,5)P is the primary modulator of channel gating, yet PKA controls TRPV5 activity by preventing CaM binding and channel inactivation. Our data provide detailed molecular mechanisms for regulation of TRPV5 by two key extrinsic modulators, low pH and PKA. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_25722.map.gz emd_25722.map.gz | 59.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-25722-v30.xml emd-25722-v30.xml emd-25722.xml emd-25722.xml | 15.2 KB 15.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_25722_fsc.xml emd_25722_fsc.xml | 8.8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_25722.png emd_25722.png | 70.1 KB | ||
| Filedesc metadata |  emd-25722.cif.gz emd-25722.cif.gz | 5.6 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-25722 http://ftp.pdbj.org/pub/emdb/structures/EMD-25722 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-25722 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-25722 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_25722_validation.pdf.gz emd_25722_validation.pdf.gz | 566.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_25722_full_validation.pdf.gz emd_25722_full_validation.pdf.gz | 565.8 KB | 表示 | |
| XML形式データ |  emd_25722_validation.xml.gz emd_25722_validation.xml.gz | 11.1 KB | 表示 | |
| CIF形式データ |  emd_25722_validation.cif.gz emd_25722_validation.cif.gz | 14.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-25722 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-25722 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-25722 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-25722 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_25722.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_25722.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 1.07 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Tetrameric assembly of TRPV5 ion channel reconstituted in deterge...
| 全体 | 名称: Tetrameric assembly of TRPV5 ion channel reconstituted in detergent with catalytic subunit of PKA |
|---|---|
| 要素 |
|
-超分子 #1: Tetrameric assembly of TRPV5 ion channel reconstituted in deterge...
| 超分子 | 名称: Tetrameric assembly of TRPV5 ion channel reconstituted in detergent with catalytic subunit of PKA タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  |
-分子 #1: Transient receptor potential cation channel subfamily V member 5
| 分子 | 名称: Transient receptor potential cation channel subfamily V member 5 タイプ: protein_or_peptide / ID: 1 / 詳細: Rabbit TRPV5 with c-terminal 1D4 epitope tag / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MGACPPKAKG PWAQLQKLLI SWPVGEQDWE QYRDRVNMLQ QERIRDSPLL QAAKENDLRL LKILLLNQSC DFQQRGAVGE TALHVAALY DNLEAATLLM EAAPELAKEP ALCEPFVGQT ALHIAVMNQN LNLVRALLAR GASVSARATG AAFRRSPHNL I YYGEHPLS ...文字列: MGACPPKAKG PWAQLQKLLI SWPVGEQDWE QYRDRVNMLQ QERIRDSPLL QAAKENDLRL LKILLLNQSC DFQQRGAVGE TALHVAALY DNLEAATLLM EAAPELAKEP ALCEPFVGQT ALHIAVMNQN LNLVRALLAR GASVSARATG AAFRRSPHNL I YYGEHPLS FAACVGSEEI VRLLIEHGAD IRAQDSLGNT VLHILILQPN KTFACQMYNL LLSYDEHSDH LQSLELVPNH QG LTPFKLA GVEGNTVMFQ HLMQKRKHVQ WTCGPLTSTL YDLTEIDSWG EELSFLELVV SSKKREARQI LEQTPVKELV SFK WKKYGR PYFCVLASLY ILYMICFTTC CIYRPLKLRD DNRTDPRDIT ILQQKLLQEA YVTHQDNIRL VGELVTVTGA VIIL LLEIP DIFRVGASRY FGQTILGGPF HVIIITYASL VLLTMVMRLT NMNGEVVPLS FALVLGWCSV MYFARGFQML GPFTI MIQK MIFGDLMRFC WLMAVVILGF ASAFHITFQT EDPNNLGEFS DYPTALFSTF ELFLTIIDGP ANYSVDLPFM YCITYA AFA IIATLLMLNL FIAMMGDTHW RVAQERDELW RAQVVATTVM LERKMPRFLW PRSGICGYEY GLGDRWFLRV ENHHDQN PL RVLRYVEAFK CSDKEDGQEQ LSEKRPSTVE SGMLSRASVA FQTPSLSRTT SQSSNSHRGW EILRRNTLGH LNLGLDLG E GDGEEVYHFT ETSQVAPA |
-分子 #2: Protein kinase A catalytic subunit
| 分子 | 名称: Protein kinase A catalytic subunit / タイプ: protein_or_peptide / ID: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MGSSHHHHHH SSGLVPRGSH MGNAAAAKKG SEQESVKEFL AKAKEDFLKK WETPSQNTAQ LDQFDRIKTL GTGSFGRVML VKHKESGNHY AMKILDKQKV VKLKQIEHTL NEKRILQAVN FPFLVKLEFS FKDNSNLYMV MEYVAGGEMF SHLRRIGRFS EPHARFYAAQ ...文字列: MGSSHHHHHH SSGLVPRGSH MGNAAAAKKG SEQESVKEFL AKAKEDFLKK WETPSQNTAQ LDQFDRIKTL GTGSFGRVML VKHKESGNHY AMKILDKQKV VKLKQIEHTL NEKRILQAVN FPFLVKLEFS FKDNSNLYMV MEYVAGGEMF SHLRRIGRFS EPHARFYAAQ IVLTFEYLHS LDLIYRDLKP ENLLIDQQGY IQVTDFGFAK RVKGRTWTLC GTPEYLAPEI ILSKGYNKAV DWWALGVLIY EMAAGYPPFF ADQPIQIYEK IVSGKVRFPS HFSSDLKDLL RNLLQVDLTK RFGNLKNGVN DIKNHKWFAT TDWIAIYQRK VEAPFIPKFK GPGDTSNFDD YEEEEIRVSI NEKCGKEFTE F |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 8 |
|---|---|
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 支持フィルム - Film thickness: 12 |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277.15 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: SUPER-RESOLUTION / 撮影したグリッド数: 2 / 実像数: 12801 / 平均電子線量: 72.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 1.2 µm / 倍率(公称値): 130000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー