+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Mycobacterium smegmatis inosine monophosphate dehydrogenase (IMPDH) ATP-bound form, compressed | |||||||||
 マップデータ マップデータ | LocScale filtered map | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Octamer / ATP complex / Purine metabolism / IMPDH / OXIDOREDUCTASE | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報IMP dehydrogenase activity / IMP dehydrogenase / GMP biosynthetic process / nucleotide binding / metal ion binding 類似検索 - 分子機能 | |||||||||
| 生物種 |  Mycolicibacterium smegmatis MC2 155 (バクテリア) Mycolicibacterium smegmatis MC2 155 (バクテリア) | |||||||||
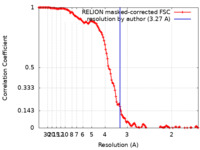
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.27 Å | |||||||||
 データ登録者 データ登録者 | Bulvas O / Kouba T / Pichova I | |||||||||
| 資金援助 | European Union, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2024 ジャーナル: Nat Commun / 年: 2024タイトル: Deciphering the allosteric regulation of mycobacterial inosine-5'-monophosphate dehydrogenase. 著者: Ondřej Bulvas / Zdeněk Knejzlík / Jakub Sýs / Anatolij Filimoněnko / Monika Čížková / Kamila Clarová / Dominik Rejman / Tomáš Kouba / Iva Pichová /  要旨: Allosteric regulation of inosine 5'-monophosphate dehydrogenase (IMPDH), an essential enzyme of purine metabolism, contributes to the homeostasis of adenine and guanine nucleotides. However, the ...Allosteric regulation of inosine 5'-monophosphate dehydrogenase (IMPDH), an essential enzyme of purine metabolism, contributes to the homeostasis of adenine and guanine nucleotides. However, the precise molecular mechanism of IMPDH regulation in bacteria remains unclear. Using biochemical and cryo-EM approaches, we reveal the intricate molecular mechanism of the IMPDH allosteric regulation in mycobacteria. The enzyme is inhibited by both GTP and (p)ppGpp, which bind to the regulatory CBS domains and, via interactions with basic residues in hinge regions, lock the catalytic core domains in a compressed conformation. This results in occlusion of inosine monophosphate (IMP) substrate binding to the active site and, ultimately, inhibition of the enzyme. The GTP and (p)ppGpp allosteric effectors bind to their dedicated sites but stabilize the compressed octamer by a common mechanism. Inhibition is relieved by the competitive displacement of GTP or (p)ppGpp by ATP allowing IMP-induced enzyme expansion. The structural knowledge and mechanistic understanding presented here open up new possibilities for the development of allosteric inhibitors with antibacterial potential. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_18607.map.gz emd_18607.map.gz | 103.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-18607-v30.xml emd-18607-v30.xml emd-18607.xml emd-18607.xml | 19.6 KB 19.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_18607_fsc.xml emd_18607_fsc.xml | 13.5 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_18607.png emd_18607.png | 120.1 KB | ||
| マスクデータ |  emd_18607_msk_1.map emd_18607_msk_1.map | 209.3 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-18607.cif.gz emd-18607.cif.gz | 6.7 KB | ||
| その他 |  emd_18607_additional_1.map.gz emd_18607_additional_1.map.gz emd_18607_half_map_1.map.gz emd_18607_half_map_1.map.gz emd_18607_half_map_2.map.gz emd_18607_half_map_2.map.gz | 195.3 MB 165.8 MB 165.8 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-18607 http://ftp.pdbj.org/pub/emdb/structures/EMD-18607 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-18607 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-18607 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_18607_validation.pdf.gz emd_18607_validation.pdf.gz | 811.8 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_18607_full_validation.pdf.gz emd_18607_full_validation.pdf.gz | 811.4 KB | 表示 | |
| XML形式データ |  emd_18607_validation.xml.gz emd_18607_validation.xml.gz | 21.1 KB | 表示 | |
| CIF形式データ |  emd_18607_validation.cif.gz emd_18607_validation.cif.gz | 27.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18607 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18607 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18607 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18607 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8qqwMC  8pw3C  8q65C  8qqpC  8qqqC  8qqrC  8qqtC  8qqvC  8qqxC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_18607.map.gz / 形式: CCP4 / 大きさ: 209.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_18607.map.gz / 形式: CCP4 / 大きさ: 209.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | LocScale filtered map | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.8336 Å | ||||||||||||||||||||||||||||||||||||
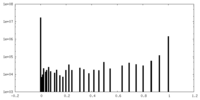
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_18607_msk_1.map emd_18607_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
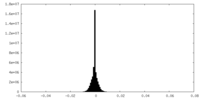
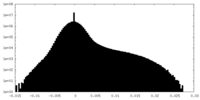
| 密度ヒストグラム |
-追加マップ: RELION post-processed map
| ファイル | emd_18607_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | RELION post-processed map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
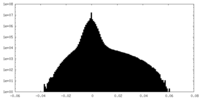
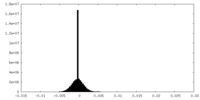
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_18607_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
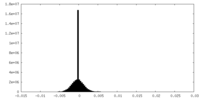
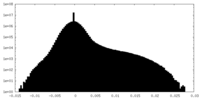
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_18607_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Octameric assembly of inosine monophosphate dehydrogenase in comp...
| 全体 | 名称: Octameric assembly of inosine monophosphate dehydrogenase in complex with ATP |
|---|---|
| 要素 |
|
-超分子 #1: Octameric assembly of inosine monophosphate dehydrogenase in comp...
| 超分子 | 名称: Octameric assembly of inosine monophosphate dehydrogenase in complex with ATP タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Mycolicibacterium smegmatis MC2 155 (バクテリア) Mycolicibacterium smegmatis MC2 155 (バクテリア) |
| 分子量 | 理論値: 426.658 KDa |
-分子 #1: Inosine-5'-monophosphate dehydrogenase
| 分子 | 名称: Inosine-5'-monophosphate dehydrogenase / タイプ: protein_or_peptide / ID: 1 / コピー数: 8 / 光学異性体: LEVO / EC番号: IMP dehydrogenase |
|---|---|
| 由来(天然) | 生物種:  Mycolicibacterium smegmatis MC2 155 (バクテリア) Mycolicibacterium smegmatis MC2 155 (バクテリア)株: MC2 155 |
| 分子量 | 理論値: 53.388988 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MSIAESSVPI AVPVPTGGDD PTKVAMLGLT FDDVLLLPAA SDVVPATADT SSQLTKRIRL RVPLVSSAMD TVTESRMAIA MARAGGMGV LHRNLPVAEQ AGQVETVKRS EAGMVTDPVT CSPDNTLAEV DAMCARFRIS GLPVVDDTGE LVGIITNRDM R FEVDQSKP ...文字列: MSIAESSVPI AVPVPTGGDD PTKVAMLGLT FDDVLLLPAA SDVVPATADT SSQLTKRIRL RVPLVSSAMD TVTESRMAIA MARAGGMGV LHRNLPVAEQ AGQVETVKRS EAGMVTDPVT CSPDNTLAEV DAMCARFRIS GLPVVDDTGE LVGIITNRDM R FEVDQSKP VSEVMTKAPL ITAKEGVSAE AALGLLRRHK IEKLPIVDGH GKLTGLITVK DFVKTEQFPL STKDSDGRLL VG AAVGVGD DAWTRAMTLV DAGVDVLIVD TAHAHNRGVL DMVSRLKQAV GERVDVVGGN VATRAAAAAL VEAGADAVKV GVG PGSICT TRVVAGVGAP QITAILEAVA ACKPYGVPVI ADGGLQYSGD IAKALAAGAS TAMLGSLLAG TAESPGELIF VNGK QFKSY RGMGSLGAMQ GRGAAKSYSK DRYFQDDVLS EDKLVPEGIE GRVPFRGPLG TVIHQLTGGL RAAMGYTGSA TIEQL QQAQ FVQITAAGLK ESHPHDITMT VEAPNYYTR UniProtKB: Inosine-5'-monophosphate dehydrogenase |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 構成要素:
詳細: 50 mM HEPES (pH 7.5), 200 mM KCl, 5 mM DTT, 4 mM MgCl2 Ligand: 2 mM ATP + 1 mM IMP | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 実像数: 11232 / 平均露光時間: 2.0 sec. / 平均電子線量: 43.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.6 µm / 最小 デフォーカス(公称値): 0.5 µm / 倍率(公称値): 165000 |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | PDB ID: Chain - Source name: AlphaFold / Chain - Initial model type: in silico model |
|---|---|
| 詳細 | Initial fitting was done in UCSF ChimeraX. Model refinement was done by iterative cycles of manual fitting with Coot and ISOLDE and automated fitting with phenix.real_space_refine. |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT / 温度因子: 50.2 / 当てはまり具合の基準: CC coefficient |
| 得られたモデル |  PDB-8qqw: |
 ムービー
ムービー コントローラー
コントローラー













 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)