+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Respiratory supercomplex (III2-IV2) from Mycobacterium smegmatis | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | RESPIRATORY SUPERCOMPLEX / MEMBRANE PROTEIN / ACTINOBACTERIA / ELECTRON TRANSPORT | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報aerobic electron transport chain / oxidative phosphorylation / cytochrome-c oxidase / quinol-cytochrome-c reductase / ubiquinol-cytochrome-c reductase activity / cytochrome-c oxidase activity / superoxide dismutase / superoxide dismutase activity / electron transport coupled proton transport / : ...aerobic electron transport chain / oxidative phosphorylation / cytochrome-c oxidase / quinol-cytochrome-c reductase / ubiquinol-cytochrome-c reductase activity / cytochrome-c oxidase activity / superoxide dismutase / superoxide dismutase activity / electron transport coupled proton transport / : / respiratory electron transport chain / electron transport chain / 2 iron, 2 sulfur cluster binding / oxidoreductase activity / iron ion binding / copper ion binding / heme binding / membrane / metal ion binding / plasma membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |  Mycolicibacterium smegmatis (バクテリア) Mycolicibacterium smegmatis (バクテリア) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.3 Å | |||||||||
 データ登録者 データ登録者 | Kovalova T / Krol S / Sjostrand D / Riepl D / Gamiz-Hernandez A / Brzezinski P / Kaila V / Hogbom M | |||||||||
| 資金援助 |  スウェーデン, 1件 スウェーデン, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2024 ジャーナル: Nat Commun / 年: 2024タイトル: Long-range charge transfer mechanism of the IIIIV mycobacterial supercomplex. 著者: Daniel Riepl / Ana P Gamiz-Hernandez / Terezia Kovalova / Sylwia M Król / Sophie L Mader / Dan Sjöstrand / Martin Högbom / Peter Brzezinski / Ville R I Kaila /  要旨: Aerobic life is powered by membrane-bound redox enzymes that shuttle electrons to oxygen and transfer protons across a biological membrane. Structural studies suggest that these energy-transducing ...Aerobic life is powered by membrane-bound redox enzymes that shuttle electrons to oxygen and transfer protons across a biological membrane. Structural studies suggest that these energy-transducing enzymes operate as higher-order supercomplexes, but their functional role remains poorly understood and highly debated. Here we resolve the functional dynamics of the 0.7 MDa IIIIV obligate supercomplex from Mycobacterium smegmatis, a close relative of M. tuberculosis, the causative agent of tuberculosis. By combining computational, biochemical, and high-resolution (2.3 Å) cryo-electron microscopy experiments, we show how the mycobacterial supercomplex catalyses long-range charge transport from its menaquinol oxidation site to the binuclear active site for oxygen reduction. Our data reveal proton and electron pathways responsible for the charge transfer reactions, mechanistic principles of the quinone catalysis, and how unique molecular adaptations, water molecules, and lipid interactions enable the proton-coupled electron transfer (PCET) reactions. Our combined findings provide a mechanistic blueprint of mycobacterial supercomplexes and a basis for developing drugs against pathogenic bacteria. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_17211.map.gz emd_17211.map.gz | 567.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-17211-v30.xml emd-17211-v30.xml emd-17211.xml emd-17211.xml | 36.6 KB 36.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_17211.png emd_17211.png | 85.4 KB | ||
| マスクデータ |  emd_17211_msk_1.map emd_17211_msk_1.map | 600.7 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-17211.cif.gz emd-17211.cif.gz | 9.7 KB | ||
| その他 |  emd_17211_half_map_1.map.gz emd_17211_half_map_1.map.gz emd_17211_half_map_2.map.gz emd_17211_half_map_2.map.gz | 556.7 MB 556.7 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-17211 http://ftp.pdbj.org/pub/emdb/structures/EMD-17211 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-17211 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-17211 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_17211_validation.pdf.gz emd_17211_validation.pdf.gz | 1.1 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_17211_full_validation.pdf.gz emd_17211_full_validation.pdf.gz | 1.1 MB | 表示 | |
| XML形式データ |  emd_17211_validation.xml.gz emd_17211_validation.xml.gz | 19.5 KB | 表示 | |
| CIF形式データ |  emd_17211_validation.cif.gz emd_17211_validation.cif.gz | 23.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17211 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17211 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17211 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17211 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8ovdMC  8ovcC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_17211.map.gz / 形式: CCP4 / 大きさ: 600.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_17211.map.gz / 形式: CCP4 / 大きさ: 600.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.828 Å | ||||||||||||||||||||||||||||||||||||
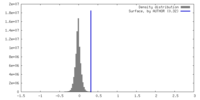
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_17211_msk_1.map emd_17211_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
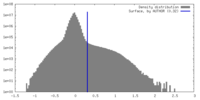
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_17211_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
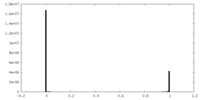
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_17211_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
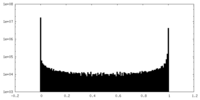
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
+全体 : The respiratory supercomplex
+超分子 #1: The respiratory supercomplex
+分子 #1: Cytochrome bc1 complex cytochrome c subunit
+分子 #2: Cytochrome bc1 complex cytochrome c subunit
+分子 #3: Cytochrome bc1 complex cytochrome b subunit
+分子 #4: Transmembrane protein
+分子 #5: Probable cytochrome c oxidase subunit 3
+分子 #6: Cytochrome c oxidase polypeptide 4
+分子 #7: Cytochrome c oxidase subunit 1
+分子 #8: cytochrome-c oxidase
+分子 #9: Cytochrome c oxidase subunit
+分子 #10: Uncharacterized protein MSMEG_4692/MSMEI_4575
+分子 #11: LpqE protein
+分子 #12: Superoxide dismutase [Cu-Zn]
+分子 #13: HEME C
+分子 #14: MENAQUINONE-9
+分子 #15: acyl-phosphatidyl-myo-inositol dimannoside (AcPIM2)
+分子 #16: FE2/S2 (INORGANIC) CLUSTER
+分子 #17: [(2~{R})-3-[[(1~{S},2~{R},3~{S},4~{S},5~{R},6~{R})-2-[(2~{R},3~{S...
+分子 #18: (2R)-2-(hexadecanoyloxy)-3-{[(S)-hydroxy{[(1R,2R,3R,4R,5R,6S)-2,3...
+分子 #19: (1R)-2-(dodecanoyloxy)-1-[(phosphonooxy)methyl]ethyl tetradecanoate
+分子 #20: PROTOPORPHYRIN IX CONTAINING FE
+分子 #21: CARDIOLIPIN
+分子 #22: TRIDECANE
+分子 #23: 1,2-Distearoyl-sn-glycerophosphoethanolamine
+分子 #24: HEME-A
+分子 #25: COPPER (II) ION
+分子 #26: MAGNESIUM ION
+分子 #27: CALCIUM ION
+分子 #28: (2S)-1-(hexadecanoyloxy)propan-2-yl (10S)-10-methyloctadecanoate
+分子 #29: PALMITIC ACID
+分子 #30: water
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 |
|---|---|
| グリッド | モデル: Quantifoil R2/2 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 120 sec. |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 平均電子線量: 40.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.2 µm / 最小 デフォーカス(公称値): 0.6 µm |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期モデル | モデルのタイプ: PDB ENTRY PDBモデル - PDB ID: |
|---|---|
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 2.3 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 208243 |
| 初期 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
| 最終 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
 ムービー
ムービー コントローラー
コントローラー


















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)