[日本語] English
 万見
万見- EMDB-14975: Saccharomyces cerevisiae L-BC virus, open particle, C5 reconstruction -
+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Saccharomyces cerevisiae L-BC virus, open particle, C5 reconstruction | |||||||||
 マップデータ マップデータ | Main map processed (masked and low-pass filtered to 15 A) | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | open particle / totivirus / C5 asymmetric unit / VIRUS | |||||||||
| 機能・相同性 | Major coat protein, L-A virus / L-A virus major coat protein superfamily / L-A virus, major coat protein / viral capsid / viral translational frameshifting / RNA binding / Major capsid protein 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |   Saccharomyces cerevisiae virus L-BC (La) (ウイルス) Saccharomyces cerevisiae virus L-BC (La) (ウイルス) | |||||||||
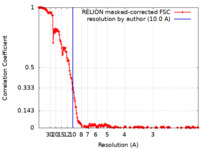
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 10.0 Å | |||||||||
 データ登録者 データ登録者 | Grybchuk D / Prochazkova M / Fuzik T / Konovalovas A / Serva S / Yurchenko V / Plevka P | |||||||||
| 資金援助 |  チェコ, 1件 チェコ, 1件
| |||||||||
 引用 引用 |  ジャーナル: Commun Biol / 年: 2022 ジャーナル: Commun Biol / 年: 2022タイトル: Structures of L-BC virus and its open particle provide insight into Totivirus capsid assembly. 著者: Danyil Grybchuk / Michaela Procházková / Tibor Füzik / Aleksandras Konovalovas / Saulius Serva / Vyacheslav Yurchenko / Pavel Plevka /  要旨: L-BC virus persists in the budding yeast Saccharomyces cerevisiae, whereas other viruses from the family Totiviridae infect a diverse group of organisms including protists, fungi, arthropods, and ...L-BC virus persists in the budding yeast Saccharomyces cerevisiae, whereas other viruses from the family Totiviridae infect a diverse group of organisms including protists, fungi, arthropods, and vertebrates. The presence of totiviruses alters the fitness of the host organisms, for example, by maintaining the killer system in yeast or increasing the virulence of Leishmania guyanensis. Despite the importance of totiviruses for their host survival, there is limited information about Totivirus structure and assembly. Here we used cryo-electron microscopy to determine the structure of L-BC virus to a resolution of 2.9 Å. The L-BC capsid is organized with icosahedral symmetry, with each asymmetric unit composed of two copies of the capsid protein. Decamers of capsid proteins are stabilized by domain swapping of the C-termini of subunits located around icosahedral fivefold axes. We show that capsids of 9% of particles in a purified L-BC sample were open and lacked one decamer of capsid proteins. The existence of the open particles together with domain swapping within a decamer provides evidence that Totiviridae capsids assemble from the decamers of capsid proteins. Furthermore, the open particles may be assembly intermediates that are prepared for the incorporation of the virus (+) strand RNA. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_14975.map.gz emd_14975.map.gz | 569.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-14975-v30.xml emd-14975-v30.xml emd-14975.xml emd-14975.xml | 19.9 KB 19.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_14975_fsc.xml emd_14975_fsc.xml | 20.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_14975.png emd_14975.png | 204.7 KB | ||
| マスクデータ |  emd_14975_msk_1.map emd_14975_msk_1.map | 669.9 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-14975.cif.gz emd-14975.cif.gz | 6.5 KB | ||
| その他 |  emd_14975_half_map_1.map.gz emd_14975_half_map_1.map.gz emd_14975_half_map_2.map.gz emd_14975_half_map_2.map.gz | 540.6 MB 540.5 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-14975 http://ftp.pdbj.org/pub/emdb/structures/EMD-14975 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-14975 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-14975 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_14975_validation.pdf.gz emd_14975_validation.pdf.gz | 1 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_14975_full_validation.pdf.gz emd_14975_full_validation.pdf.gz | 1 MB | 表示 | |
| XML形式データ |  emd_14975_validation.xml.gz emd_14975_validation.xml.gz | 27.3 KB | 表示 | |
| CIF形式データ |  emd_14975_validation.cif.gz emd_14975_validation.cif.gz | 36.5 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-14975 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-14975 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-14975 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-14975 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_14975.map.gz / 形式: CCP4 / 大きさ: 669.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_14975.map.gz / 形式: CCP4 / 大きさ: 669.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Main map processed (masked and low-pass filtered to 15 A) | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.07852 Å | ||||||||||||||||||||||||||||||||||||
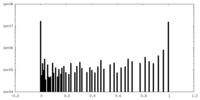
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_14975_msk_1.map emd_14975_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Half-map2
| ファイル | emd_14975_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half-map2 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
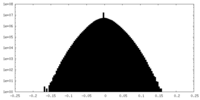
| 密度ヒストグラム |
-ハーフマップ: Half-map1
| ファイル | emd_14975_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half-map1 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
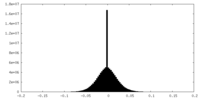
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Saccharomyces cerevisiae virus L-BC (La)
| 全体 | 名称:  Saccharomyces cerevisiae virus L-BC (La) (ウイルス) Saccharomyces cerevisiae virus L-BC (La) (ウイルス) |
|---|---|
| 要素 |
|
-超分子 #1: Saccharomyces cerevisiae virus L-BC (La)
| 超分子 | 名称: Saccharomyces cerevisiae virus L-BC (La) / タイプ: virus / ID: 1 / 親要素: 0 / 含まれる分子: all 詳細: Virus was isolated by shearing with glass beads and overnight precipitation in 5% PEG-4000 and 500 mM NaCl NCBI-ID: 42478 / 生物種: Saccharomyces cerevisiae virus L-BC (La) / ウイルスタイプ: VIRUS-LIKE PARTICLE / ウイルス・単離状態: OTHER / ウイルス・エンベロープ: No / ウイルス・中空状態: Yes |
|---|---|
| 宿主 | 生物種:  |
| ウイルス殻 | Shell ID: 1 / 直径: 400.0 Å / T番号(三角分割数): 2 |
-分子 #1: Major capsid protein
| 分子 | 名称: Major capsid protein / タイプ: protein_or_peptide / ID: 1 / コピー数: 22 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 78.393812 KDa |
| 配列 | 文字列: MSSLLNSLLP EYFKPKTNLN INSSRVQYGF NARIDMQYED DSGTRKGSRP NAFMSNTVAF IGNYEGIIVD DIPILDGLRA DIFDTHGDL DMGLVEDALS KSTMIRRNVP TYTAYASELL YKRNLTSLFY NMLRLYYIKK WGSIKYEKDA IFYDNGHACL L NRQLFPKS ...文字列: MSSLLNSLLP EYFKPKTNLN INSSRVQYGF NARIDMQYED DSGTRKGSRP NAFMSNTVAF IGNYEGIIVD DIPILDGLRA DIFDTHGDL DMGLVEDALS KSTMIRRNVP TYTAYASELL YKRNLTSLFY NMLRLYYIKK WGSIKYEKDA IFYDNGHACL L NRQLFPKS RDASLESSLS LPEAEIAMLD PGLEFPEEDV PAILWHGRVS SRATCILGQA CSEFAPLAPF SIAHYSPQLT RK LFVNAPA GIEPSSGRYT HEDVKDAITI LVSANQAYTD FEAAYLMLAQ TLVSPVPRTA EASAWFINAG MVNMPTLSCA NGY YPALTN VNPYHRLDTW KDTLNHWVAY PDMLFYHSVA MIESCYVELG NVARVSDSDA INKYTFTELS VQGRPVMNRG IIVD LTLVA MRTGREISLP YPVSCGLTRT DALLQGTEIH VPVVVKDIDM PQYYNAIDKD VIEGQETVIK VKQLPPAMYP IYTYG INTT EFYSDHFEDQ VQVEMAPIDN GKAVFNDARK FSKFMSIMRM MGNDVTATDL VTGRKVSNWA DNSSGRFLYT DVKYEG QTA FLVDMDTVKA RDHCWVSIVD PNGTMNLSYK MTNFRAAMFS RNKPLYMTGG SVRTIATGNY RDAAERLRAM DETLRLK PF KITEKLDFRV AAYAIPSLSG SNMPSLHHQE QLQISEVDAE PINPIGEDEL PPDIE UniProtKB: Major capsid protein |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 1.5 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 / 詳細: 20 mM Tris-HCl pH 7.5, 50 mM KCl, 10 mM MgCl2 |
| グリッド | モデル: Quantifoil R2/2 / 材質: COPPER / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY ARRAY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 15 sec. / 前処理 - 雰囲気: OTHER / 前処理 - 気圧: 0.007 kPa / 詳細: Glow discharge current 7 mA |
| 凍結 | 凍結剤: ETHANE-PROPANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV / 詳細: blot force 0, blot time 3 s, 4 C, 100% humidity. |
| 詳細 | Virus was isolated by shearing with glass beads and overnight precipitation in 5% PEG-4000 and 500 mM NaCl |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 温度 | 最低: 70.0 K / 最高: 80.0 K |
| 特殊光学系 | エネルギーフィルター - 名称: GIF Bioquantum / エネルギーフィルター - スリット幅: 10 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / デジタル化 - サイズ - 横: 3600 pixel / デジタル化 - サイズ - 縦: 3600 pixel / デジタル化 - 画像ごとのフレーム数: 1-30 / 撮影したグリッド数: 1 / 実像数: 11977 / 平均露光時間: 6.0 sec. / 平均電子線量: 36.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 30.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 1.7 µm 最小 デフォーカス(公称値): 0.7000000000000001 µm 倍率(公称値): 130000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 詳細 | Initial model generated by RaptorX server |
|---|---|
| 精密化 | 空間: REAL / プロトコル: FLEXIBLE FIT |
| 得られたモデル |  PDB-7zuf: |
 ムービー
ムービー コントローラー
コントローラー









 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)