+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-0289 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of a functional obligate respiratory supercomplex from Mycobacterium smegmatis | |||||||||
 マップデータ マップデータ | Respiratory supercomplex from Mycobacterium smegmatis | |||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報aerobic electron transport chain / cytochrome-c oxidase / oxidative phosphorylation / quinol-cytochrome-c reductase / ubiquinol-cytochrome-c reductase activity / cytochrome-c oxidase activity / : / electron transport coupled proton transport / ATP synthesis coupled electron transport / aerobic respiration ...aerobic electron transport chain / cytochrome-c oxidase / oxidative phosphorylation / quinol-cytochrome-c reductase / ubiquinol-cytochrome-c reductase activity / cytochrome-c oxidase activity / : / electron transport coupled proton transport / ATP synthesis coupled electron transport / aerobic respiration / respiratory electron transport chain / electron transport chain / 2 iron, 2 sulfur cluster binding / membrane => GO:0016020 / oxidoreductase activity / iron ion binding / copper ion binding / heme binding / membrane / metal ion binding / plasma membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |  Mycobacterium smegmatis str. MC2 155 (バクテリア) / Mycobacterium smegmatis str. MC2 155 (バクテリア) /  Mycobacterium smegmatis (strain ATCC 700084 / mc(2)155) (バクテリア) / Mycobacterium smegmatis (strain ATCC 700084 / mc(2)155) (バクテリア) /  Mycobacterium smegmatis MC2 155 (バクテリア) Mycobacterium smegmatis MC2 155 (バクテリア) | |||||||||
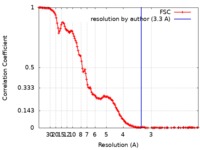
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.3 Å | |||||||||
 データ登録者 データ登録者 | Wiseman B / Nitharwal RG / Fedotovskaya O / Schafer J / Guo H / Kuang Q / Benlekbir S / Sjostrand D / Adelroth P / Rubinstein JL ...Wiseman B / Nitharwal RG / Fedotovskaya O / Schafer J / Guo H / Kuang Q / Benlekbir S / Sjostrand D / Adelroth P / Rubinstein JL / Brzezinski P / Hogbom M | |||||||||
| 資金援助 |  カナダ, カナダ,  スウェーデン, 2件 スウェーデン, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nat Struct Mol Biol / 年: 2018 ジャーナル: Nat Struct Mol Biol / 年: 2018タイトル: Structure of a functional obligate complex IIIIV respiratory supercomplex from Mycobacterium smegmatis. 著者: Benjamin Wiseman / Ram Gopal Nitharwal / Olga Fedotovskaya / Jacob Schäfer / Hui Guo / Qie Kuang / Samir Benlekbir / Dan Sjöstrand / Pia Ädelroth / John L Rubinstein / Peter Brzezinski / Martin Högbom /    要旨: In the mycobacterial electron-transport chain, respiratory complex III passes electrons from menaquinol to complex IV, which in turn reduces oxygen, the terminal acceptor. Electron transfer is ...In the mycobacterial electron-transport chain, respiratory complex III passes electrons from menaquinol to complex IV, which in turn reduces oxygen, the terminal acceptor. Electron transfer is coupled to transmembrane proton translocation, thus establishing the electrochemical proton gradient that drives ATP synthesis. We isolated, biochemically characterized, and determined the structure of the obligate IIIIV supercomplex from Mycobacterium smegmatis, a model for Mycobacterium tuberculosis. The supercomplex has quinol:O oxidoreductase activity without exogenous cytochrome c and includes a superoxide dismutase subunit that may detoxify reactive oxygen species produced during respiration. We found menaquinone bound in both the Q and Q sites of complex III. The complex III-intrinsic diheme cytochrome cc subunit, which functionally replaces both cytochrome c and soluble cytochrome c in canonical electron-transport chains, displays two conformations: one in which it provides a direct electronic link to complex IV and another in which it serves as an electrical switch interrupting the connection. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_0289.map.gz emd_0289.map.gz | 10.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-0289-v30.xml emd-0289-v30.xml emd-0289.xml emd-0289.xml | 29.5 KB 29.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_0289_fsc.xml emd_0289_fsc.xml | 15.8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_0289.png emd_0289.png | 59.6 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-0289 http://ftp.pdbj.org/pub/emdb/structures/EMD-0289 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0289 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0289 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_0289_validation.pdf.gz emd_0289_validation.pdf.gz | 249.8 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_0289_full_validation.pdf.gz emd_0289_full_validation.pdf.gz | 249 KB | 表示 | |
| XML形式データ |  emd_0289_validation.xml.gz emd_0289_validation.xml.gz | 13.6 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0289 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0289 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0289 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0289 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_0289.map.gz / 形式: CCP4 / 大きさ: 209.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_0289.map.gz / 形式: CCP4 / 大きさ: 209.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Respiratory supercomplex from Mycobacterium smegmatis | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.06 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
+全体 : Respiratory Supercomplex from Mycobacterium smegmatis
+超分子 #1: Respiratory Supercomplex from Mycobacterium smegmatis
+分子 #1: Ubiquinol-cytochrome c reductase iron-sulfur subunit
+分子 #2: Co-purified unknown transmembrane helices built as polyALA
+分子 #3: Co-purified unknown transmembrane helices built as polyALA
+分子 #4: Co-purified unknown peptide built as polyALA
+分子 #5: Co-purified unknown peptide built as polyALA
+分子 #6: Cytochrome bc1 complex cytochrome c subunit
+分子 #7: Cytochrome c oxidase subunit 2
+分子 #8: MSMEG_4693
+分子 #9: Uncharacterized protein MSMEG_4692/MSMEI_4575
+分子 #10: Cytochrome c oxidase subunit 1
+分子 #11: Cytochrome c oxidase polypeptide 4
+分子 #12: Cytochrome c oxidase subunit 3
+分子 #13: Ubiquinol-cytochrome C reductase QcrB
+分子 #14: FE2/S2 (INORGANIC) CLUSTER
+分子 #15: CARDIOLIPIN
+分子 #16: MENAQUINONE-9
+分子 #17: COPPER (II) ION
+分子 #18: HEME-AS
+分子 #19: HEME C
+分子 #20: PROTOPORPHYRIN IX CONTAINING FE
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 5 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 |
| グリッド | 材質: COPPER / メッシュ: 300 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 雰囲気: AIR / 詳細: 40 seconds at 20 mA |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: COUNTING / 撮影したグリッド数: 1 / 実像数: 5316 / 平均露光時間: 60.0 sec. / 平均電子線量: 43.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 詳細 | Model was built de novo; except for chains i,j which are polyALA homology models rigid-body docked into low resolution density. |
|---|---|
| 精密化 | 空間: REAL / プロトコル: OTHER 当てはまり具合の基準: Cross-correlation coefficient |
| 得られたモデル |  PDB-6hwh: |
 ムービー
ムービー コントローラー
コントローラー