+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-1674 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | The cryo-EM structure of actin filament in the presence of phosphate | |||||||||
 マップデータ マップデータ | This is an image of a surface with B-factor correction. | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード |  actin (アクチン) / actin (アクチン) /  cytoskeleton (細胞骨格) / cytoskeleton (細胞骨格) /  cell adhesion (細胞接着) / cell adhesion (細胞接着) /  cellular signaling / cellular signaling /  cytokinesis (細胞質分裂) / cytokinesis (細胞質分裂) /  muscle (骨格筋) muscle (骨格筋) | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報cytoskeletal motor activator activity /  tropomyosin binding / tropomyosin binding /  myosin heavy chain binding / mesenchyme migration / myosin heavy chain binding / mesenchyme migration /  troponin I binding / actin filament bundle / filamentous actin / actin filament bundle assembly / skeletal muscle thin filament assembly / striated muscle thin filament ...cytoskeletal motor activator activity / troponin I binding / actin filament bundle / filamentous actin / actin filament bundle assembly / skeletal muscle thin filament assembly / striated muscle thin filament ...cytoskeletal motor activator activity /  tropomyosin binding / tropomyosin binding /  myosin heavy chain binding / mesenchyme migration / myosin heavy chain binding / mesenchyme migration /  troponin I binding / actin filament bundle / filamentous actin / actin filament bundle assembly / skeletal muscle thin filament assembly / striated muscle thin filament / skeletal muscle myofibril / actin monomer binding / skeletal muscle fiber development / troponin I binding / actin filament bundle / filamentous actin / actin filament bundle assembly / skeletal muscle thin filament assembly / striated muscle thin filament / skeletal muscle myofibril / actin monomer binding / skeletal muscle fiber development /  stress fiber / stress fiber /  titin binding / actin filament polymerization / titin binding / actin filament polymerization /  filopodium / filopodium /  マイクロフィラメント / マイクロフィラメント /  加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与 / calcium-dependent protein binding / 加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与 / calcium-dependent protein binding /  lamellipodium / lamellipodium /  cell body / cell body /  hydrolase activity / protein domain specific binding / hydrolase activity / protein domain specific binding /  calcium ion binding / positive regulation of gene expression / magnesium ion binding / calcium ion binding / positive regulation of gene expression / magnesium ion binding /  ATP binding / identical protein binding / ATP binding / identical protein binding /  細胞質 細胞質類似検索 - 分子機能 | |||||||||
| 生物種 |   Oryctolagus cuniculus (ウサギ) Oryctolagus cuniculus (ウサギ) | |||||||||
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 6.0 Å クライオ電子顕微鏡法 / 解像度: 6.0 Å | |||||||||
 データ登録者 データ登録者 | Murakami K / Yasunaga T / Noguchi TQ / Uyeda TQ / Wakabayashi T | |||||||||
 引用 引用 |  ジャーナル: Cell / 年: 2010 ジャーナル: Cell / 年: 2010タイトル: Structural basis for actin assembly, activation of ATP hydrolysis, and delayed phosphate release. 著者: Kenji Murakami / Takuo Yasunaga / Taro Q P Noguchi / Yuki Gomibuchi / Kien X Ngo / Taro Q P Uyeda / Takeyuki Wakabayashi /  要旨: Assembled actin filaments support cellular signaling, intracellular trafficking, and cytokinesis. ATP hydrolysis triggered by actin assembly provides the structural cues for filament turnover in vivo. ...Assembled actin filaments support cellular signaling, intracellular trafficking, and cytokinesis. ATP hydrolysis triggered by actin assembly provides the structural cues for filament turnover in vivo. Here, we present the cryo-electron microscopic (cryo-EM) structure of filamentous actin (F-actin) in the presence of phosphate, with the visualization of some α-helical backbones and large side chains. A complete atomic model based on the EM map identified intermolecular interactions mediated by bound magnesium and phosphate ions. Comparison of the F-actin model with G-actin monomer crystal structures reveals a critical role for bending of the conserved proline-rich loop in triggering phosphate release following ATP hydrolysis. Crystal structures of G-actin show that mutations in this loop trap the catalytic site in two intermediate states of the ATPase cycle. The combined structural information allows us to propose a detailed molecular mechanism for the biochemical events, including actin polymerization and ATPase activation, critical for actin filament dynamics. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_1674.map.gz emd_1674.map.gz | 2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-1674-v30.xml emd-1674-v30.xml emd-1674.xml emd-1674.xml | 10.4 KB 10.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  1674.png 1674.png | 345 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-1674 http://ftp.pdbj.org/pub/emdb/structures/EMD-1674 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1674 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1674 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_1674.map.gz / 形式: CCP4 / 大きさ: 6.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_1674.map.gz / 形式: CCP4 / 大きさ: 6.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | This is an image of a surface with B-factor correction. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 2.275 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
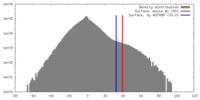
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Actin filament in the presence of phosphate
| 全体 | 名称: Actin filament in the presence of phosphate マイクロフィラメント マイクロフィラメント |
|---|---|
| 要素 |
|
-超分子 #1000: Actin filament in the presence of phosphate
| 超分子 | 名称: Actin filament in the presence of phosphate / タイプ: sample / ID: 1000 / 集合状態: Filament / Number unique components: 1 |
|---|---|
| 分子量 | 理論値: 1.17 MDa |
-分子 #1: Actin
| 分子 | 名称: Actin / タイプ: protein_or_peptide / ID: 1 / Name.synonym: Actin / コピー数: 26 / 集合状態: Filament / 組換発現: No / データベース: NCBI |
|---|---|
| 由来(天然) | 生物種:   Oryctolagus cuniculus (ウサギ) / 別称: Rabbit / 組織: Muscle Oryctolagus cuniculus (ウサギ) / 別称: Rabbit / 組織: Muscle |
| 分子量 | 理論値: 45 KDa |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 詳細: 50 mM NaCl, 5 mM MgCl2, 0.025 mM ATP, 10 mM sodium phosphate (pH 7.4), 0.05 %NaN3, and 0.7 mM DTT |
|---|---|
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 90 % / チャンバー内温度: 77 K / 装置: OTHER |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | HITACHI EF2000 |
|---|---|
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD Bright-field microscopy / 最大 デフォーカス(公称値): 1.5 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 100000 Bright-field microscopy / 最大 デフォーカス(公称値): 1.5 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 100000 |
| 特殊光学系 | エネルギーフィルター - 名称: HITACH |
| 試料ステージ | 試料ホルダー: Side entry liquid nitrogen-cooled cryo specimen holder 試料ホルダーモデル: GATAN LIQUID NITROGEN |
| 温度 | 最低: 77 K / 最高: 77 K / 平均: 77 K |
| 撮影 | カテゴリ: CCD / フィルム・検出器のモデル: GENERIC CCD / デジタル化 - サンプリング間隔: 2.275 µm / 平均電子線量: 15 e/Å2 |
| Tilt angle min | 0 |
| Tilt angle max | 0 |
- 画像解析
画像解析
| CTF補正 | 詳細: Each particle |
|---|---|
| 最終 2次元分類 | クラス数: 72 |
| 最終 再構成 | アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 6.0 Å / 解像度の算出法: FSC 0.143 CUT-OFF / ソフトウェア - 名称: EOS / 使用した粒子像数: 8000 |
-原子モデル構築 1
| ソフトウェア | 名称: O, NAMD, EOS |
|---|---|
| 詳細 | Protocol: Real-space refinement. The initial model was docked manually and refined using O, NAMD, and EOS. |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT / 当てはまり具合の基準: R-factor |
| 得られたモデル |  PDB-3g37: |
 ムービー
ムービー コントローラー
コントローラー





















 Z (Sec.)
Z (Sec.) X (Row.)
X (Row.) Y (Col.)
Y (Col.)