+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | 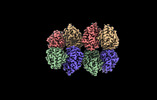 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of the Glutaminase C core filament (fGAC) | |||||||||
 マップデータ マップデータ | Local refinement, after helical refinement with D2 symmetry expansion | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード |  Mitochondria (ミトコンドリア) / Mitochondria (ミトコンドリア) /  Filament / Filament /  HYDROLASE (加水分解酵素) HYDROLASE (加水分解酵素) | |||||||||
| 機能・相同性 |  グルタミナーゼ / Isoform 2 of Glutaminase kidney isoform, mitochondrial グルタミナーゼ / Isoform 2 of Glutaminase kidney isoform, mitochondrial 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |   Mus musculus (ハツカネズミ) Mus musculus (ハツカネズミ) | |||||||||
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.1 Å クライオ電子顕微鏡法 / 解像度: 3.1 Å | |||||||||
 データ登録者 データ登録者 | Ambrosio AL / Dias SM / Quesnay JE / Portugal RV / Cassago A / van Heel MG / Islam Z / Rodrigues CT | |||||||||
| 資金援助 |  ブラジル, 1件 ブラジル, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Struct Mol Biol / 年: 2023 ジャーナル: Nat Struct Mol Biol / 年: 2023タイトル: Molecular mechanism of glutaminase activation through filamentation and the role of filaments in mitophagy protection. 著者: Douglas Adamoski / Marilia Meira Dias / Jose Edwin Neciosup Quesñay / Zhengyi Yang / Ievgeniia Zagoriy / Anna M Steyer / Camila Tanimoto Rodrigues / Alliny Cristiny da Silva Bastos / Bianca ...著者: Douglas Adamoski / Marilia Meira Dias / Jose Edwin Neciosup Quesñay / Zhengyi Yang / Ievgeniia Zagoriy / Anna M Steyer / Camila Tanimoto Rodrigues / Alliny Cristiny da Silva Bastos / Bianca Novaes da Silva / Renna Karoline Eloi Costa / Flávia Mayumi Odahara de Abreu / Zeyaul Islam / Alexandre Cassago / Marin Gerard van Heel / Sílvio Roberto Consonni / Simone Mattei / Julia Mahamid / Rodrigo Villares Portugal / Andre Luis Berteli Ambrosio / Sandra Martha Gomes Dias /     要旨: Glutaminase (GLS), which deaminates glutamine to form glutamate, is a mitochondrial tetrameric protein complex. Although inorganic phosphate (Pi) is known to promote GLS filamentation and activation, ...Glutaminase (GLS), which deaminates glutamine to form glutamate, is a mitochondrial tetrameric protein complex. Although inorganic phosphate (Pi) is known to promote GLS filamentation and activation, the molecular basis of this mechanism is unknown. Here we aimed to determine the molecular mechanism of Pi-induced mouse GLS filamentation and its impact on mitochondrial physiology. Single-particle cryogenic electron microscopy revealed an allosteric mechanism in which Pi binding at the tetramer interface and the activation loop is coupled to direct nucleophile activation at the active site. The active conformation is prone to enzyme filamentation. Notably, human GLS filaments form inside tubulated mitochondria following glutamine withdrawal, as shown by in situ cryo-electron tomography of cells thinned by cryo-focused ion beam milling. Mitochondria with GLS filaments exhibit increased protection from mitophagy. We reveal roles of filamentous GLS in mitochondrial morphology and recycling. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_28013.map.gz emd_28013.map.gz | 230 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-28013-v30.xml emd-28013-v30.xml emd-28013.xml emd-28013.xml | 20 KB 20 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_28013_fsc.xml emd_28013_fsc.xml | 13.2 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_28013.png emd_28013.png | 50.8 KB | ||
| Filedesc metadata |  emd-28013.cif.gz emd-28013.cif.gz | 6.6 KB | ||
| その他 |  emd_28013_half_map_1.map.gz emd_28013_half_map_1.map.gz emd_28013_half_map_2.map.gz emd_28013_half_map_2.map.gz | 226.9 MB 226.9 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-28013 http://ftp.pdbj.org/pub/emdb/structures/EMD-28013 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-28013 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-28013 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8ec6MC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_28013.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_28013.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Local refinement, after helical refinement with D2 symmetry expansion | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.1 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: Half-map A
| ファイル | emd_28013_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half-map A | ||||||||||||
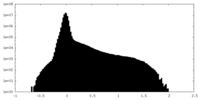
| 投影像・断面図 |
| ||||||||||||
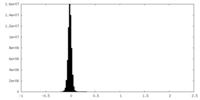
| 密度ヒストグラム |
-ハーフマップ: Half-map B
| ファイル | emd_28013_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half-map B | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
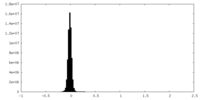
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Glutaminase C filament, bound to inorganic phosphate
| 全体 | 名称: Glutaminase C filament, bound to inorganic phosphate |
|---|---|
| 要素 |
|
-超分子 #1: Glutaminase C filament, bound to inorganic phosphate
| 超分子 | 名称: Glutaminase C filament, bound to inorganic phosphate タイプ: organelle_or_cellular_component / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:   Mus musculus (ハツカネズミ) / Organelle: Mitochondria / 細胞中の位置: Matrix Mus musculus (ハツカネズミ) / Organelle: Mitochondria / 細胞中の位置: Matrix |
| 分子量 | 理論値: 0.53 kDa/nm |
-分子 #1: Isoform 2 of Glutaminase kidney isoform, mitochondrial
| 分子 | 名称: Isoform 2 of Glutaminase kidney isoform, mitochondrial タイプ: protein_or_peptide / ID: 1 / コピー数: 8 / 光学異性体: LEVO / EC番号:  グルタミナーゼ グルタミナーゼ |
|---|---|
| 由来(天然) | 生物種:   Mus musculus (ハツカネズミ) Mus musculus (ハツカネズミ) |
| 分子量 | 理論値: 53.326961 KDa |
| 組換発現 | 生物種:   Escherichia coli BL21(DE3) (大腸菌) Escherichia coli BL21(DE3) (大腸菌) |
| 配列 | 文字列: GSHMVAAGDN KIKQGLLPSL EDLLFYTIAE GQEKIPVHKF ITALKSTGLR TSDPRLKECM DMLRLTLQTT SDGVMLDKDL FKKCVQSNI VLLTQAFRRK FVIPDFMSFT SHIDELYESA KKQSGGKVAD YIPQLAKFSP DLWGVSVCTV DGQRHSIGDT K VPFCLQSC ...文字列: GSHMVAAGDN KIKQGLLPSL EDLLFYTIAE GQEKIPVHKF ITALKSTGLR TSDPRLKECM DMLRLTLQTT SDGVMLDKDL FKKCVQSNI VLLTQAFRRK FVIPDFMSFT SHIDELYESA KKQSGGKVAD YIPQLAKFSP DLWGVSVCTV DGQRHSIGDT K VPFCLQSC VKPLKYAIAV NDLGTEYVHR YVGKEPSGLR FNKLFLNEDD KPHNPMVNAG AIVVTSLIKQ GVNNAEKFDY VM QFLNKMA GNEYVGFSNA TFQSERESGD RNFAIGYYLK EKKCFPEGTD MVGILDFYFQ LCSIEVTCES ASVMAATLAN GGF CPITGE RVLSPEAVRN TLSLMHSCGM YDFSGQFAFH VGLPAKSGVA GGILLVVPNV MGMMCWSPPL DKMGNSVKGI HFCH DLVSL CNFHNYDNLR HFAKKLDPRR EGGDQRHSFG PLDYESLQQE LALKDTVWKK VSPESSDDTS TTVVYRMESL GERS UniProtKB: Isoform 2 of Glutaminase kidney isoform, mitochondrial |
-分子 #2: PHOSPHATE ION
| 分子 | 名称: PHOSPHATE ION / タイプ: ligand / ID: 2 / コピー数: 8 / 式: PO4 |
|---|---|
| 分子量 | 理論値: 94.971 Da |
| Chemical component information |  ChemComp-PO4: |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 濃度 | 0.33 mg/mL | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8.5 構成要素:
| |||||||||||||||
| グリッド | モデル: Quantifoil R2/2 / 材質: COPPER / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE | |||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV | |||||||||||||||
| 詳細 | In the presence of phosphate, GAC polymerizes and becomes polydisperse. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 最大 デフォーカス(補正後): 3.0 µm / 最小 デフォーカス(補正後): 2.0 µm / 倍率(補正後): 59000 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 0.01 mm / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 2.0 µm / 倍率(公称値): 59000 Bright-field microscopy / Cs: 0.01 mm / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 2.0 µm / 倍率(公称値): 59000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: COUNTING / 平均電子線量: 30.0 e/Å2 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | PDB ID: Chain - Chain ID: A / Chain - Residue range: 128-674 / Chain - Source name: PDB / Chain - Initial model type: experimental model |
|---|---|
| 詳細 | run = *minimization_global *rigid_body local_grid_search *adp *occupancy *nqh_flips |
| 精密化 | 空間: REAL / プロトコル: FLEXIBLE FIT / 温度因子: 162.1 / 当てはまり具合の基準: Correlation Coefficient |
| 得られたモデル |  PDB-8ec6: |
 ムービー
ムービー コントローラー
コントローラー



 Z
Z Y
Y X
X