+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 7y5n | ||||||
|---|---|---|---|---|---|---|---|
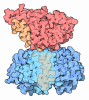
| タイトル | Structure of 1:1 PAPP-A.ProMBP complex(half map) | ||||||
 要素 要素 |
| ||||||
 キーワード キーワード | METAL BINDING PROTEIN/HYDROLASE /  Hydrolase (加水分解酵素) / METAL BINDING PROTEIN-HYDROLASE complex Hydrolase (加水分解酵素) / METAL BINDING PROTEIN-HYDROLASE complex | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報extracellular matrix structural constituent conferring compression resistance / defense response to nematode /  パパリシン-1 / response to follicle-stimulating hormone / negative regulation of macrophage cytokine production / protein metabolic process / negative regulation of interleukin-10 production / response to dexamethasone / positive regulation of interleukin-4 production / パパリシン-1 / response to follicle-stimulating hormone / negative regulation of macrophage cytokine production / protein metabolic process / negative regulation of interleukin-10 production / response to dexamethasone / positive regulation of interleukin-4 production /  小胞 ...extracellular matrix structural constituent conferring compression resistance / defense response to nematode / 小胞 ...extracellular matrix structural constituent conferring compression resistance / defense response to nematode /  パパリシン-1 / response to follicle-stimulating hormone / negative regulation of macrophage cytokine production / protein metabolic process / negative regulation of interleukin-10 production / response to dexamethasone / positive regulation of interleukin-4 production / パパリシン-1 / response to follicle-stimulating hormone / negative regulation of macrophage cytokine production / protein metabolic process / negative regulation of interleukin-10 production / response to dexamethasone / positive regulation of interleukin-4 production /  小胞 / female pregnancy / protein catabolic process / 小胞 / female pregnancy / protein catabolic process /  metalloendopeptidase activity / Regulation of Insulin-like Growth Factor (IGF) transport and uptake by Insulin-like Growth Factor Binding Proteins (IGFBPs) / metalloendopeptidase activity / Regulation of Insulin-like Growth Factor (IGF) transport and uptake by Insulin-like Growth Factor Binding Proteins (IGFBPs) /  metallopeptidase activity / metallopeptidase activity /  heparin binding / heparin binding /  carbohydrate binding / collagen-containing extracellular matrix / ficolin-1-rich granule lumen / cell surface receptor signaling pathway / defense response to bacterium / carbohydrate binding / collagen-containing extracellular matrix / ficolin-1-rich granule lumen / cell surface receptor signaling pathway / defense response to bacterium /  免疫応答 / Neutrophil degranulation / 免疫応答 / Neutrophil degranulation /  タンパク質分解 / タンパク質分解 /  extracellular space / extracellular exosome / zinc ion binding / extracellular region extracellular space / extracellular exosome / zinc ion binding / extracellular region類似検索 - 分子機能 | ||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||
| 手法 |  電子顕微鏡法 / 電子顕微鏡法 /  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.45 Å クライオ電子顕微鏡法 / 解像度: 3.45 Å | ||||||
 データ登録者 データ登録者 | Zhong, Q.H. / Chu, H.L. / Wang, G.P. / Zhang, C. / Wei, Y. / Qiao, J. / Hang, J. | ||||||
| 資金援助 |  中国, 1件 中国, 1件
| ||||||
 引用 引用 |  ジャーナル: Cell Discov / 年: 2022 ジャーナル: Cell Discov / 年: 2022タイトル: Structural insights into the covalent regulation of PAPP-A activity by proMBP and STC2. 著者: Qihang Zhong / Honglei Chu / Guopeng Wang / Cheng Zhang / Rong Li / Fusheng Guo / Xinlu Meng / Xiaoguang Lei / Youli Zhou / Ruobing Ren / Lin Tao / Ningning Li / Ning Gao / Yuan Wei / Jie Qiao / Jing Hang /  要旨: Originally discovered in the circulation of pregnant women as a protein secreted by placental trophoblasts, the metalloprotease pregnancy-associated plasma protein A (PAPP-A) is also widely expressed ...Originally discovered in the circulation of pregnant women as a protein secreted by placental trophoblasts, the metalloprotease pregnancy-associated plasma protein A (PAPP-A) is also widely expressed by many other tissues. It cleaves insulin-like growth factor-binding proteins (IGFBPs) to increase the bioavailability of IGFs and plays essential roles in multiple growth-promoting processes. While the vast majority of the circulatory PAPP-A in pregnancy is proteolytically inactive due to covalent inhibition by proform of eosinophil major basic protein (proMBP), the activity of PAPP-A can also be covalently inhibited by another less characterized modulator, stanniocalcin-2 (STC2). However, the structural basis of PAPP-A proteolysis and the mechanistic differences between these two modulators are poorly understood. Here we present two cryo-EM structures of endogenous purified PAPP-A in complex with either proMBP or STC2. Both modulators form 2:2 heterotetramer with PAPP-A and establish extensive interactions with multiple domains of PAPP-A that are distal to the catalytic cleft. This exosite-binding property results in a steric hindrance to prevent the binding and cleavage of IGFBPs, while the IGFBP linker region-derived peptides harboring the cleavage sites are no longer sensitive to the modulator treatment. Functional investigation into proMBP-mediated PAPP-A regulation in selective intrauterine growth restriction (sIUGR) pregnancy elucidates that PAPP-A and proMBP collaboratively regulate extravillous trophoblast invasion and the consequent fetal growth. Collectively, our work reveals a novel covalent exosite-competitive inhibition mechanism of PAPP-A and its regulatory effect on placental function. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  7y5n.cif.gz 7y5n.cif.gz | 324.2 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb7y5n.ent.gz pdb7y5n.ent.gz | 246.3 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  7y5n.json.gz 7y5n.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/y5/7y5n https://data.pdbj.org/pub/pdb/validation_reports/y5/7y5n ftp://data.pdbj.org/pub/pdb/validation_reports/y5/7y5n ftp://data.pdbj.org/pub/pdb/validation_reports/y5/7y5n | HTTPS FTP |
|---|
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
-タンパク質 , 2種, 3分子 ACD
| #1: タンパク質 | 分子量: 25236.564 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)   Homo sapiens (ヒト) / 参照: UniProt: P13727 Homo sapiens (ヒト) / 参照: UniProt: P13727 |
|---|---|
| #2: タンパク質 |  パパリシン-1 / Insulin-like growth factor-dependent IGF-binding protein 4 protease / IGF-dependent IGFBP-4 ...Insulin-like growth factor-dependent IGF-binding protein 4 protease / IGF-dependent IGFBP-4 protease / IGFBP-4ase / Pregnancy-associated plasma protein A / PAPP-A パパリシン-1 / Insulin-like growth factor-dependent IGF-binding protein 4 protease / IGF-dependent IGFBP-4 ...Insulin-like growth factor-dependent IGF-binding protein 4 protease / IGF-dependent IGFBP-4 protease / IGFBP-4ase / Pregnancy-associated plasma protein A / PAPP-A分子量: 172475.484 Da / 分子数: 2 / 由来タイプ: 天然 / 由来: (天然)   Homo sapiens (ヒト) / 参照: UniProt: Q13219, Homo sapiens (ヒト) / 参照: UniProt: Q13219,  パパリシン-1 パパリシン-1 |
-糖 , 2種, 11分子 
| #3: 多糖 | 2-acetamido-2-deoxy-beta-D-glucopyranose-(1-4)-2-acetamido-2-deoxy-beta-D-glucopyranose オリゴ糖 / 分子量: 424.401 Da / 分子数: 1 / 由来タイプ: 組換発現 オリゴ糖 / 分子量: 424.401 Da / 分子数: 1 / 由来タイプ: 組換発現 |
|---|---|
| #4: 糖 | ChemComp-NAG /  N-アセチルグルコサミン N-アセチルグルコサミン |
-非ポリマー , 2種, 8分子 


| #5: 化合物 | ChemComp-ZN / |
|---|---|
| #6: 化合物 | ChemComp-CA / |
-詳細
| 研究の焦点であるリガンドがあるか | Y |
|---|
-実験情報
-実験
| 実験 | 手法:  電子顕微鏡法 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法:  単粒子再構成法 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: Structure of 1:1 PAPP-A/ProMBP complex(half map) / タイプ: COMPLEX / Entity ID: #1-#2 / 由来: NATURAL |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 緩衝液 | pH: 7.4 |
| 試料 | 包埋: NO / シャドウイング: NO / 染色 : NO / 凍結 : NO / 凍結 : YES : YES |
| 試料支持 | グリッドの材料: GOLD / グリッドのサイズ: 300 divisions/in. / グリッドのタイプ: Quantifoil R1.2/1.3 |
急速凍結 | 凍結剤: ETHANE |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源 : :  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD Bright-field microscopy / 最大 デフォーカス(公称値): 1200 nm / 最小 デフォーカス(公称値): 700 nm Bright-field microscopy / 最大 デフォーカス(公称値): 1200 nm / 最小 デフォーカス(公称値): 700 nm |
| 試料ホルダ | 凍結剤: NITROGEN |
| 撮影 | 電子線照射量: 60.1 e/Å2 / 検出モード: COUNTING フィルム・検出器のモデル: GATAN K2 QUANTUM (4k x 4k) |
| 電子光学装置 | エネルギーフィルター名称 : GIF Bioquantum / エネルギーフィルタースリット幅: 20 eV : GIF Bioquantum / エネルギーフィルタースリット幅: 20 eV |
- 解析
解析
| ソフトウェア | 名称: PHENIX / バージョン: 1.19.1_4122: / 分類: 精密化 | ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| EMソフトウェア |
| ||||||||||||||||||||||||||||
CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||||||
| 対称性 | 点対称性 : C1 (非対称) : C1 (非対称) | ||||||||||||||||||||||||||||
3次元再構成 | 解像度: 3.45 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 142469 / 対称性のタイプ: POINT | ||||||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー









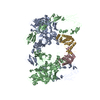
 PDBj
PDBj