[English] 日本語
 Yorodumi
Yorodumi- PDB-5u4s: Crystal structure of a Short chain dehydrogenase from Burkholderi... -
+ Open data
Open data
- Basic information
Basic information
| Entry | Database: PDB / ID: 5u4s | ||||||
|---|---|---|---|---|---|---|---|
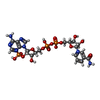
| Title | Crystal structure of a Short chain dehydrogenase from Burkholderia cenocepacia J2315 in complex with NADP. | ||||||
 Components Components | Putative short chain dehydrogenase | ||||||
 Keywords Keywords |  OXIDOREDUCTASE / SSGCID / OXIDOREDUCTASE / SSGCID /  dehydrogenase / dehydrogenase /  structural genomics / Seattle Structural Genomics Center for Infectious Disease structural genomics / Seattle Structural Genomics Center for Infectious Disease | ||||||
| Function / homology | short chain dehydrogenase / Short-chain dehydrogenase/reductase SDR /  oxidoreductase activity / NAD(P)-binding domain superfamily / oxidoreductase activity / NAD(P)-binding domain superfamily /  nucleotide binding / nucleotide binding /  BENZOIC ACID / NADP NICOTINAMIDE-ADENINE-DINUCLEOTIDE PHOSPHATE / BENZOIC ACID / NADP NICOTINAMIDE-ADENINE-DINUCLEOTIDE PHOSPHATE /  PHOSPHATE ION / Putative short chain dehydrogenase PHOSPHATE ION / Putative short chain dehydrogenase Function and homology information Function and homology information | ||||||
| Biological species |   Burkholderia cenocepacia (bacteria) Burkholderia cenocepacia (bacteria) | ||||||
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  SYNCHROTRON / SYNCHROTRON /  SAD / Resolution: 1.4 Å SAD / Resolution: 1.4 Å | ||||||
 Authors Authors | Seattle Structural Genomics Center for Infectious Disease (SSGCID) | ||||||
 Citation Citation |  Journal: to be published Journal: to be publishedTitle: Crystal structure of a Short chain dehydrogenase from Burkholderia cenocepacia J2315 in complex with NADP Authors: Abendroth, J. / Dranow, D.M. / Lorimer, D.D. / Edwards, T.E. | ||||||
| History |
|
- Structure visualization
Structure visualization
| Structure viewer | Molecule:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- Downloads & links
Downloads & links
- Download
Download
| PDBx/mmCIF format |  5u4s.cif.gz 5u4s.cif.gz | 197.1 KB | Display |  PDBx/mmCIF format PDBx/mmCIF format |
|---|---|---|---|---|
| PDB format |  pdb5u4s.ent.gz pdb5u4s.ent.gz | 157.4 KB | Display |  PDB format PDB format |
| PDBx/mmJSON format |  5u4s.json.gz 5u4s.json.gz | Tree view |  PDBx/mmJSON format PDBx/mmJSON format | |
| Others |  Other downloads Other downloads |
-Validation report
| Arichive directory |  https://data.pdbj.org/pub/pdb/validation_reports/u4/5u4s https://data.pdbj.org/pub/pdb/validation_reports/u4/5u4s ftp://data.pdbj.org/pub/pdb/validation_reports/u4/5u4s ftp://data.pdbj.org/pub/pdb/validation_reports/u4/5u4s | HTTPS FTP |
|---|
-Related structure data
- Links
Links
- Assembly
Assembly
| Deposited unit | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||
| Unit cell |
|
- Components
Components
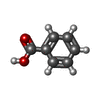
| #1: Protein | Mass: 26023.188 Da / Num. of mol.: 2 Source method: isolated from a genetically manipulated source Source: (gene. exp.)   Burkholderia cenocepacia (strain ATCC BAA-245 / DSM 16553 / LMG 16656 / NCTC 13227 / J2315 / CF5610) (bacteria) Burkholderia cenocepacia (strain ATCC BAA-245 / DSM 16553 / LMG 16656 / NCTC 13227 / J2315 / CF5610) (bacteria)Strain: ATCC BAA-245 / DSM 16553 / LMG 16656 / NCTC 13227 / J2315 / CF5610 Gene: BCAM2128 / Plasmid: BuceA.00010.y.B1 / Production host:   Escherichia coli (E. coli) / Strain (production host): BL21(DE3) / References: UniProt: B4EFS5 Escherichia coli (E. coli) / Strain (production host): BL21(DE3) / References: UniProt: B4EFS5#2: Chemical |  Nicotinamide adenine dinucleotide phosphate Nicotinamide adenine dinucleotide phosphate#3: Chemical |  Benzoic acid Benzoic acid#4: Chemical | ChemComp-PO4 / |  Phosphate Phosphate#5: Water | ChemComp-HOH / |  Water Water |
|---|
-Experimental details
-Experiment
| Experiment | Method:  X-RAY DIFFRACTION / Number of used crystals: 1 X-RAY DIFFRACTION / Number of used crystals: 1 |
|---|
- Sample preparation
Sample preparation
| Crystal | Density Matthews: 2.09 Å3/Da / Density % sol: 41.1 % |
|---|---|
Crystal grow | Temperature: 290 K / Method: vapor diffusion, sitting drop Details: RigakuReagents JCSG+ screen C6: 40% PEG 300, 100mM Sodium phosphate dibasic / citric acid pH 4.20: BuceA.00010.g.B1.PS01748 at 23.45mg/ml + 5mM NADP: cryo: direct: tray 285429c6, puck izz8-4. ...Details: RigakuReagents JCSG+ screen C6: 40% PEG 300, 100mM Sodium phosphate dibasic / citric acid pH 4.20: BuceA.00010.g.B1.PS01748 at 23.45mg/ml + 5mM NADP: cryo: direct: tray 285429c6, puck izz8-4. For phasing a crystal from the same condition was incubated in reservoir with 10% 5M NaI in EG, with a final concentrations of 10% EG and 500mM NaI, for 30sec and flash frozen. Phasing data were collected at CuKa |
-Data collection
| Diffraction |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Diffraction source |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Detector |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radiation |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radiation wavelength |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection | Resolution: 1.4→50 Å / Num. obs: 86241 / % possible obs: 99.5 % / Observed criterion σ(I): -3 / Redundancy: 5.734 % / Biso Wilson estimate: 12.61 Å2 / CC1/2: 0.998 / Rmerge(I) obs: 0.072 / Net I/σ(I): 13.91 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection shell |
|
- Processing
Processing
| Software |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Refinement | Method to determine structure : :  SAD / Resolution: 1.4→50 Å / SU ML: 0.12 / Cross valid method: FREE R-VALUE / σ(F): 1.35 / Phase error: 15.82 SAD / Resolution: 1.4→50 Å / SU ML: 0.12 / Cross valid method: FREE R-VALUE / σ(F): 1.35 / Phase error: 15.82
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solvent computation | Shrinkage radii: 0.9 Å / VDW probe radii: 1.11 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Displacement parameters | Biso max: 88.9 Å2 / Biso mean: 19.6795 Å2 / Biso min: 6.73 Å2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement step | Cycle: final / Resolution: 1.4→50 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS refinement shell | Refine-ID: X-RAY DIFFRACTION / Rfactor Rfree error: 0
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS params. | Method: refined / Refine-ID: X-RAY DIFFRACTION
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS group |
|
 Movie
Movie Controller
Controller













 PDBj
PDBj