+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 2zyk | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
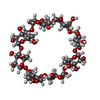
| タイトル | Crystal structure of cyclo/maltodextrin-binding protein complexed with gamma-cyclodextrin | ||||||||||||
 要素 要素 | Solute-binding protein | ||||||||||||
 キーワード キーワード | SUGAR BINDING PROTEIN / solute-binding protein / closed form | ||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 | ||||||||||||
| 生物種 |   Thermoactinomyces vulgaris (バクテリア) Thermoactinomyces vulgaris (バクテリア) | ||||||||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 2.5 Å 分子置換 / 解像度: 2.5 Å | ||||||||||||
 データ登録者 データ登録者 | Tonozuka, T. / Sogawa, A. / Yamada, M. / Matsumoto, N. / Yoshida, H. / Kamitori, S. / Ichikawa, K. / Mizuno, M. / Nishikawa, A. / Sakano, Y. | ||||||||||||
 引用 引用 |  ジャーナル: Febs J. / 年: 2007 ジャーナル: Febs J. / 年: 2007タイトル: Structural basis for cyclodextrin recognition by Thermoactinomyces vulgaris cyclo/maltodextrin-binding protein 著者: Tonozuka, T. / Sogawa, A. / Yamada, M. / Matsumoto, N. / Yoshida, H. / Kamitori, S. / Ichikawa, K. / Mizuno, M. / Nishikawa, A. / Sakano, Y. #1:  ジャーナル: Febs J. / 年: 2009 ジャーナル: Febs J. / 年: 2009タイトル: Crystal structures of open and closed forms of cyclo/maltodextrin-binding protein 著者: Matsumoto, M. / Yamada, M. / Kurakata, Y. / Yoshida, H. / Kamitori, S. / Nishikawa, A. / Tonozuka, T. | ||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  2zyk.cif.gz 2zyk.cif.gz | 313.7 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb2zyk.ent.gz pdb2zyk.ent.gz | 259.1 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  2zyk.json.gz 2zyk.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/zy/2zyk https://data.pdbj.org/pub/pdb/validation_reports/zy/2zyk ftp://data.pdbj.org/pub/pdb/validation_reports/zy/2zyk ftp://data.pdbj.org/pub/pdb/validation_reports/zy/2zyk | HTTPS FTP |
|---|
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||
| 2 | 
| ||||||||
| 3 | 
| ||||||||
| 4 | 
| ||||||||
| 単位格子 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 43686.863 Da / 分子数: 4 / 断片: residues 1-397 / 由来タイプ: 組換発現 由来: (組換発現)   Thermoactinomyces vulgaris (バクテリア) Thermoactinomyces vulgaris (バクテリア)株: R-47 / プラスミド: pETCBP / 発現宿主:   Escherichia coli BL21(DE3) (大腸菌) / 株 (発現宿主): BL21(DE3) / 参照: UniProt: Q9AJF5 Escherichia coli BL21(DE3) (大腸菌) / 株 (発現宿主): BL21(DE3) / 参照: UniProt: Q9AJF5#2: 多糖 | Cyclooctakis-(1-4)-(alpha-D-glucopyranose) / gamma-cyclodextrin #3: 水 | ChemComp-HOH / |  水 水 |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2 Å3/Da / 溶媒含有率: 38.49 % |
|---|---|
結晶化 | 温度: 293 K / 手法: 蒸気拡散法, ハンギングドロップ法 / pH: 6.25 詳細: 25% PEG 6000, 0.1M MES, pH 6.25, VAPOR DIFFUSION, HANGING DROP, temperature 293K |
-データ収集
| 回折 | 平均測定温度: 100 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  Photon Factory Photon Factory  / ビームライン: AR-NW12A / 波長: 1 Å / ビームライン: AR-NW12A / 波長: 1 Å |
| 検出器 | タイプ: ADSC QUANTUM 4 / 検出器: CCD / 日付: 2003年12月9日 |
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長 : 1 Å / 相対比: 1 : 1 Å / 相対比: 1 |
| 反射 | 解像度: 2.5→50 Å / Num. all: 47691 / Num. obs: 47691 / % possible obs: 100 % / 冗長度: 3.8 % / Biso Wilson estimate: 20.9 Å2 / Rmerge(I) obs: 0.069 / Net I/σ(I): 24 |
| 反射 シェル | 解像度: 2.5→2.66 Å / Rmerge(I) obs: 0.217 / Mean I/σ(I) obs: 8.6 / Num. unique all: 4735 / % possible all: 100 |
- 解析
解析
| ソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法 : :  分子置換 分子置換開始モデル: a rough model of the selenomethionine-substituted protein 解像度: 2.5→48.51 Å / Rfactor Rfree error: 0.004 / Data cutoff high absF: 3030046.79 / Data cutoff low absF: 0 / Isotropic thermal model: RESTRAINED / 交差検証法: THROUGHOUT / σ(F): 0 / 立体化学のターゲット値: Engh & Huber
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | 溶媒モデル: FLAT MODEL / Bsol: 29.0713 Å2 / ksol: 0.361716 e/Å3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 24.2 Å2
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine analyze |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 2.5→48.51 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS精密化 シェル | 解像度: 2.5→2.66 Å / Rfactor Rfree error: 0.012 / Total num. of bins used: 6
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Xplor file |
|
 ムービー
ムービー コントローラー
コントローラー













 PDBj
PDBj