+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1gse | ||||||
|---|---|---|---|---|---|---|---|
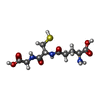
| タイトル | GLUTATHIONE TRANSFERASE A1-1 COMPLEXED WITH AN ETHACRYNIC ACID GLUTATHIONE CONJUGATE (MUTANT R15K) | ||||||
 要素 要素 | GLUTATHIONE TRANSFERASE グルタチオン-S-トランスフェラーゼ グルタチオン-S-トランスフェラーゼ | ||||||
 キーワード キーワード | TRANSFERASE (GLUTATHIONE) / A1-1 | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 異性化酵素; 分子内で酸化還元酵素として働くもの; C=C結合の転位 / glutathione derivative biosynthetic process / 異性化酵素; 分子内で酸化還元酵素として働くもの; C=C結合の転位 / glutathione derivative biosynthetic process /  steroid delta-isomerase activity / linoleic acid metabolic process / steroid delta-isomerase activity / linoleic acid metabolic process /  薬物代謝 / 薬物代謝 /  glutathione peroxidase activity / Azathioprine ADME / Heme degradation / NFE2L2 regulating anti-oxidant/detoxification enzymes / prostaglandin metabolic process ... glutathione peroxidase activity / Azathioprine ADME / Heme degradation / NFE2L2 regulating anti-oxidant/detoxification enzymes / prostaglandin metabolic process ... 異性化酵素; 分子内で酸化還元酵素として働くもの; C=C結合の転位 / glutathione derivative biosynthetic process / 異性化酵素; 分子内で酸化還元酵素として働くもの; C=C結合の転位 / glutathione derivative biosynthetic process /  steroid delta-isomerase activity / linoleic acid metabolic process / steroid delta-isomerase activity / linoleic acid metabolic process /  薬物代謝 / 薬物代謝 /  glutathione peroxidase activity / Azathioprine ADME / Heme degradation / NFE2L2 regulating anti-oxidant/detoxification enzymes / prostaglandin metabolic process / glutathione peroxidase activity / Azathioprine ADME / Heme degradation / NFE2L2 regulating anti-oxidant/detoxification enzymes / prostaglandin metabolic process /  グルタチオン-S-トランスフェラーゼ / グルタチオン-S-トランスフェラーゼ /  glutathione transferase activity / glutathione transferase activity /  酸化還元酵素; 過酸化物を電子受容体にする; ペルオキシダーゼ / glutathione metabolic process / epithelial cell differentiation / xenobiotic metabolic process / 酸化還元酵素; 過酸化物を電子受容体にする; ペルオキシダーゼ / glutathione metabolic process / epithelial cell differentiation / xenobiotic metabolic process /  fatty acid binding / extracellular exosome / fatty acid binding / extracellular exosome /  細胞質基質 細胞質基質類似検索 - 分子機能 | ||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||
| 手法 |  X線回折 / 解像度: 2 Å X線回折 / 解像度: 2 Å | ||||||
 データ登録者 データ登録者 | Cameron, A.D. / Jones, T.A. | ||||||
 引用 引用 |  ジャーナル: Structure / 年: 1995 ジャーナル: Structure / 年: 1995タイトル: Structural analysis of human alpha-class glutathione transferase A1-1 in the apo-form and in complexes with ethacrynic acid and its glutathione conjugate. 著者: Cameron, A.D. / Sinning, I. / L'Hermite, G. / Olin, B. / Board, P.G. / Mannervik, B. / Jones, T.A. #1:  ジャーナル: J.Mol.Biol. / 年: 1993 ジャーナル: J.Mol.Biol. / 年: 1993タイトル: Structure Determination and Refinement of Human Alpha Class Glutathione Transferase A1-1, and a Comparison with the Mu and Pi Class Enzyme 著者: Sinning, I. / Kleywegt, G.J. / Cowan, S.W. / Reinemer, P. / Dirr, H.W. / Huber, R. / Gilliland, G.L. / Armstrong, R.N. / Ji, X. / Board, P.G. / Olin, B. / Mannervik, B. / Jones, T.A. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1gse.cif.gz 1gse.cif.gz | 113.2 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1gse.ent.gz pdb1gse.ent.gz | 88.1 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1gse.json.gz 1gse.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/gs/1gse https://data.pdbj.org/pub/pdb/validation_reports/gs/1gse ftp://data.pdbj.org/pub/pdb/validation_reports/gs/1gse ftp://data.pdbj.org/pub/pdb/validation_reports/gs/1gse | HTTPS FTP |
|---|
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 |
| |||||||||||||||
| 単位格子 |
| |||||||||||||||
| Atom site foot note | 1: CIS PROLINE - PRO A 56 / 2: CIS PROLINE - PRO B 56 | |||||||||||||||
| Components on special symmetry positions |
| |||||||||||||||
| 非結晶学的対称性 (NCS) | NCS oper: (Code: given Matrix: (-0.60546, 0.04633, 0.79453), ベクター  : : 詳細 | MTRIX THE TRANSFORMATIONS PRESENTED ON MTRIX RECORDS BELOW DESCRIBE NON-CRYSTALLOGRAPHIC RELATIONSHIPS AMONG THE VARIOUS DOMAINS IN THIS ENTRY. APPLYING THE APPROPRIATE MTRIX TRANSFORMATION TO THE RESIDUES LISTED FIRST WILL YIELD APPROXIMATE COORDINATES FOR THE RESIDUES LISTED SECOND. APPLIED TO TRANSFORMED TO MTRIX RESIDUES RESIDUES RMSD M1 A 4 .. A 222 B 4 .. B 222 0.123 | |
- 要素
要素
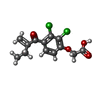
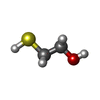
| #1: タンパク質 |  グルタチオン-S-トランスフェラーゼ グルタチオン-S-トランスフェラーゼ分子量: 25510.910 Da / 分子数: 2 / 変異: R15K / 由来タイプ: 組換発現 / 由来: (組換発現)   Homo sapiens (ヒト) / 器官: LIVER Homo sapiens (ヒト) / 器官: LIVER 肝臓 / プラスミド: PTACGST2 / 発現宿主: 肝臓 / プラスミド: PTACGST2 / 発現宿主:   Escherichia coli (大腸菌) / 株 (発現宿主): JM103 Escherichia coli (大腸菌) / 株 (発現宿主): JM103参照: UniProt: P08263,  グルタチオン-S-トランスフェラーゼ グルタチオン-S-トランスフェラーゼ#2: 化合物 |  グルタチオン グルタチオン#3: 化合物 |  Etacrynic acid Etacrynic acid#4: 化合物 | ChemComp-BME /  2-メルカプトエタノール 2-メルカプトエタノール#5: 水 | ChemComp-HOH / |  水 水非ポリマーの詳細 | THE ETHACRYNIC ACID MOIETY OF THE LIGAND HAS BEEN MODELLED IN TWO ALTERNATE CONFORMATIONS. TO ...THE ETHACRYNIC | |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 X線回折 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2.41 Å3/Da / 溶媒含有率: 48.99 % | ||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
結晶化 | *PLUS 温度: 20 ℃ / 手法: 蒸気拡散法 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶液の組成 | *PLUS
|
-データ収集
| 放射光源 | 波長: 1.54 |
|---|---|
| 検出器 | タイプ: RIGAKU RAXIS / 検出器: IMAGE PLATE / 日付: 1994年1月20日 |
| 放射 | 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長 : 1.54 Å / 相対比: 1 : 1.54 Å / 相対比: 1 |
| 反射 | 解像度: 2→15 Å / Num. obs: 30538 / % possible obs: 93.4 % / Observed criterion σ(I): 0 / 冗長度: 2.1 % / Rmerge(I) obs: 0.073 |
| 反射 | *PLUS Num. measured all: 64609 / Rmerge(I) obs: 0.073 |
- 解析
解析
| ソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 解像度: 2→7.5 Å / σ(F): 0 詳細: TWO B-MERCAPTOETHANOL RESIDUES (SEO) HAVE BEEN INSERTED INTO EACH MONOMER SUCH THAT THEY FORM A 2-HYDROXYETHYL DISULFIDE (RESIDUES 225 AND 226). IN EACH CASE ONE OF THE BME'S HAS BEEN ...詳細: TWO B-MERCAPTOETHANOL RESIDUES (SEO) HAVE BEEN INSERTED INTO EACH MONOMER SUCH THAT THEY FORM A 2-HYDROXYETHYL DISULFIDE (RESIDUES 225 AND 226). IN EACH CASE ONE OF THE BME'S HAS BEEN MODELLED IN TWO CONFORMATIONS.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 27 Å2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine analyze | Luzzati coordinate error obs: 0.25 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 2→7.5 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ソフトウェア | *PLUS 名称:  X-PLOR / 分類: refinement X-PLOR / 分類: refinement | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化 | *PLUS Rfactor Rfree : 0.244 : 0.244 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | *PLUS | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | *PLUS | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 | *PLUS
|
 ムービー
ムービー コントローラー
コントローラー















 PDBj
PDBj