+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of the Fmoc-Tau-PAM4 Type 2 amyloid fibril | |||||||||
 マップデータ マップデータ | Final postprocessed, sharpened, helical symmetrised map of the fmoc-TauPAM4 fibril form 1a | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード |  amyloid (アミロイド) / tau / helical / cross-beta / amyloid (アミロイド) / tau / helical / cross-beta /  fibril (フィブリル) / fibril (フィブリル) /  neurodegeneration (神経変性疾患) / Fmoc / PROTEIN FIBRIL neurodegeneration (神経変性疾患) / Fmoc / PROTEIN FIBRIL | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報plus-end-directed organelle transport along microtubule /  軸索輸送 / histone-dependent DNA binding / 軸索輸送 / histone-dependent DNA binding /  neurofibrillary tangle assembly / positive regulation of diacylglycerol kinase activity / negative regulation of establishment of protein localization to mitochondrion / neurofibrillary tangle assembly / positive regulation of diacylglycerol kinase activity / negative regulation of establishment of protein localization to mitochondrion /  neurofibrillary tangle / positive regulation of protein localization to synapse / microtubule lateral binding / neurofibrillary tangle / positive regulation of protein localization to synapse / microtubule lateral binding /  tubulin complex ...plus-end-directed organelle transport along microtubule / tubulin complex ...plus-end-directed organelle transport along microtubule /  軸索輸送 / histone-dependent DNA binding / 軸索輸送 / histone-dependent DNA binding /  neurofibrillary tangle assembly / positive regulation of diacylglycerol kinase activity / negative regulation of establishment of protein localization to mitochondrion / neurofibrillary tangle assembly / positive regulation of diacylglycerol kinase activity / negative regulation of establishment of protein localization to mitochondrion /  neurofibrillary tangle / positive regulation of protein localization to synapse / microtubule lateral binding / neurofibrillary tangle / positive regulation of protein localization to synapse / microtubule lateral binding /  tubulin complex / tubulin complex /  phosphatidylinositol bisphosphate binding / main axon / regulation of long-term synaptic depression / negative regulation of kinase activity / negative regulation of tubulin deacetylation / generation of neurons / regulation of chromosome organization / positive regulation of protein localization / rRNA metabolic process / internal protein amino acid acetylation / phosphatidylinositol bisphosphate binding / main axon / regulation of long-term synaptic depression / negative regulation of kinase activity / negative regulation of tubulin deacetylation / generation of neurons / regulation of chromosome organization / positive regulation of protein localization / rRNA metabolic process / internal protein amino acid acetylation /  regulation of mitochondrial fission / intracellular distribution of mitochondria / axonal transport of mitochondrion / axon development / regulation of mitochondrial fission / intracellular distribution of mitochondria / axonal transport of mitochondrion / axon development /  central nervous system neuron development / central nervous system neuron development /  regulation of microtubule polymerization / regulation of microtubule polymerization /  微小管 / minor groove of adenine-thymine-rich DNA binding / 微小管 / minor groove of adenine-thymine-rich DNA binding /  lipoprotein particle binding / lipoprotein particle binding /  dynactin binding / glial cell projection / negative regulation of mitochondrial membrane potential / dynactin binding / glial cell projection / negative regulation of mitochondrial membrane potential /  apolipoprotein binding / protein polymerization / negative regulation of mitochondrial fission / apolipoprotein binding / protein polymerization / negative regulation of mitochondrial fission /  axolemma / Caspase-mediated cleavage of cytoskeletal proteins / regulation of microtubule polymerization or depolymerization / positive regulation of axon extension / Activation of AMPK downstream of NMDARs / regulation of microtubule cytoskeleton organization / supramolecular fiber organization / axolemma / Caspase-mediated cleavage of cytoskeletal proteins / regulation of microtubule polymerization or depolymerization / positive regulation of axon extension / Activation of AMPK downstream of NMDARs / regulation of microtubule cytoskeleton organization / supramolecular fiber organization /  stress granule assembly / regulation of cellular response to heat / cytoplasmic microtubule organization / regulation of calcium-mediated signaling / positive regulation of microtubule polymerization / axon cytoplasm / somatodendritic compartment / cellular response to brain-derived neurotrophic factor stimulus / stress granule assembly / regulation of cellular response to heat / cytoplasmic microtubule organization / regulation of calcium-mediated signaling / positive regulation of microtubule polymerization / axon cytoplasm / somatodendritic compartment / cellular response to brain-derived neurotrophic factor stimulus /  synapse assembly / synapse assembly /  phosphatidylinositol binding / nuclear periphery / cellular response to nerve growth factor stimulus / positive regulation of superoxide anion generation / protein phosphatase 2A binding / phosphatidylinositol binding / nuclear periphery / cellular response to nerve growth factor stimulus / positive regulation of superoxide anion generation / protein phosphatase 2A binding /  regulation of autophagy / astrocyte activation / response to lead ion / synapse organization / microglial cell activation / regulation of autophagy / astrocyte activation / response to lead ion / synapse organization / microglial cell activation /  Hsp90 protein binding / Hsp90 protein binding /  regulation of synaptic plasticity / PKR-mediated signaling / protein homooligomerization / regulation of synaptic plasticity / PKR-mediated signaling / protein homooligomerization /  記憶 / cellular response to reactive oxygen species / microtubule cytoskeleton organization / 記憶 / cellular response to reactive oxygen species / microtubule cytoskeleton organization /  SH3 domain binding / cytoplasmic ribonucleoprotein granule / activation of cysteine-type endopeptidase activity involved in apoptotic process / neuron projection development / microtubule cytoskeleton / cell-cell signaling / protein-macromolecule adaptor activity / cellular response to heat / SH3 domain binding / cytoplasmic ribonucleoprotein granule / activation of cysteine-type endopeptidase activity involved in apoptotic process / neuron projection development / microtubule cytoskeleton / cell-cell signaling / protein-macromolecule adaptor activity / cellular response to heat /  actin binding / actin binding /  single-stranded DNA binding / single-stranded DNA binding /  cell body / protein-folding chaperone binding / cell body / protein-folding chaperone binding /  成長円錐 / 成長円錐 /  microtubule binding / microtubule binding /  double-stranded DNA binding / double-stranded DNA binding /  微小管 / sequence-specific DNA binding / amyloid fibril formation / 微小管 / sequence-specific DNA binding / amyloid fibril formation /  樹状突起スパイン / learning or memory / nuclear speck / neuron projection / 樹状突起スパイン / learning or memory / nuclear speck / neuron projection /  脂質ラフト / 脂質ラフト /  神経繊維 / negative regulation of gene expression / neuronal cell body / DNA damage response / 神経繊維 / negative regulation of gene expression / neuronal cell body / DNA damage response /  樹状突起 / 樹状突起 /  protein kinase binding / protein kinase binding /  enzyme binding / enzyme binding /  ミトコンドリア / ミトコンドリア /  DNA binding DNA binding類似検索 - 分子機能 | |||||||||
| 生物種 | synthetic construct (人工物) | |||||||||
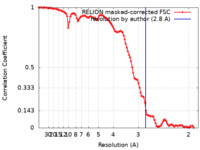
| 手法 | らせん対称体再構成法 /  クライオ電子顕微鏡法 / 解像度: 2.8 Å クライオ電子顕微鏡法 / 解像度: 2.8 Å | |||||||||
 データ登録者 データ登録者 | Wilkinson M / Louros N / Tsaka G / Ramakers M / Morelli C / Garcia T / Gallardo RU / D'Haeyer S / Goossens V / Audenaert D ...Wilkinson M / Louros N / Tsaka G / Ramakers M / Morelli C / Garcia T / Gallardo RU / D'Haeyer S / Goossens V / Audenaert D / Thal DR / Ranson NA / Radford SE / Rousseau F / Schymkowitz J | |||||||||
| 資金援助 |  ベルギー, 1件 ベルギー, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2024 ジャーナル: Nat Commun / 年: 2024タイトル: Local structural preferences in shaping tau amyloid polymorphism. 著者: Nikolaos Louros / Martin Wilkinson / Grigoria Tsaka / Meine Ramakers / Chiara Morelli / Teresa Garcia / Rodrigo Gallardo / Sam D'Haeyer / Vera Goossens / Dominique Audenaert / Dietmar Rudolf ...著者: Nikolaos Louros / Martin Wilkinson / Grigoria Tsaka / Meine Ramakers / Chiara Morelli / Teresa Garcia / Rodrigo Gallardo / Sam D'Haeyer / Vera Goossens / Dominique Audenaert / Dietmar Rudolf Thal / Ian R Mackenzie / Rosa Rademakers / Neil A Ranson / Sheena E Radford / Frederic Rousseau / Joost Schymkowitz /    要旨: Tauopathies encompass a group of neurodegenerative disorders characterised by diverse tau amyloid fibril structures. The persistence of polymorphism across tauopathies suggests that distinct ...Tauopathies encompass a group of neurodegenerative disorders characterised by diverse tau amyloid fibril structures. The persistence of polymorphism across tauopathies suggests that distinct pathological conditions dictate the adopted polymorph for each disease. However, the extent to which intrinsic structural tendencies of tau amyloid cores contribute to fibril polymorphism remains uncertain. Using a combination of experimental approaches, we here identify a new amyloidogenic motif, PAM4 (Polymorphic Amyloid Motif of Repeat 4), as a significant contributor to tau polymorphism. Calculation of per-residue contributions to the stability of the fibril cores of different pathologic tau structures suggests that PAM4 plays a central role in preserving structural integrity across amyloid polymorphs. Consistent with this, cryo-EM structural analysis of fibrils formed from a synthetic PAM4 peptide shows that the sequence adopts alternative structures that closely correspond to distinct disease-associated tau strains. Furthermore, in-cell experiments revealed that PAM4 deletion hampers the cellular seeding efficiency of tau aggregates extracted from Alzheimer's disease, corticobasal degeneration, and progressive supranuclear palsy patients, underscoring PAM4's pivotal role in these tauopathies. Together, our results highlight the importance of the intrinsic structural propensity of amyloid core segments to determine the structure of tau in cells, and in propagating amyloid structures in disease. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_16881.map.gz emd_16881.map.gz | 16.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-16881-v30.xml emd-16881-v30.xml emd-16881.xml emd-16881.xml | 18.6 KB 18.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_16881_fsc.xml emd_16881_fsc.xml | 10.6 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_16881.png emd_16881.png | 77.1 KB | ||
| Filedesc metadata |  emd-16881.cif.gz emd-16881.cif.gz | 5.9 KB | ||
| その他 |  emd_16881_half_map_1.map.gz emd_16881_half_map_1.map.gz emd_16881_half_map_2.map.gz emd_16881_half_map_2.map.gz | 81 MB 80.8 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-16881 http://ftp.pdbj.org/pub/emdb/structures/EMD-16881 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-16881 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-16881 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_16881.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_16881.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Final postprocessed, sharpened, helical symmetrised map of the fmoc-TauPAM4 fibril form 1a | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.94 Å | ||||||||||||||||||||
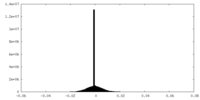
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: halfmap2
| ファイル | emd_16881_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | halfmap2 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
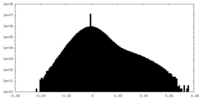
| 密度ヒストグラム |
-ハーフマップ: halfmap1
| ファイル | emd_16881_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | halfmap1 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
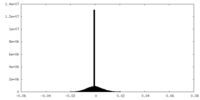
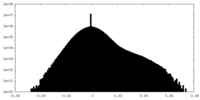
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Amyloid fibril form 1a of Tau-PAM4 peptide adducted with the Fmoc...
| 全体 | 名称: Amyloid fibril form 1a of Tau-PAM4 peptide adducted with the Fmoc protection group |
|---|---|
| 要素 |
|
-超分子 #1: Amyloid fibril form 1a of Tau-PAM4 peptide adducted with the Fmoc...
| 超分子 | 名称: Amyloid fibril form 1a of Tau-PAM4 peptide adducted with the Fmoc protection group タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all / 詳細: Synthesised peptide assembled into amyloid fibril |
|---|---|
| 由来(天然) | 生物種: synthetic construct (人工物) |
-分子 #1: Microtubule-associated protein tau
| 分子 | 名称: Microtubule-associated protein tau / タイプ: protein_or_peptide / ID: 1 詳細: 13-residue peptide of the PAM4 motif of Tau, corresponding to residues 350-362 of the Tau repeat domain. The peptide is supposed to be N-terminally acetylated but 10% (by mass spec) was still ...詳細: 13-residue peptide of the PAM4 motif of Tau, corresponding to residues 350-362 of the Tau repeat domain. The peptide is supposed to be N-terminally acetylated but 10% (by mass spec) was still adducted to the Fmoc protection group from synthesis. The peptide in the fibrils is dominated by this impurity. The peptide is also C-terminally amidated. コピー数: 18 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種: synthetic construct (人工物) |
| 分子量 | 理論値: 1.652269 KDa |
| 配列 | 文字列: (VP1)VQSKIGSLD NIT(HIA) UniProtKB:  タウタンパク質 タウタンパク質 |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | らせん対称体再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 濃度 | 0.6 mg/mL |
|---|---|
| 緩衝液 | pH: 7 詳細: Peptide resuspended in MilliQ water for aggregation reaction |
| グリッド | モデル: EMS Lacey Carbon / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: LACEY / 前処理 - タイプ: PLASMA CLEANING / 前処理 - 時間: 60 sec. |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 90 % / チャンバー内温度: 279 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.4 µm / 最小 デフォーカス(公称値): 1.2 µm / 倍率(公称値): 130000 Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.4 µm / 最小 デフォーカス(公称値): 1.2 µm / 倍率(公称値): 130000 |
| 特殊光学系 | エネルギーフィルター - 名称: TFS Selectris / エネルギーフィルター - スリット幅: 10 eV |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 撮影 | フィルム・検出器のモデル: FEI FALCON IV (4k x 4k) デジタル化 - サイズ - 横: 4096 pixel / デジタル化 - サイズ - 縦: 4096 pixel / 撮影したグリッド数: 1 / 実像数: 1957 / 平均露光時間: 5.0 sec. / 平均電子線量: 32.0 e/Å2 詳細: Movies were collected as 1204 EER frames compressed and re-grouped into 35 TIF fractions |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
-原子モデル構築 1
| 詳細 | Initial model built manually in coot, no starting template |
|---|---|
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL / 温度因子: 48 当てはまり具合の基準: Cross-correlation coefficient |
| 得られたモデル |  PDB-8ohi: |
 ムービー
ムービー コントローラー
コントローラー














 Z
Z Y
Y X
X