+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 6scj | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
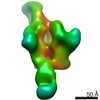
| タイトル | The structure of human thyroglobulin | |||||||||
 要素 要素 | Thyroglobulin チログロブリン チログロブリン | |||||||||
 キーワード キーワード |  HORMONE (ホルモン) / HORMONE (ホルモン) /  Thyroglobulin (チログロブリン) / Thyroglobulin (チログロブリン) /  Thyroid (甲状腺) / Thyroid (甲状腺) /  thyroid hormones (甲状腺ホルモン) / Tri-iodo-thyronine / thyroid hormones (甲状腺ホルモン) / Tri-iodo-thyronine /  Thyroxine (甲状腺ホルモン) Thyroxine (甲状腺ホルモン) | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報hormone biosynthetic process / iodide transport / thyroid hormone generation /  regulation of myelination / thyroid gland development / regulation of myelination / thyroid gland development /  hormone activity / hormone activity /  シグナル伝達 / シグナル伝達 /  extracellular space / extracellular region / identical protein binding extracellular space / extracellular region / identical protein binding類似検索 - 分子機能 | |||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 |  電子顕微鏡法 / 電子顕微鏡法 /  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.6 Å クライオ電子顕微鏡法 / 解像度: 3.6 Å | |||||||||
 データ登録者 データ登録者 | Coscia, F. / Turk, D. / Lowe, J. | |||||||||
| 資金援助 |  英国, 2件 英国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2020 ジャーナル: Nature / 年: 2020タイトル: The structure of human thyroglobulin. 著者: Francesca Coscia / Ajda Taler-Verčič / Veronica T Chang / Ludwig Sinn / Francis J O'Reilly / Thierry Izoré / Miha Renko / Imre Berger / Juri Rappsilber / Dušan Turk / Jan Löwe /    要旨: Thyroglobulin (TG) is the protein precursor of thyroid hormones, which are essential for growth, development and the control of metabolism in vertebrates. Hormone synthesis from TG occurs in the ...Thyroglobulin (TG) is the protein precursor of thyroid hormones, which are essential for growth, development and the control of metabolism in vertebrates. Hormone synthesis from TG occurs in the thyroid gland via the iodination and coupling of pairs of tyrosines, and is completed by TG proteolysis. Tyrosine proximity within TG is thought to enable the coupling reaction but hormonogenic tyrosines have not been clearly identified, and the lack of a three-dimensional structure of TG has prevented mechanistic understanding. Here we present the structure of full-length human thyroglobulin at a resolution of approximately 3.5 Å, determined by cryo-electron microscopy. We identified all of the hormonogenic tyrosine pairs in the structure, and verified them using site-directed mutagenesis and in vitro hormone-production assays using human TG expressed in HEK293T cells. Our analysis revealed that the proximity, flexibility and solvent exposure of the tyrosines are the key characteristics of hormonogenic sites. We transferred the reaction sites from TG to an engineered tyrosine donor-acceptor pair in the unrelated bacterial maltose-binding protein (MBP), which yielded hormone production with an efficiency comparable to that of TG. Our study provides a framework to further understand the production and regulation of thyroid hormones. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  6scj.cif.gz 6scj.cif.gz | 871.2 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb6scj.ent.gz pdb6scj.ent.gz | 719.5 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  6scj.json.gz 6scj.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/sc/6scj https://data.pdbj.org/pub/pdb/validation_reports/sc/6scj ftp://data.pdbj.org/pub/pdb/validation_reports/sc/6scj ftp://data.pdbj.org/pub/pdb/validation_reports/sc/6scj | HTTPS FTP |
|---|
-関連構造データ
| 関連構造データ |  10141MC M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | |
| 電子顕微鏡画像生データ |  EMPIAR-10666 (タイトル: Human thyroglobulin / Data size: 1.7 TB EMPIAR-10666 (タイトル: Human thyroglobulin / Data size: 1.7 TBData #1: un-aligned frames for endogenous human thyroglobulin (eTG) on graphene oxide grids (Krios 300 kV, K2 camera) [micrographs - multiframe] Data #2: un-aligned frames for recombinant human thyroglobulin produced in HEK cells (rTG) on graphene oxide grids (Krios 300 kV, K2 camera) [micrographs - multiframe]) |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 |  チログロブリン / Tg チログロブリン / Tg分子量: 305069.844 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)   Homo sapiens (ヒト) / 遺伝子: TG / 細胞株 (発現宿主): HEK / 発現宿主: Homo sapiens (ヒト) / 遺伝子: TG / 細胞株 (発現宿主): HEK / 発現宿主:   Homo sapiens (ヒト) / Variant (発現宿主): 293T / 参照: UniProt: P01266 Homo sapiens (ヒト) / Variant (発現宿主): 293T / 参照: UniProt: P01266#2: 多糖 |  オリゴ糖 / 分子量: 586.542 Da / 分子数: 2 / 由来タイプ: 組換発現 オリゴ糖 / 分子量: 586.542 Da / 分子数: 2 / 由来タイプ: 組換発現#3: 糖 | ChemComp-NAG /  N-アセチルグルコサミン N-アセチルグルコサミン研究の焦点であるリガンドがあるか | Y | |
|---|
-実験情報
-実験
| 実験 | 手法:  電子顕微鏡法 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法:  単粒子再構成法 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: human thyroglobulin チログロブリン / タイプ: COMPLEX / 詳細: dimeric / Entity ID: #1 / 由来: RECOMBINANT チログロブリン / タイプ: COMPLEX / 詳細: dimeric / Entity ID: #1 / 由来: RECOMBINANT |
|---|---|
| 分子量 | 値: 0.660 MDa / 実験値: YES |
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 由来(組換発現) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 緩衝液 | pH: 8 / 詳細: TRIS 0.05M, 0.2M NaCl pH 8 |
| 試料 | 濃度: 0.05 mg/ml / 包埋: NO / シャドウイング: NO / 染色 : NO / 凍結 : NO / 凍結 : YES : YES |
急速凍結 | 装置: FEI VITROBOT MARK III / 凍結剤: ETHANE |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源 : :  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD Bright-field microscopy Bright-field microscopy |
| 撮影 | 電子線照射量: 40 e/Å2 / 検出モード: COUNTING フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) |
- 解析
解析
| ソフトウェア | 名称: PHENIX / バージョン: (1.14rc2_3191: phenix.real_space_refine) / 分類: 精密化 |
|---|---|
CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION |
| 対称性 | 点対称性 : C2 (2回回転対称 : C2 (2回回転対称 ) ) |
3次元再構成 | 解像度: 3.6 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 151601 / 対称性のタイプ: POINT |
 ムービー
ムービー コントローラー
コントローラー










 PDBj
PDBj


