+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 6nut | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
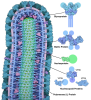
| タイトル | Ebola virus nucleoprotein - RNA complex | |||||||||
 要素 要素 |
| |||||||||
 キーワード キーワード |  VIRAL PROTEIN/RNA (ウイルス性) / RNA-binding / VIRAL PROTEIN/RNA (ウイルス性) / RNA-binding /  nucleoprotein (核タンパク質) / nucleoprotein (核タンパク質) /  nucleocapsid (カプシド) / nucleocapsid (カプシド) /  capsid (カプシド) / capsid (カプシド) /  VIRAL PROTEIN-RNA complex (ウイルス性) VIRAL PROTEIN-RNA complex (ウイルス性) | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報viral RNA genome packaging / helical viral capsid / viral nucleocapsid / host cell cytoplasm /  ribonucleoprotein complex / ribonucleoprotein complex /  RNA binding RNA binding類似検索 - 分子機能 | |||||||||
| 生物種 |   Zaire ebolavirus (エボラウイルス) Zaire ebolavirus (エボラウイルス)  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 |  電子顕微鏡法 / らせん対称体再構成法 / 電子顕微鏡法 / らせん対称体再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.1 Å クライオ電子顕微鏡法 / 解像度: 3.1 Å | |||||||||
 データ登録者 データ登録者 | Kirchdoerfer, R.N. / Ward, A.B. | |||||||||
| 資金援助 |  米国, 2件 米国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Acta Crystallogr F Struct Biol Commun / 年: 2019 ジャーナル: Acta Crystallogr F Struct Biol Commun / 年: 2019タイトル: Cryo-EM structure of the Ebola virus nucleoprotein-RNA complex. 著者: Robert N Kirchdoerfer / Erica Ollmann Saphire / Andrew B Ward /  要旨: Ebola virus is an emerging virus that is capable of causing a deadly disease in humans. Replication, transcription and packaging of the viral genome are carried out by the viral nucleocapsid. The ...Ebola virus is an emerging virus that is capable of causing a deadly disease in humans. Replication, transcription and packaging of the viral genome are carried out by the viral nucleocapsid. The nucleocapsid is a complex of the viral nucleoprotein, RNA and several other viral proteins. The nucleoprotein forms large, RNA-bound, helical filaments and acts as a scaffold for additional viral proteins. The 3.1 Å resolution single-particle cryo-electron microscopy structure of the nucleoprotein-RNA helical filament presented here resembles previous structures determined at lower resolution, while providing improved molecular details of protein-protein and protein-RNA interactions. The higher resolution of the structure presented here will facilitate the design and characterization of novel and specific Ebola virus therapeutics targeting the nucleocapsid. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  6nut.cif.gz 6nut.cif.gz | 92.8 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb6nut.ent.gz pdb6nut.ent.gz | 68.1 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  6nut.json.gz 6nut.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/nu/6nut https://data.pdbj.org/pub/pdb/validation_reports/nu/6nut ftp://data.pdbj.org/pub/pdb/validation_reports/nu/6nut ftp://data.pdbj.org/pub/pdb/validation_reports/nu/6nut | HTTPS FTP |
|---|
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 | x 50
|
| 2 |
|
| 対称性 | らせん対称: (回転対称性: 1 / Dyad axis: no / N subunits divisor: 1 / Num. of operations: 50 / Rise per n subunits: 2.84 Å / Rotation per n subunits: -14.71 °) |
- 要素
要素
| #1: タンパク質 |  核タンパク質 / Ebola NP / eNP / Nucleocapsid protein / Protein N 核タンパク質 / Ebola NP / eNP / Nucleocapsid protein / Protein N分子量: 50267.098 Da / 分子数: 1 / 由来タイプ: 組換発現 由来: (組換発現)   Zaire ebolavirus (strain Mayinga-76) (エボラウイルス) Zaire ebolavirus (strain Mayinga-76) (エボラウイルス)株: Mayinga-76 / 遺伝子: NP / プラスミド: pDisplay / 細胞株 (発現宿主): 293F / 発現宿主:   Homo sapiens (ヒト) / 参照: UniProt: P18272 Homo sapiens (ヒト) / 参照: UniProt: P18272 |
|---|---|
| #2: RNA鎖 | 分子量: 1930.277 Da / 分子数: 1 / 由来タイプ: 天然 詳細: The poly-adenosine sequence was modeled to represent the mixed identity of nucleotide sequences bound to nucleoprotein. 由来: (天然)   Homo sapiens (ヒト) / 細胞株: 293F Homo sapiens (ヒト) / 細胞株: 293F |
-実験情報
-実験
| 実験 | 手法:  電子顕微鏡法 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: FILAMENT / 3次元再構成法: らせん対称体再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: Ebola virus nucleoprotein bound to RNA / タイプ: COMPLEX / Entity ID: all / 由来: RECOMBINANT | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 分子量 | 値: 177 kDa/nm / 実験値: NO | |||||||||||||||||||||||||
| 由来(天然) | 生物種:   Ebola virus - Mayinga, Zaire, 1976 (エボラウイルス) Ebola virus - Mayinga, Zaire, 1976 (エボラウイルス) | |||||||||||||||||||||||||
| 由来(組換発現) | 生物種:   Homo sapiens (ヒト) / 細胞: 293F Homo sapiens (ヒト) / 細胞: 293F | |||||||||||||||||||||||||
| 緩衝液 | pH: 7.4 | |||||||||||||||||||||||||
| 緩衝液成分 |
| |||||||||||||||||||||||||
| 試料 | 濃度: 3.8 mg/ml / 包埋: NO / シャドウイング: NO / 染色 : NO / 凍結 : NO / 凍結 : YES : YES | |||||||||||||||||||||||||
| 試料支持 | グリッドの材料: GOLD / グリッドのサイズ: 300 divisions/in. / グリッドのタイプ: Quantifoil, UltrAuFoil, R1.2/1.3 | |||||||||||||||||||||||||
急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE / 湿度: 100 % / 凍結前の試料温度: 277 K |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TALOS ARCTICA |
| 電子銃 | 電子線源 : :  FIELD EMISSION GUN / 加速電圧: 200 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 200 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD Bright-field microscopy / 倍率(補正後): 47478 X / Calibrated defocus min: 600 nm / 最大 デフォーカス(補正後): 2000 nm / Cs Bright-field microscopy / 倍率(補正後): 47478 X / Calibrated defocus min: 600 nm / 最大 デフォーカス(補正後): 2000 nm / Cs : 2.7 mm / C2レンズ絞り径: 70 µm : 2.7 mm / C2レンズ絞り径: 70 µm |
| 試料ホルダ | 凍結剤: NITROGEN 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 撮影 | 平均露光時間: 13 sec. / 電子線照射量: 49.7 e/Å2 / 検出モード: COUNTING フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 撮影したグリッド数: 1 / 実像数: 731 |
| 画像スキャン | 横: 3838 / 縦: 3710 / 動画フレーム数/画像: 65 / 利用したフレーム数/画像: 1-65 |
- 解析
解析
| EMソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
CTF補正 | タイプ: NONE | ||||||||||||||||||||||||||||||||||||||||
| らせん対称 | 回転角度/サブユニット: -14.71 ° / 軸方向距離/サブユニット: 2.84 Å / らせん対称軸の対称性: C1 | ||||||||||||||||||||||||||||||||||||||||
| 粒子像の選択 | 選択した粒子像数: 24608 | ||||||||||||||||||||||||||||||||||||||||
3次元再構成 | 解像度: 3.1 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 24609 / クラス平均像の数: 1 / 対称性のタイプ: HELICAL | ||||||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | 空間: REAL | ||||||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | 3D fitting-ID: 1 / PDB chain-ID: A / Source name: PDB / タイプ: experimental model
|
 ムービー
ムービー コントローラー
コントローラー








 PDBj
PDBj