+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1t36 | ||||||
|---|---|---|---|---|---|---|---|
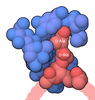
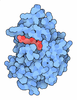
| タイトル | Crystal structure of E. coli carbamoyl phosphate synthetase small subunit mutant C248D complexed with uridine 5'-monophosphate | ||||||
 要素 要素 | (Carbamoyl-phosphate synthase ...) x 2 | ||||||
 キーワード キーワード |  LIGASE (リガーゼ) / channeling / LIGASE (リガーゼ) / channeling /  pyrimidine biosynthesis / arginine biosynthesis pyrimidine biosynthesis / arginine biosynthesis | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報carbamoyl-phosphate synthase complex /  carbamoyl-phosphate synthase (glutamine-hydrolysing) / carbamoyl-phosphate synthase (glutamine-hydrolysing) /  carbamoyl-phosphate synthase (ammonia) / carbamoyl-phosphate synthase (ammonia) /  carbamoyl-phosphate synthase (ammonia) activity / carbamoyl-phosphate synthase (ammonia) activity /  carbamoyl-phosphate synthase (glutamine-hydrolyzing) activity / pyrimidine nucleobase biosynthetic process / arginine biosynthetic process / carbamoyl-phosphate synthase (glutamine-hydrolyzing) activity / pyrimidine nucleobase biosynthetic process / arginine biosynthetic process /  glutaminase activity / : / glutaminase activity / : /  amino acid binding ...carbamoyl-phosphate synthase complex / amino acid binding ...carbamoyl-phosphate synthase complex /  carbamoyl-phosphate synthase (glutamine-hydrolysing) / carbamoyl-phosphate synthase (glutamine-hydrolysing) /  carbamoyl-phosphate synthase (ammonia) / carbamoyl-phosphate synthase (ammonia) /  carbamoyl-phosphate synthase (ammonia) activity / carbamoyl-phosphate synthase (ammonia) activity /  carbamoyl-phosphate synthase (glutamine-hydrolyzing) activity / pyrimidine nucleobase biosynthetic process / arginine biosynthetic process / carbamoyl-phosphate synthase (glutamine-hydrolyzing) activity / pyrimidine nucleobase biosynthetic process / arginine biosynthetic process /  glutaminase activity / : / glutaminase activity / : /  amino acid binding / glutamine metabolic process / amino acid biosynthetic process / 'de novo' UMP biosynthetic process / 'de novo' pyrimidine nucleobase biosynthetic process / protein heterodimerization activity / amino acid binding / glutamine metabolic process / amino acid biosynthetic process / 'de novo' UMP biosynthetic process / 'de novo' pyrimidine nucleobase biosynthetic process / protein heterodimerization activity /  nucleotide binding / nucleotide binding /  ATP binding / ATP binding /  metal ion binding / metal ion binding /  細胞質基質 / 細胞質基質 /  細胞質 細胞質類似検索 - 分子機能 | ||||||
| 生物種 |   Escherichia coli (大腸菌) Escherichia coli (大腸菌) | ||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  フーリエ合成 / 解像度: 2.1 Å フーリエ合成 / 解像度: 2.1 Å | ||||||
 データ登録者 データ登録者 | Thoden, J.B. / Huang, X. / Raushel, F.M. / Holden, H.M. | ||||||
 引用 引用 |  ジャーナル: Protein Sci. / 年: 2004 ジャーナル: Protein Sci. / 年: 2004タイトル: Long-range allosteric transitions in carbamoyl phosphate synthetase. 著者: Thoden, J.B. / Huang, X. / Kim, J. / Raushel, F.M. / Holden, H.M. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1t36.cif.gz 1t36.cif.gz | 1.2 MB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1t36.ent.gz pdb1t36.ent.gz | 977.4 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1t36.json.gz 1t36.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/t3/1t36 https://data.pdbj.org/pub/pdb/validation_reports/t3/1t36 ftp://data.pdbj.org/pub/pdb/validation_reports/t3/1t36 ftp://data.pdbj.org/pub/pdb/validation_reports/t3/1t36 | HTTPS FTP |
|---|
-関連構造データ
| 関連構造データ |  1jdbS S: 精密化の開始モデル |
|---|---|
| 類似構造データ |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||
| 単位格子 |
| ||||||||
| 詳細 | Hetero-octamer comprising chains A,B,C,D,E,F,G,H. THese chains, as deposited, represent the biological assebmly |
- 要素
要素
-Carbamoyl-phosphate synthase ... , 2種, 8分子 ACEGBDFH
| #1: タンパク質 | 分子量: 117981.750 Da / 分子数: 4 / 由来タイプ: 組換発現 / 由来: (組換発現)   Escherichia coli (大腸菌) / 遺伝子: CARB, PYRA, B0033 / プラスミド: pet15 / 生物種 (発現宿主): Escherichia coli / 発現宿主: Escherichia coli (大腸菌) / 遺伝子: CARB, PYRA, B0033 / プラスミド: pet15 / 生物種 (発現宿主): Escherichia coli / 発現宿主:   Escherichia coli BL21 (大腸菌) / 株 (発現宿主): BL21 Escherichia coli BL21 (大腸菌) / 株 (発現宿主): BL21参照: UniProt: P00968,  carbamoyl-phosphate synthase (glutamine-hydrolysing) carbamoyl-phosphate synthase (glutamine-hydrolysing)#2: タンパク質 | 分子量: 41493.824 Da / 分子数: 4 / Mutation: C248D / 由来タイプ: 組換発現 / 由来: (組換発現)   Escherichia coli (大腸菌) / 遺伝子: CARA, PYRA, B0032, Z0037, ECS0035 / プラスミド: pet15 / 発現宿主: Escherichia coli (大腸菌) / 遺伝子: CARA, PYRA, B0032, Z0037, ECS0035 / プラスミド: pet15 / 発現宿主:   Escherichia coli (大腸菌) Escherichia coli (大腸菌)参照: UniProt: P00907, UniProt: P0A6F1*PLUS,  carbamoyl-phosphate synthase (glutamine-hydrolysing) carbamoyl-phosphate synthase (glutamine-hydrolysing) |
|---|
-非ポリマー , 9種, 3993分子 













| #3: 化合物 | ChemComp-MN / #4: 化合物 | ChemComp-K / #5: 化合物 | ChemComp-PO4 /  リン酸塩 リン酸塩#6: 化合物 | ChemComp-CL /  塩化物 塩化物#7: 化合物 | ChemComp-ADP /  アデノシン二リン酸 アデノシン二リン酸#8: 化合物 | ChemComp-ORN /  オルニチン オルニチン#9: 化合物 | ChemComp-NET /  テトラエチルアンモニウム テトラエチルアンモニウム#10: 化合物 | ChemComp-U /  ウリジル酸 ウリジル酸#11: 水 | ChemComp-HOH / |  水 水 |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 3.2 Å3/Da / 溶媒含有率: 62 % |
|---|---|
結晶化 | 温度: 277 K / 手法: バッチ法 / pH: 7.4 詳細: PEG 8000, tetramethylammonium chloride, potassium chloride, manganese chloride, ornithine, ADP, HEPES, pH 7.4, batch, temperature 277K |
-データ収集
| 回折 | 平均測定温度: 100 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  APS APS  / ビームライン: 19-ID / 波長: 0.65 Å / ビームライン: 19-ID / 波長: 0.65 Å |
| 検出器 | タイプ: CUSTOM-MADE / 検出器: CCD / 日付: 1998年11月11日 |
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長 : 0.65 Å / 相対比: 1 : 0.65 Å / 相対比: 1 |
| 反射 | 解像度: 2.1→30 Å / Num. all: 433843 / Num. obs: 433843 / % possible obs: 90 % / Observed criterion σ(F): 0 / Observed criterion σ(I): 0 / 冗長度: 2.7 % / Rsym value: 0.048 / Net I/σ(I): 15.2 |
| 反射 シェル | 解像度: 2.1→2.18 Å / 冗長度: 2.3 % / Mean I/σ(I) obs: 3.3 / Num. unique all: 39976 / Rsym value: 0.203 / % possible all: 83 |
- 解析
解析
| ソフトウェア |
| |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法 : :  フーリエ合成 フーリエ合成開始モデル: PDB entry 1JDB 解像度: 2.1→30 Å / 交差検証法: THROUGHOUT / σ(F): 0 / 立体化学のターゲット値: Engh & Huber
| |||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 2.1→30 Å
| |||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー












 PDBj
PDBj