+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-8230 | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of GluA2-1xSTZ complex at 6.4 Angstrom resolution | |||||||||||||||
 マップデータ マップデータ | Cryo-EM structure of GluA2-1xSTZ complex at 6.4 Angstrom resolution | |||||||||||||||
 試料 試料 |
| |||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報Presynaptic depolarization and calcium channel opening / LGI-ADAM interactions /  regulation of postsynaptic neurotransmitter receptor activity / Trafficking of AMPA receptors / eye blink reflex / positive regulation of protein localization to basolateral plasma membrane / cerebellar mossy fiber / neurotransmitter receptor transport, postsynaptic endosome to lysosome / regulation of postsynaptic neurotransmitter receptor activity / Trafficking of AMPA receptors / eye blink reflex / positive regulation of protein localization to basolateral plasma membrane / cerebellar mossy fiber / neurotransmitter receptor transport, postsynaptic endosome to lysosome /  regulation of AMPA receptor activity / neurotransmitter receptor internalization ...Presynaptic depolarization and calcium channel opening / LGI-ADAM interactions / regulation of AMPA receptor activity / neurotransmitter receptor internalization ...Presynaptic depolarization and calcium channel opening / LGI-ADAM interactions /  regulation of postsynaptic neurotransmitter receptor activity / Trafficking of AMPA receptors / eye blink reflex / positive regulation of protein localization to basolateral plasma membrane / cerebellar mossy fiber / neurotransmitter receptor transport, postsynaptic endosome to lysosome / regulation of postsynaptic neurotransmitter receptor activity / Trafficking of AMPA receptors / eye blink reflex / positive regulation of protein localization to basolateral plasma membrane / cerebellar mossy fiber / neurotransmitter receptor transport, postsynaptic endosome to lysosome /  regulation of AMPA receptor activity / neurotransmitter receptor internalization / channel regulator activity / membrane hyperpolarization / postsynaptic neurotransmitter receptor diffusion trapping / regulation of AMPA receptor activity / neurotransmitter receptor internalization / channel regulator activity / membrane hyperpolarization / postsynaptic neurotransmitter receptor diffusion trapping /  nervous system process / protein targeting to membrane / neurotransmitter receptor localization to postsynaptic specialization membrane / neuromuscular junction development / spine synapse / dendritic spine neck / nervous system process / protein targeting to membrane / neurotransmitter receptor localization to postsynaptic specialization membrane / neuromuscular junction development / spine synapse / dendritic spine neck /  voltage-gated calcium channel complex / dendritic spine head / Activation of AMPA receptors / response to lithium ion / perisynaptic space / cellular response to glycine / transmission of nerve impulse / AMPA glutamate receptor activity / regulation of postsynaptic membrane neurotransmitter receptor levels / Trafficking of GluR2-containing AMPA receptors / voltage-gated calcium channel complex / dendritic spine head / Activation of AMPA receptors / response to lithium ion / perisynaptic space / cellular response to glycine / transmission of nerve impulse / AMPA glutamate receptor activity / regulation of postsynaptic membrane neurotransmitter receptor levels / Trafficking of GluR2-containing AMPA receptors /  脱分極 / 脱分極 /  immunoglobulin binding / AMPA glutamate receptor complex / kainate selective glutamate receptor activity / immunoglobulin binding / AMPA glutamate receptor complex / kainate selective glutamate receptor activity /  ionotropic glutamate receptor complex / extracellularly glutamate-gated ion channel activity / asymmetric synapse / regulation of receptor recycling / Unblocking of NMDA receptors, glutamate binding and activation / ionotropic glutamate receptor complex / extracellularly glutamate-gated ion channel activity / asymmetric synapse / regulation of receptor recycling / Unblocking of NMDA receptors, glutamate binding and activation /  voltage-gated calcium channel activity / voltage-gated calcium channel activity /  glutamate receptor binding / positive regulation of synaptic transmission / presynaptic active zone membrane / response to fungicide / glutamate-gated receptor activity / glutamate receptor binding / positive regulation of synaptic transmission / presynaptic active zone membrane / response to fungicide / glutamate-gated receptor activity /  regulation of synaptic transmission, glutamatergic / cellular response to brain-derived neurotrophic factor stimulus / somatodendritic compartment / dendrite membrane / ligand-gated monoatomic ion channel activity involved in regulation of presynaptic membrane potential / regulation of synaptic transmission, glutamatergic / cellular response to brain-derived neurotrophic factor stimulus / somatodendritic compartment / dendrite membrane / ligand-gated monoatomic ion channel activity involved in regulation of presynaptic membrane potential /  ionotropic glutamate receptor binding / hippocampal mossy fiber to CA3 synapse / ionotropic glutamate receptor binding / hippocampal mossy fiber to CA3 synapse /  cytoskeletal protein binding / cytoskeletal protein binding /  regulation of membrane potential / ionotropic glutamate receptor signaling pathway / dendrite cytoplasm / positive regulation of synaptic transmission, glutamatergic / regulation of membrane potential / ionotropic glutamate receptor signaling pathway / dendrite cytoplasm / positive regulation of synaptic transmission, glutamatergic /  SNARE binding / dendritic shaft / transmitter-gated monoatomic ion channel activity involved in regulation of postsynaptic membrane potential / SNARE binding / dendritic shaft / transmitter-gated monoatomic ion channel activity involved in regulation of postsynaptic membrane potential /  synaptic membrane / synaptic membrane /  synaptic transmission, glutamatergic / synaptic transmission, glutamatergic /  PDZ domain binding / postsynaptic density membrane / protein tetramerization / modulation of chemical synaptic transmission / Schaffer collateral - CA1 synapse / establishment of protein localization / PDZ domain binding / postsynaptic density membrane / protein tetramerization / modulation of chemical synaptic transmission / Schaffer collateral - CA1 synapse / establishment of protein localization /  terminal bouton / terminal bouton /  receptor internalization / synaptic vesicle membrane / cerebral cortex development / response to calcium ion / receptor internalization / synaptic vesicle membrane / cerebral cortex development / response to calcium ion /  シナプス小胞 / presynapse / シナプス小胞 / presynapse /  signaling receptor activity / signaling receptor activity /  presynaptic membrane / presynaptic membrane /  amyloid-beta binding / amyloid-beta binding /  成長円錐 / chemical synaptic transmission / 成長円錐 / chemical synaptic transmission /  perikaryon / perikaryon /  postsynaptic membrane / postsynaptic membrane /  scaffold protein binding / scaffold protein binding /  樹状突起スパイン / 樹状突起スパイン /  postsynaptic density / neuron projection / postsynaptic density / neuron projection /  神経繊維 / 神経繊維 /  樹状突起 / neuronal cell body / glutamatergic synapse / 樹状突起 / neuronal cell body / glutamatergic synapse /  シナプス / protein-containing complex binding / endoplasmic reticulum membrane / シナプス / protein-containing complex binding / endoplasmic reticulum membrane /  protein kinase binding / protein kinase binding /  細胞膜 / 細胞膜 /  小胞体 / protein-containing complex / 小胞体 / protein-containing complex /  生体膜 / identical protein binding / 生体膜 / identical protein binding /  細胞膜 細胞膜類似検索 - 分子機能 | |||||||||||||||
| 生物種 |   Rattus norvegicus (ドブネズミ) / Rattus norvegicus (ドブネズミ) /   Mus musculus (ハツカネズミ) Mus musculus (ハツカネズミ) | |||||||||||||||
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 6.4 Å クライオ電子顕微鏡法 / 解像度: 6.4 Å | |||||||||||||||
 データ登録者 データ登録者 | Twomey EC / Yelshanskaya MV / Grassucci RA / Frank J / Sobolevsky AI | |||||||||||||||
| 資金援助 |  米国, 4件 米国, 4件
| |||||||||||||||
 引用 引用 |  ジャーナル: Science / 年: 2016 ジャーナル: Science / 年: 2016タイトル: Elucidation of AMPA receptor-stargazin complexes by cryo-electron microscopy. 著者: Edward C Twomey / Maria V Yelshanskaya / Robert A Grassucci / Joachim Frank / Alexander I Sobolevsky /  要旨: AMPA-subtype ionotropic glutamate receptors (AMPARs) mediate fast excitatory neurotransmission and contribute to high cognitive processes such as learning and memory. In the brain, AMPAR trafficking, ...AMPA-subtype ionotropic glutamate receptors (AMPARs) mediate fast excitatory neurotransmission and contribute to high cognitive processes such as learning and memory. In the brain, AMPAR trafficking, gating, and pharmacology is tightly controlled by transmembrane AMPAR regulatory proteins (TARPs). Here, we used cryo-electron microscopy to elucidate the structural basis of AMPAR regulation by one of these auxiliary proteins, TARP γ2, or stargazin (STZ). Our structures illuminate the variable interaction stoichiometry of the AMPAR-TARP complex, with one or two TARP molecules binding one tetrameric AMPAR. Analysis of the AMPAR-STZ binding interfaces suggests that electrostatic interactions between the extracellular domains of AMPAR and STZ play an important role in modulating AMPAR function through contact surfaces that are conserved across AMPARs and TARPs. We propose a model explaining how TARPs stabilize the activated state of AMPARs and how the interactions between AMPARs and their auxiliary proteins control fast excitatory synaptic transmission. | |||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_8230.map.gz emd_8230.map.gz | 13.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-8230-v30.xml emd-8230-v30.xml emd-8230.xml emd-8230.xml | 14.7 KB 14.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_8230.png emd_8230.png | 42.3 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-8230 http://ftp.pdbj.org/pub/emdb/structures/EMD-8230 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8230 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8230 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_8230.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_8230.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Cryo-EM structure of GluA2-1xSTZ complex at 6.4 Angstrom resolution | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.02 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Protein
| 全体 | 名称: Protein タンパク質 タンパク質 |
|---|---|
| 要素 |
|
-超分子 #1: Protein
| 超分子 | 名称: Protein / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:   Rattus norvegicus (ドブネズミ) Rattus norvegicus (ドブネズミ) |
| 組換発現 | 生物種:   Homo sapiens (ヒト) / 組換細胞: HEK293 / 組換プラスミド: Bacmam Homo sapiens (ヒト) / 組換細胞: HEK293 / 組換プラスミド: Bacmam |
-分子 #1: Glutamate receptor 2,Voltage-dependent calcium channel gamma-2 subunit
| 分子 | 名称: Glutamate receptor 2,Voltage-dependent calcium channel gamma-2 subunit タイプ: protein_or_peptide / ID: 1 / コピー数: 4 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:   Mus musculus (ハツカネズミ) Mus musculus (ハツカネズミ) |
| 分子量 | 理論値: 115.515984 KDa |
| 組換発現 | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: NSIQIGGLFP RGADQEYSAF RVGMVQFSTS EFRLTPHIDN LEVANSFAVT NAFCSQFSRG VYAIFGFYDK KSVNTITSFC GTLHVSFIT PSFPTDGTHP FVIQMRPDLK GALLSLIEYY QWDKFAYLYD SDRGLSTLQA VLDSAAEKKW QVTAINVGNI N NDKKDETY ...文字列: NSIQIGGLFP RGADQEYSAF RVGMVQFSTS EFRLTPHIDN LEVANSFAVT NAFCSQFSRG VYAIFGFYDK KSVNTITSFC GTLHVSFIT PSFPTDGTHP FVIQMRPDLK GALLSLIEYY QWDKFAYLYD SDRGLSTLQA VLDSAAEKKW QVTAINVGNI N NDKKDETY RSLFQDLELK KERRVILDCE RDKVNDIVDQ VITIGKHVKG YHYIIANLGF TDGDLLKIQF GGAEVSGFQI VD YDDSLVS KFIERWSTLE EKEYPGAHTA TIKYTSALTY DAVQVMTEAF RNLRKQRIEI SRRGNAGDCL ANPAVPWGQG VEI ERALKQ VQVEGLSGNI KFDQNGKRIN YTINIMELKT NGPRKIGYWS EVDKMVLTED DTSGLEQKTV VVTTILESPY VMMK KNHEM LEGNERYEGY CVDLAAEIAK HCGFKYKLTI VGDGKYGARD ADTKIWNGMV GELVYGKADI AIAPLTITLV REEVI DFSK PFMSLGISIM IKKPQKSKPG VFSFLDPLAY EIWMCIVFAY IGVSVVLFLV SRFSPYEWHT EEFEDGRETQ SSESTN EFG IFNSLWFSLG AFMQQGCDIS PRSLSGRIVG GVWWFFTLII ISSYTANLAA FLTVERMVSP IESAEDLSKQ TEIAYGT LD SGSTKEFFRR SKIAVFDKMW TYMRSAEPSV FVRTTAEGVA RVRKSKGKYA YLLESTMNEY IEQRKPCDTM KVGGNLDS K GYGIATPKGS SLGTPVNLAV LKLSEQGLLD KLKNKWWYDK GECGAKDSGS KEKTSALSLS NVAGVFYILV GGLGLAMLV ALIEFCYKSR AEAKRMKGTG LFDRGVQMLL TTVGAFAAFS LMTIAVGTDY WLYSRGVCKT KSVSEDETSK KNEEVMTHSG LWRTCCLEG NFKGLCKQID HFPEDADYEA DTAEYFLRAV RASSIFPILS VILLFMGGLC IAASEFYKTR HNIILSAGIF F VSAGLSNI IGIIVYISAN AGDPSKSDSK KNSYSYGWSF YFGALSFIIA EMVGVLAVHM FIDRHKQLTG GLVPRG |
-分子 #2: {[7-morpholin-4-yl-2,3-dioxo-6-(trifluoromethyl)-3,4-dihydroquino...
| 分子 | 名称: {[7-morpholin-4-yl-2,3-dioxo-6-(trifluoromethyl)-3,4-dihydroquinoxalin-1(2H)-yl]methyl}phosphonic acid タイプ: ligand / ID: 2 / コピー数: 4 / 式: ZK1 |
|---|---|
| 分子量 | 理論値: 409.254 Da |
| Chemical component information | 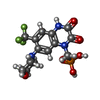 ChemComp-ZK1: |
-分子 #3: 2-acetamido-2-deoxy-beta-D-glucopyranose
| 分子 | 名称: 2-acetamido-2-deoxy-beta-D-glucopyranose / タイプ: ligand / ID: 3 / コピー数: 4 / 式: NAG |
|---|---|
| 分子量 | 理論値: 221.208 Da |
| Chemical component information |  ChemComp-NAG: |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 2 mg/mL |
|---|---|
| 緩衝液 | pH: 8 |
| グリッド | モデル: C-Flat Au 1.2/1.3 / 材質: GOLD / メッシュ: 200 / 詳細: Grid coated with gold prior to use. |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 295 K / 装置: FEI VITROBOT MARK IV / 詳細: 3 blot force, 8.0 s blot time. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD Bright-field microscopy Bright-field microscopy |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: SUPER-RESOLUTION / デジタル化 - 画像ごとのフレーム数: 1-40 / 撮影したグリッド数: 1 / 平均露光時間: 8.0 sec. / 平均電子線量: 80.0 e/Å2 詳細: 40 frames were collected across 8 seconds per image. |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| CTF補正 | ソフトウェア - 名称: CTFFIND (ver. 4.0) |
|---|---|
| 初期モデル | モデルのタイプ: PDB ENTRY PDBモデル - PDB ID: |
| 初期 角度割当 | タイプ: OTHER / ソフトウェア - 名称: RELION (ver. 1.4) |
| 最終 角度割当 | タイプ: OTHER / ソフトウェア - 名称: RELION (ver. 1.4) |
| 最終 再構成 | 想定した対称性 - 点群: C1 (非対称) / 解像度のタイプ: BY AUTHOR / 解像度: 6.4 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 39972 |
 ムービー
ムービー コントローラー
コントローラー


























