+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-4403 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
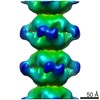
| タイトル | Electron microscopy map of human IMPDH isoform 1 bound to ATP in 150 g/L Ficoll-70 | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | らせん対称体再構成法 /  ネガティブ染色法 / 解像度: 24.0 Å ネガティブ染色法 / 解像度: 24.0 Å | |||||||||
 データ登録者 データ登録者 | Martin-Benito J / Nunez R / Fernandez-Justel D / Revuelta JL / Buey RM | |||||||||
 引用 引用 |  ジャーナル: J Mol Biol / 年: 2019 ジャーナル: J Mol Biol / 年: 2019タイトル: A Nucleotide-Dependent Conformational Switch Controls the Polymerization of Human IMP Dehydrogenases to Modulate their Catalytic Activity. 著者: David Fernández-Justel / Rafael Núñez / Jaime Martín-Benito / David Jimeno / Adrián González-López / Eva María Soriano / José Luis Revuelta / Rubén M Buey /  要旨: Inosine 5'-monophosphate dehydrogenase (IMPDH) catalyzes the rate-limiting step in the de novo GTP biosynthetic pathway and plays essential roles in cell proliferation. As a clinical target, IMPDH ...Inosine 5'-monophosphate dehydrogenase (IMPDH) catalyzes the rate-limiting step in the de novo GTP biosynthetic pathway and plays essential roles in cell proliferation. As a clinical target, IMPDH has been studied for decades, but it has only been within the last years that we are starting to understand the complexity of the mechanisms of its physiological regulation. Here, we report structural and functional insights into how adenine and guanine nucleotides control a conformational switch that modulates the assembly of the two human IMPDH enzymes into cytoophidia and allosterically regulates their catalytic activity. In vitro reconstituted micron-length cytoophidia-like structures show catalytic activity comparable to unassembled IMPDH but, in turn, are more resistant to GTP/GDP allosteric inhibition. Therefore, IMPDH cytoophidia formation facilitates the accumulation of high levels of guanine nucleotides when the cell requires it. Finally, we demonstrate that most of the IMPDH retinopathy-associated mutations abrogate GTP/GDP-induced allosteric inhibition and alter cytoophidia dynamics. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_4403.map.gz emd_4403.map.gz | 4.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-4403-v30.xml emd-4403-v30.xml emd-4403.xml emd-4403.xml | 12.3 KB 12.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_4403.png emd_4403.png | 37 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-4403 http://ftp.pdbj.org/pub/emdb/structures/EMD-4403 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4403 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4403 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_4403.map.gz / 形式: CCP4 / 大きさ: 6.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_4403.map.gz / 形式: CCP4 / 大きさ: 6.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 2.7 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : filaments of human IMP dehydrogenase isoform 1 in complex with ATP
| 全体 | 名称: filaments of human IMP dehydrogenase isoform 1 in complex with ATP |
|---|---|
| 要素 |
|
-超分子 #1: filaments of human IMP dehydrogenase isoform 1 in complex with ATP
| 超分子 | 名称: filaments of human IMP dehydrogenase isoform 1 in complex with ATP タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all 詳細: The filaments are formed in the presence of macromolecular crowding conditions (150 g/L Ficoll-70) |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 組換発現 | 生物種:   Escherichia coli (大腸菌) Escherichia coli (大腸菌) |
-分子 #1: human IMP dehydrogenase isoform 1
| 分子 | 名称: human IMP dehydrogenase isoform 1 / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO / EC番号:  IMPデヒドロゲナーゼ IMPデヒドロゲナーゼ |
|---|---|
| 配列 | 文字列: gshmadylis ggtgyvpedg ltaqqlfasa dgltyndfli lpgfidfiad evdltsaltr kitlktplis spmdtvtead maiamalmgg igfihhnctp efqanevrkv kkfeqgfitd pvvlspshtv gdvleakmrh gfsgipitet gtmgsklvgi vtsrdidfla ...文字列: gshmadylis ggtgyvpedg ltaqqlfasa dgltyndfli lpgfidfiad evdltsaltr kitlktplis spmdtvtead maiamalmgg igfihhnctp efqanevrkv kkfeqgfitd pvvlspshtv gdvleakmrh gfsgipitet gtmgsklvgi vtsrdidfla ekdhttllse vmtprielvv apagvtlkea neilqrskkg klpivndcde lvaiiartdl kknrdyplas kdsqkqllcg aavgtreddk yrldlltqag vdvivldssq gnsvyqiamv hyikqkyphl qviggnvvta aqaknlidag vdglrvgmgc gsicitqevm acgrpqgtav ykvaeyarrf gvpiiadggi qtvghvvkal algastvmmg sllaatteap geyffsdgvr lkkyrgmgsl damekssssq kryfsegdkv kiaqgvsgsi qdkgsiqkfv pyliagiqhg cqdigarsls vlrsmmysge lkfekrtmsa qieggvhglh syekrly |
-実験情報
-構造解析
| 手法 |  ネガティブ染色法 ネガティブ染色法 |
|---|---|
 解析 解析 | らせん対称体再構成法 |
| 試料の集合状態 | helical array |
- 試料調製
試料調製
| 緩衝液 | pH: 8 |
|---|---|
| 染色 | タイプ: NEGATIVE / 材質: Uranyl Acetate |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | JEOL 1230 |
|---|---|
| 電子線 | 加速電圧: 100 kV / 電子線源: TUNGSTEN HAIRPIN |
| 電子光学系 | C2レンズ絞り径: 100.0 µm / 最大 デフォーカス(補正後): 1.5 µm / 最小 デフォーカス(補正後): 1.0 µm / 倍率(補正後): 54929 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 2.9 mm / 最大 デフォーカス(公称値): 1.5 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 40000 Bright-field microscopy / Cs: 2.9 mm / 最大 デフォーカス(公称値): 1.5 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 40000 |
| 試料ステージ | 試料ホルダーモデル: JEOL |
| 撮影 | フィルム・検出器のモデル: TVIPS TEMCAM-F416 (4k x 4k) デジタル化 - サイズ - 横: 4096 pixel / デジタル化 - サイズ - 縦: 4096 pixel / デジタル化 - サンプリング間隔: 15.6 µm / 撮影したグリッド数: 1 / 実像数: 75 / 平均露光時間: 1.0 sec. / 平均電子線量: 20.0 e/Å2 |
- 画像解析
画像解析
| Segment selection | 選択した数: 3050 / ソフトウェア - 名称: Xmipp (ver. 3.0) |
|---|---|
| CTF補正 | ソフトウェア - 名称: CTFFIND (ver. 3) |
| 初期モデル | モデルのタイプ: INSILICO MODEL / In silico モデル: Generated with IHRSR 詳細: Horizontally pre-aligned using CL2D protocol implemented in Scipon/XMIPP software. |
| 最終 角度割当 | タイプ: NOT APPLICABLE / ソフトウェア - 名称: RELION (ver. 2.0) |
| 最終 再構成 | 使用したクラス数: 1 想定した対称性 - らせんパラメータ - Δz: 114.7 Å 想定した対称性 - らせんパラメータ - ΔΦ: 30.5 ° 想定した対称性 - らせんパラメータ - 軸対称性: C4 (4回回転対称  ) )アルゴリズム: BACK PROJECTION / 解像度のタイプ: BY AUTHOR / 解像度: 24.0 Å / 解像度の算出法: OTHER / ソフトウェア - 名称: RELION (ver. 2.0) / 使用した粒子像数: 1226 |
 ムービー
ムービー コントローラー
コントローラー