+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-0290 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
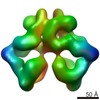
| タイトル | Immature M-PMV capsid hexamer structure in intact virus particles | |||||||||
 マップデータ マップデータ | None | |||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 dUTP diphosphatase / dUTP diphosphatase /  dUTP diphosphatase activity / nucleotide metabolic process / dUTP diphosphatase activity / nucleotide metabolic process /  加水分解酵素; プロテアーゼ; ペプチド結合加水分解酵素; アスパラギン酸プロテアーゼ / 加水分解酵素; プロテアーゼ; ペプチド結合加水分解酵素; アスパラギン酸プロテアーゼ /  リボヌクレアーゼH / viral process / DNA integration / リボヌクレアーゼH / viral process / DNA integration /  逆転写酵素 / viral genome integration into host DNA / establishment of integrated proviral latency ... 逆転写酵素 / viral genome integration into host DNA / establishment of integrated proviral latency ... dUTP diphosphatase / dUTP diphosphatase /  dUTP diphosphatase activity / nucleotide metabolic process / dUTP diphosphatase activity / nucleotide metabolic process /  加水分解酵素; プロテアーゼ; ペプチド結合加水分解酵素; アスパラギン酸プロテアーゼ / 加水分解酵素; プロテアーゼ; ペプチド結合加水分解酵素; アスパラギン酸プロテアーゼ /  リボヌクレアーゼH / viral process / DNA integration / リボヌクレアーゼH / viral process / DNA integration /  逆転写酵素 / viral genome integration into host DNA / establishment of integrated proviral latency / 逆転写酵素 / viral genome integration into host DNA / establishment of integrated proviral latency /  RNA-directed DNA polymerase activity / RNA-directed DNA polymerase activity /  転移酵素; リンを含む基を移すもの; 核酸を移すもの / RNA-DNA hybrid ribonuclease activity / viral nucleocapsid / DNA recombination / structural constituent of virion / 転移酵素; リンを含む基を移すもの; 核酸を移すもの / RNA-DNA hybrid ribonuclease activity / viral nucleocapsid / DNA recombination / structural constituent of virion /  加水分解酵素; エステル加水分解酵素 / 加水分解酵素; エステル加水分解酵素 /  DNAポリメラーゼ / aspartic-type endopeptidase activity / DNAポリメラーゼ / aspartic-type endopeptidase activity /  DNA-directed DNA polymerase activity / symbiont entry into host cell / DNA-directed DNA polymerase activity / symbiont entry into host cell /  タンパク質分解 / タンパク質分解 /  DNA binding / DNA binding /  RNA binding / zinc ion binding RNA binding / zinc ion binding類似検索 - 分子機能 | |||||||||
| 生物種 |   Mason-Pfizer monkey virus (ウイルス) Mason-Pfizer monkey virus (ウイルス) | |||||||||
| 手法 | サブトモグラム平均法 /  クライオ電子顕微鏡法 / 解像度: 7.2 Å クライオ電子顕微鏡法 / 解像度: 7.2 Å | |||||||||
 データ登録者 データ登録者 | Qu K / Glass B / Dolezal M / Schur FKM / Rein A / Rumlova M / Ruml T / Kraeusslich HG / Briggs JAG | |||||||||
 引用 引用 |  ジャーナル: Proc Natl Acad Sci U S A / 年: 2018 ジャーナル: Proc Natl Acad Sci U S A / 年: 2018タイトル: Structure and architecture of immature and mature murine leukemia virus capsids. 著者: Kun Qu / Bärbel Glass / Michal Doležal / Florian K M Schur / Brice Murciano / Alan Rein / Michaela Rumlová / Tomáš Ruml / Hans-Georg Kräusslich / John A G Briggs /      要旨: Retroviruses assemble and bud from infected cells in an immature form and require proteolytic maturation for infectivity. The CA (capsid) domains of the Gag polyproteins assemble a protein lattice as ...Retroviruses assemble and bud from infected cells in an immature form and require proteolytic maturation for infectivity. The CA (capsid) domains of the Gag polyproteins assemble a protein lattice as a truncated sphere in the immature virion. Proteolytic cleavage of Gag induces dramatic structural rearrangements; a subset of cleaved CA subsequently assembles into the mature core, whose architecture varies among retroviruses. Murine leukemia virus (MLV) is the prototypical γ-retrovirus and serves as the basis of retroviral vectors, but the structure of the MLV CA layer is unknown. Here we have combined X-ray crystallography with cryoelectron tomography to determine the structures of immature and mature MLV CA layers within authentic viral particles. This reveals the structural changes associated with maturation, and, by comparison with HIV-1, uncovers conserved and variable features. In contrast to HIV-1, most MLV CA is used for assembly of the mature core, which adopts variable, multilayered morphologies and does not form a closed structure. Unlike in HIV-1, there is similarity between protein-protein interfaces in the immature MLV CA layer and those in the mature CA layer, and structural maturation of MLV could be achieved through domain rotations that largely maintain hexameric interactions. Nevertheless, the dramatic architectural change on maturation indicates that extensive disassembly and reassembly are required for mature core growth. The core morphology suggests that wrapping of the genome in CA sheets may be sufficient to protect the MLV ribonucleoprotein during cell entry. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_0290.map.gz emd_0290.map.gz | 24.9 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-0290-v30.xml emd-0290-v30.xml emd-0290.xml emd-0290.xml | 14.5 KB 14.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_0290.png emd_0290.png | 385.1 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-0290 http://ftp.pdbj.org/pub/emdb/structures/EMD-0290 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0290 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0290 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  6hwiMC  0291C  0292C  0293C  4419C  4421C  4422C  6gzaC  6hwwC  6hwxC  6hwyC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_0290.map.gz / 形式: CCP4 / 大きさ: 27 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_0290.map.gz / 形式: CCP4 / 大きさ: 27 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | None | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.35 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Mason-Pfizer monkey virus
| 全体 | 名称:   Mason-Pfizer monkey virus (ウイルス) Mason-Pfizer monkey virus (ウイルス) |
|---|---|
| 要素 |
|
-超分子 #1: Mason-Pfizer monkey virus
| 超分子 | 名称: Mason-Pfizer monkey virus / タイプ: virus / ID: 1 / 親要素: 0 / 含まれる分子: all / NCBI-ID: 11855 / 生物種: Mason-Pfizer monkey virus / ウイルスタイプ: VIRION / ウイルス・単離状態: STRAIN / ウイルス・エンベロープ: Yes / ウイルス・中空状態: No |
|---|---|
| Host system | 生物種:   Homo sapiens (ヒト) / 組換細胞: HEK 293T / 組換プラスミド: pSHRM15 D26N Homo sapiens (ヒト) / 組換細胞: HEK 293T / 組換プラスミド: pSHRM15 D26N |
-分子 #1: Gag-Pro-Pol polyprotein
| 分子 | 名称: Gag-Pro-Pol polyprotein / タイプ: protein_or_peptide / ID: 1 / コピー数: 3 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:   Mason-Pfizer monkey virus (ウイルス) Mason-Pfizer monkey virus (ウイルス) |
| 分子量 | 理論値: 21.817359 KDa |
| 組換発現 | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: GFDFAVIKEL KTAASQYGAT APYTLAIVES VADNWLTPTD WNTLVRAVLS GGDHLLWKSE FFENCRDTAK RNQQAGNGWD FDMLTGSGN YSSTDAQMQY DPGLFAQIQA AATKAWRKLP VKGDPGASLT GVKQGPDEPF ADFVHRLITT AGRIFGSAEA G VDYVKQLA ...文字列: GFDFAVIKEL KTAASQYGAT APYTLAIVES VADNWLTPTD WNTLVRAVLS GGDHLLWKSE FFENCRDTAK RNQQAGNGWD FDMLTGSGN YSSTDAQMQY DPGLFAQIQA AATKAWRKLP VKGDPGASLT GVKQGPDEPF ADFVHRLITT AGRIFGSAEA G VDYVKQLA YENANPACQA AIRPYRKKTD LTGYIRLCSD IG |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | サブトモグラム平均法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 6 |
|---|---|
| グリッド | モデル: C-flat-2/1 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 95 % / チャンバー内温度: 288 K / 装置: FEI VITROBOT MARK II |
| 詳細 | Purified virus solution was inactivated and diluted 1:1 with PBS containing 10 nm colloidal gold. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 4.5 µm / 最小 デフォーカス(公称値): 2.0 µm / 倍率(公称値): 105000 Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 4.5 µm / 最小 デフォーカス(公称値): 2.0 µm / 倍率(公称値): 105000 |
| 特殊光学系 | エネルギーフィルター - 名称: GIF Quantum LS / エネルギーフィルター - スリット幅: 20 eV |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 撮影 | フィルム・検出器のモデル: GATAN K2 QUANTUM (4k x 4k) 検出モード: SUPER-RESOLUTION / デジタル化 - サイズ - 横: 3710 pixel / デジタル化 - サイズ - 縦: 3838 pixel / デジタル化 - サンプリング間隔: 5.0 µm / デジタル化 - 画像ごとのフレーム数: 1-6 / 撮影したグリッド数: 1 / 平均露光時間: 0.6 sec. / 平均電子線量: 2.0 e/Å2 詳細: Dose fluctuation was caused by the ring collapse of FEG during data collection. |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 抽出 | トモグラム数: 34 / 使用した粒子像数: 17109 ソフトウェア:
| ||||||
|---|---|---|---|---|---|---|---|
| CTF補正 | ソフトウェア:
| ||||||
| 最終 角度割当 | タイプ: OTHER / ソフトウェア: (名称: AV3, TOM) / 詳細: Subtomogram Averaging. | ||||||
| 最終 再構成 | 想定した対称性 - 点群: C6 (6回回転対称 ) / 解像度のタイプ: BY AUTHOR / 解像度: 7.2 Å / 解像度の算出法: FSC 0.143 CUT-OFF / ソフトウェア: (名称: AV3, TOM) / 使用したサブトモグラム数: 17109 ) / 解像度のタイプ: BY AUTHOR / 解像度: 7.2 Å / 解像度の算出法: FSC 0.143 CUT-OFF / ソフトウェア: (名称: AV3, TOM) / 使用したサブトモグラム数: 17109 |
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: FLEXIBLE FIT |
|---|---|
| 得られたモデル |  PDB-6hwi: |
 ムービー
ムービー コントローラー
コントローラー