+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-3417 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
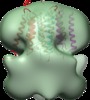
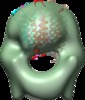
| タイトル | Structure of tetrameric MotA complex | |||||||||
 マップデータ マップデータ | Reconstruction of Aquifex aeolicus stator protein, tetrameric MotA complex | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Flagella motor /  Stator (固定子) / Stator (固定子) /  Single Particle analysis (単粒子解析法) / Single Particle analysis (単粒子解析法) /  Proton motive force (化学浸透) Proton motive force (化学浸透) | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報bacterial-type flagellum-dependent swarming motility / proton transmembrane transport /  走化性 / membrane => GO:0016020 / 走化性 / membrane => GO:0016020 /  細胞膜 細胞膜類似検索 - 分子機能 | |||||||||
| 生物種 |    Aquifex aeolicus (バクテリア) Aquifex aeolicus (バクテリア) | |||||||||
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  ネガティブ染色法 / 解像度: 25.0 Å ネガティブ染色法 / 解像度: 25.0 Å | |||||||||
 データ登録者 データ登録者 | Takekawa N / Terahara N / Kato T / Gohara M / Mayanagi K / Hijikata A / Onoue Y / Kojima S / Shirai T / Namba K / Homma M | |||||||||
 引用 引用 |  ジャーナル: Sci Rep / 年: 2016 ジャーナル: Sci Rep / 年: 2016タイトル: The tetrameric MotA complex as the core of the flagellar motor stator from hyperthermophilic bacterium. 著者: Norihiro Takekawa / Naoya Terahara / Takayuki Kato / Mizuki Gohara / Kouta Mayanagi / Atsushi Hijikata / Yasuhiro Onoue / Seiji Kojima / Tsuyoshi Shirai / Keiichi Namba / Michio Homma /  要旨: Rotation of bacterial flagellar motor is driven by the interaction between the stator and rotor, and the driving energy is supplied by ion influx through the stator channel. The stator is composed of ...Rotation of bacterial flagellar motor is driven by the interaction between the stator and rotor, and the driving energy is supplied by ion influx through the stator channel. The stator is composed of the MotA and MotB proteins, which form a hetero-hexameric complex with a stoichiometry of four MotA and two MotB molecules. MotA and MotB are four- and single-transmembrane proteins, respectively. To generate torque, the MotA/MotB stator unit changes its conformation in response to the ion influx, and interacts with the rotor protein FliG. Here, we overproduced and purified MotA of the hyperthermophilic bacterium Aquifex aeolicus. A chemical crosslinking experiment revealed that MotA formed a multimeric complex, most likely a tetramer. The three-dimensional structure of the purified MotA, reconstructed by electron microscopy single particle imaging, consisted of a slightly elongated globular domain and a pair of arch-like domains with spiky projections, likely to correspond to the transmembrane and cytoplasmic domains, respectively. We show that MotA molecules can form a stable tetrameric complex without MotB, and for the first time, demonstrate the cytoplasmic structure of the stator. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_3417.map.gz emd_3417.map.gz | 741.5 KB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-3417-v30.xml emd-3417-v30.xml emd-3417.xml emd-3417.xml | 9.6 KB 9.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_3417.png emd_3417.png emd_3417_1.png emd_3417_1.png | 327.4 KB 319.5 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-3417 http://ftp.pdbj.org/pub/emdb/structures/EMD-3417 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3417 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3417 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_3417.map.gz / 形式: CCP4 / 大きさ: 1001 KB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_3417.map.gz / 形式: CCP4 / 大きさ: 1001 KB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Reconstruction of Aquifex aeolicus stator protein, tetrameric MotA complex | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 2.8 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Aquifex aeolicus MotA
| 全体 | 名称: Aquifex aeolicus MotA |
|---|---|
| 要素 |
|
-超分子 #1000: Aquifex aeolicus MotA
| 超分子 | 名称: Aquifex aeolicus MotA / タイプ: sample / ID: 1000 / 集合状態: tetramer / Number unique components: 1 |
|---|---|
| 分子量 | 理論値: 109 KDa |
-分子 #1: Motility protein A
| 分子 | 名称: Motility protein A / タイプ: protein_or_peptide / ID: 1 / Name.synonym: Chemotaxis protein MotA / コピー数: 4 / 集合状態: Tetramer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:    Aquifex aeolicus (バクテリア) / 株: VF5 Aquifex aeolicus (バクテリア) / 株: VF5 |
| 分子量 | 理論値: 109 KDa |
| 組換発現 | 生物種:   Escherichia coli (大腸菌) / 組換株: BL21-CodonPlus(DE3)-RIPL / 組換プラスミド: pColdI Escherichia coli (大腸菌) / 組換株: BL21-CodonPlus(DE3)-RIPL / 組換プラスミド: pColdI |
| 配列 | UniProtKB:  Motility protein A Motility protein A |
-実験情報
-構造解析
| 手法 |  ネガティブ染色法 ネガティブ染色法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.1 mg/mL |
|---|---|
| 緩衝液 | pH: 8 / 詳細: 50 mM Tris-HCl, 200 mM NaCl, 0.02% DMNG |
| 染色 | タイプ: NEGATIVE / 詳細: 2% w/v uranyl acetate |
| グリッド | 詳細: 200 mesh copper grid with continuous carbon suport, glow discharged |
| 凍結 | 凍結剤: NONE / 装置: OTHER |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | JEOL 3200FSC |
|---|---|
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 107140 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 4.1 mm / 最大 デフォーカス(公称値): 2.2 µm / 最小 デフォーカス(公称値): 1.135 µm / 倍率(公称値): 80000 Bright-field microscopy / Cs: 4.1 mm / 最大 デフォーカス(公称値): 2.2 µm / 最小 デフォーカス(公称値): 1.135 µm / 倍率(公称値): 80000 |
| 特殊光学系 | エネルギーフィルター - 名称: Omega Filter エネルギーフィルター - エネルギー下限: 0.0 eV エネルギーフィルター - エネルギー上限: 20.0 eV |
| 試料ステージ | 試料ホルダー: Nitrogen cooled / 試料ホルダーモデル: JEOL 3200FSC CRYOHOLDER |
| 温度 | 最低: 85.5 K / 最高: 85.7 K / 平均: 85.5 K |
| 日付 | 2015年11月16日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: TVIPS TEMCAM-F415 (4k x 4k) 実像数: 50 / 平均電子線量: 2.8 e/Å2 |
- 画像解析
画像解析
| 最終 再構成 | 想定した対称性 - 点群: C2 (2回回転対称 ) / 解像度のタイプ: BY AUTHOR / 解像度: 25.0 Å / 解像度の算出法: FSC 0.143 CUT-OFF / ソフトウェア - 名称: Relion-1.4 / 使用した粒子像数: 5419 ) / 解像度のタイプ: BY AUTHOR / 解像度: 25.0 Å / 解像度の算出法: FSC 0.143 CUT-OFF / ソフトウェア - 名称: Relion-1.4 / 使用した粒子像数: 5419 |
|---|
 ムービー
ムービー コントローラー
コントローラー