+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-2215 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | DOLORS: Versatile Strategy for Internal Labeling and Domain Localization in Electron Microscopy | |||||||||
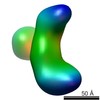
 マップデータ マップデータ | Platform-labeled Dicer | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Dicer Enzyme /  Ribonuclease III / MicroRNA Processing / Single Particle Electron Microscopy Ribonuclease III / MicroRNA Processing / Single Particle Electron Microscopy | |||||||||
| 生物種 |   Homo sapiens (ヒト) / Homo sapiens (ヒト) /   Streptomyces avidinii (バクテリア) Streptomyces avidinii (バクテリア) | |||||||||
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  ネガティブ染色法 ネガティブ染色法 | |||||||||
 データ登録者 データ登録者 | Lau PW / Potter CS / Carragher B / MacRae IJ | |||||||||
 引用 引用 |  ジャーナル: Structure / 年: 2012 ジャーナル: Structure / 年: 2012タイトル: DOLORS: versatile strategy for internal labeling and domain localization in electron microscopy. 著者: Pick-Wei Lau / Clinton S Potter / Bridget Carragher / Ian J MacRae /  要旨: Single-particle electron microscopy (EM) is a powerful tool for studying the structures of large biological molecules. However, the achievable resolution does not always allow for direct recognition ...Single-particle electron microscopy (EM) is a powerful tool for studying the structures of large biological molecules. However, the achievable resolution does not always allow for direct recognition of individual protein domains. Labels that can be visualized by EM have been developed for protein termini, but tagging internal domains remains a challenge. We describe a robust strategy for determining the position of internal sites within EM maps, termed domain localization by RCT sampling (DOLORS). DOLORS uses monovalent streptavidin added posttranslationally to tagged sites in the target protein. Internal labels generally display less conformational flexibility than terminal labels, providing more precise positional information. Automated methods are used to rapidly generate assemblies of unique 3D models allowing the attachment sites of labeled domains to be accurately identified and thus provide an overall architectural map of the molecule. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_2215.map.gz emd_2215.map.gz | 1.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-2215-v30.xml emd-2215-v30.xml emd-2215.xml emd-2215.xml | 9.7 KB 9.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  image2215.png image2215.png | 39.6 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-2215 http://ftp.pdbj.org/pub/emdb/structures/EMD-2215 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2215 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2215 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_2215.map.gz / 形式: CCP4 / 大きさ: 3.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_2215.map.gz / 形式: CCP4 / 大きさ: 3.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Platform-labeled Dicer | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 3.52 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Dicer labeled with streptavidin at the Platform domain
| 全体 | 名称: Dicer labeled with streptavidin at the Platform domain |
|---|---|
| 要素 |
|
-超分子 #1000: Dicer labeled with streptavidin at the Platform domain
| 超分子 | 名称: Dicer labeled with streptavidin at the Platform domain タイプ: sample / ID: 1000 / 詳細: The sample was mostly monodisperse / 集合状態: One human Dicer and one streptavidin molecule / Number unique components: 2 |
|---|---|
| 分子量 | 理論値: 280 KDa |
-分子 #1: Human Dicer
| 分子 | 名称: Human Dicer / タイプ: protein_or_peptide / ID: 1 / Name.synonym: hDicer / コピー数: 1 / 集合状態: Monomer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) / 別称: Human Homo sapiens (ヒト) / 別称: Human |
| 分子量 | 理論値: 220 KDa |
| 組換発現 | 生物種:   Spodoptera frugiperda (ツマジロクサヨトウ) Spodoptera frugiperda (ツマジロクサヨトウ) |
-分子 #2: Streptavidin
| 分子 | 名称: Streptavidin / タイプ: protein_or_peptide / ID: 2 / コピー数: 1 / 集合状態: Tetramer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:   Streptomyces avidinii (バクテリア) Streptomyces avidinii (バクテリア) |
| 分子量 | 理論値: 60 KDa |
| 組換発現 | 生物種:   Escherichia coli (大腸菌) Escherichia coli (大腸菌) |
-実験情報
-構造解析
| 手法 |  ネガティブ染色法 ネガティブ染色法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 / 詳細: 150mM KCl, 25mM HEPES |
|---|---|
| 染色 | タイプ: NEGATIVE 詳細: Grids with adsorbed protein floated on 2% w/v uranyl acetate |
| グリッド | 詳細: holey C-flat grids covered with an additional layer of thin carbon |
| 凍結 | 凍結剤: NONE / 装置: OTHER |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI F20 |
|---|---|
| 電子線 | 加速電圧: 120 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 62000 Bright-field microscopy / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 62000 |
| 試料ステージ | 試料ホルダーモデル: SIDE ENTRY, EUCENTRIC / Tilt angle max: 50 |
| 日付 | 2011年1月10日 |
| 撮影 | 実像数: 340 / 平均電子線量: 20 e/Å2 |
| Tilt angle min | 0 |
| 実験機器 |  モデル: Tecnai F20 / 画像提供: FEI Company |
- 画像解析
画像解析
| CTF補正 | 詳細: Each micrograph |
|---|---|
| 最終 2次元分類 | クラス数: 1 |
| 最終 再構成 | 想定した対称性 - 点群: C1 (非対称) / アルゴリズム: OTHER / ソフトウェア - 名称: Spider / 使用した粒子像数: 12639 |
| 詳細 | Processing was done using APPION pipeline |
-原子モデル構築 1
| 初期モデル | PDB ID: Chain - Chain ID: A |
|---|---|
| ソフトウェア | 名称:  Chimera Chimera |
| 詳細 | Protocol: Rigid body. manual docking based upon overall fit and correspondence to tagging data |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT |
 ムービー
ムービー コントローラー
コントローラー