+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Late alpha-Synuclein fibril structure from liquid-liquid phase separations. | |||||||||
 マップデータ マップデータ | helical refinement | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード |  Amyloid (アミロイド) / Amyloid (アミロイド) /  Fibril (フィブリル) / Fibril (フィブリル) /  Neurodegeneration (神経変性疾患) / Neurodegeneration (神経変性疾患) /  Parkinson's Disease (パーキンソン病) / PROTEIN FIBRIL Parkinson's Disease (パーキンソン病) / PROTEIN FIBRIL | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報negative regulation of mitochondrial electron transport, NADH to ubiquinone / neutral lipid metabolic process /  regulation of phospholipase activity / negative regulation of monooxygenase activity / regulation of acyl-CoA biosynthetic process / negative regulation of dopamine uptake involved in synaptic transmission / negative regulation of norepinephrine uptake / positive regulation of glutathione peroxidase activity / positive regulation of SNARE complex assembly / positive regulation of hydrogen peroxide catabolic process ...negative regulation of mitochondrial electron transport, NADH to ubiquinone / neutral lipid metabolic process / regulation of phospholipase activity / negative regulation of monooxygenase activity / regulation of acyl-CoA biosynthetic process / negative regulation of dopamine uptake involved in synaptic transmission / negative regulation of norepinephrine uptake / positive regulation of glutathione peroxidase activity / positive regulation of SNARE complex assembly / positive regulation of hydrogen peroxide catabolic process ...negative regulation of mitochondrial electron transport, NADH to ubiquinone / neutral lipid metabolic process /  regulation of phospholipase activity / negative regulation of monooxygenase activity / regulation of acyl-CoA biosynthetic process / negative regulation of dopamine uptake involved in synaptic transmission / negative regulation of norepinephrine uptake / positive regulation of glutathione peroxidase activity / positive regulation of SNARE complex assembly / positive regulation of hydrogen peroxide catabolic process / supramolecular fiber / negative regulation of transporter activity / negative regulation of chaperone-mediated autophagy / mitochondrial membrane organization / regulation of reactive oxygen species biosynthetic process / positive regulation of protein localization to cell periphery / regulation of phospholipase activity / negative regulation of monooxygenase activity / regulation of acyl-CoA biosynthetic process / negative regulation of dopamine uptake involved in synaptic transmission / negative regulation of norepinephrine uptake / positive regulation of glutathione peroxidase activity / positive regulation of SNARE complex assembly / positive regulation of hydrogen peroxide catabolic process / supramolecular fiber / negative regulation of transporter activity / negative regulation of chaperone-mediated autophagy / mitochondrial membrane organization / regulation of reactive oxygen species biosynthetic process / positive regulation of protein localization to cell periphery /  regulation of synaptic vesicle recycling / negative regulation of platelet-derived growth factor receptor signaling pathway / negative regulation of exocytosis / regulation of glutamate secretion / response to iron(II) ion / regulation of norepinephrine uptake / dopamine biosynthetic process / regulation of synaptic vesicle recycling / negative regulation of platelet-derived growth factor receptor signaling pathway / negative regulation of exocytosis / regulation of glutamate secretion / response to iron(II) ion / regulation of norepinephrine uptake / dopamine biosynthetic process /  SNARE complex assembly / positive regulation of neurotransmitter secretion / synaptic vesicle priming / dopamine uptake involved in synaptic transmission / regulation of locomotion / positive regulation of inositol phosphate biosynthetic process / SNARE complex assembly / positive regulation of neurotransmitter secretion / synaptic vesicle priming / dopamine uptake involved in synaptic transmission / regulation of locomotion / positive regulation of inositol phosphate biosynthetic process /  regulation of macrophage activation / mitochondrial ATP synthesis coupled electron transport / negative regulation of microtubule polymerization / synaptic vesicle transport / dynein complex binding / positive regulation of receptor recycling / regulation of dopamine secretion / regulation of macrophage activation / mitochondrial ATP synthesis coupled electron transport / negative regulation of microtubule polymerization / synaptic vesicle transport / dynein complex binding / positive regulation of receptor recycling / regulation of dopamine secretion /  protein kinase inhibitor activity / negative regulation of thrombin-activated receptor signaling pathway / response to type II interferon / cuprous ion binding / positive regulation of exocytosis / synaptic vesicle exocytosis / positive regulation of endocytosis / cysteine-type endopeptidase inhibitor activity involved in apoptotic process / response to magnesium ion / protein kinase inhibitor activity / negative regulation of thrombin-activated receptor signaling pathway / response to type II interferon / cuprous ion binding / positive regulation of exocytosis / synaptic vesicle exocytosis / positive regulation of endocytosis / cysteine-type endopeptidase inhibitor activity involved in apoptotic process / response to magnesium ion /  kinesin binding / regulation of presynapse assembly / alpha-tubulin binding / synaptic vesicle endocytosis / negative regulation of serotonin uptake / localization / phospholipid metabolic process / supramolecular fiber organization / axon terminus / kinesin binding / regulation of presynapse assembly / alpha-tubulin binding / synaptic vesicle endocytosis / negative regulation of serotonin uptake / localization / phospholipid metabolic process / supramolecular fiber organization / axon terminus /  封入体 / cellular response to copper ion / 封入体 / cellular response to copper ion /  Hsp70 protein binding / cellular response to epinephrine stimulus / Hsp70 protein binding / cellular response to epinephrine stimulus /  excitatory postsynaptic potential / response to interleukin-1 / adult locomotory behavior / excitatory postsynaptic potential / response to interleukin-1 / adult locomotory behavior /  SNARE binding / positive regulation of release of sequestered calcium ion into cytosol / fatty acid metabolic process / long-term synaptic potentiation / regulation of transmembrane transporter activity / SNARE binding / positive regulation of release of sequestered calcium ion into cytosol / fatty acid metabolic process / long-term synaptic potentiation / regulation of transmembrane transporter activity /  ferrous iron binding / protein tetramerization / synapse organization / ferrous iron binding / protein tetramerization / synapse organization /  phosphoprotein binding / regulation of long-term neuronal synaptic plasticity / microglial cell activation / negative regulation of protein kinase activity / phosphoprotein binding / regulation of long-term neuronal synaptic plasticity / microglial cell activation / negative regulation of protein kinase activity /  phospholipid binding / protein destabilization / PKR-mediated signaling / negative regulation of cysteine-type endopeptidase activity involved in apoptotic process / tau protein binding / positive regulation of protein serine/threonine kinase activity / phospholipid binding / protein destabilization / PKR-mediated signaling / negative regulation of cysteine-type endopeptidase activity involved in apoptotic process / tau protein binding / positive regulation of protein serine/threonine kinase activity /  receptor internalization / synaptic vesicle membrane / positive regulation of inflammatory response / activation of cysteine-type endopeptidase activity involved in apoptotic process / receptor internalization / synaptic vesicle membrane / positive regulation of inflammatory response / activation of cysteine-type endopeptidase activity involved in apoptotic process /  マイクロフィラメント / positive regulation of peptidyl-serine phosphorylation / cellular response to oxidative stress / マイクロフィラメント / positive regulation of peptidyl-serine phosphorylation / cellular response to oxidative stress /  actin binding / actin binding /  細胞皮質 / 細胞皮質 /  成長円錐 / 成長円錐 /  histone binding / chemical synaptic transmission / postsynapse / neuron apoptotic process / negative regulation of neuron apoptotic process / amyloid fibril formation / response to lipopolysaccharide / histone binding / chemical synaptic transmission / postsynapse / neuron apoptotic process / negative regulation of neuron apoptotic process / amyloid fibril formation / response to lipopolysaccharide /  リソソーム / リソソーム /  oxidoreductase activity / molecular adaptor activity / transcription cis-regulatory region binding oxidoreductase activity / molecular adaptor activity / transcription cis-regulatory region binding類似検索 - 分子機能 | |||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | らせん対称体再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.3 Å クライオ電子顕微鏡法 / 解像度: 3.3 Å | |||||||||
 データ登録者 データ登録者 | De Simone A / Barritt JD / Chen S / Cascella R / Cecchi C / Bigi A / Jarvis JA / Chiti F / Dobson CM / Fusco G | |||||||||
| 資金援助 | European Union, 1件
| |||||||||
 引用 引用 |  ジャーナル: J Am Chem Soc / 年: 2024 ジャーナル: J Am Chem Soc / 年: 2024タイトル: Structure-Toxicity Relationship in Intermediate Fibrils from α-Synuclein Condensates. 著者: Serene W Chen / Joseph D Barritt / Roberta Cascella / Alessandra Bigi / Cristina Cecchi / Martina Banchelli / Angelo Gallo / James A Jarvis / Fabrizio Chiti / Christopher M Dobson / Giuliana ...著者: Serene W Chen / Joseph D Barritt / Roberta Cascella / Alessandra Bigi / Cristina Cecchi / Martina Banchelli / Angelo Gallo / James A Jarvis / Fabrizio Chiti / Christopher M Dobson / Giuliana Fusco / Alfonso De Simone /   要旨: The aberrant aggregation of α-synuclein (αS) into amyloid fibrils is associated with a range of highly debilitating neurodegenerative conditions, including Parkinson's disease. Although the ...The aberrant aggregation of α-synuclein (αS) into amyloid fibrils is associated with a range of highly debilitating neurodegenerative conditions, including Parkinson's disease. Although the structural properties of mature amyloids of αS are currently understood, the nature of transient protofilaments and fibrils that appear during αS aggregation remains elusive. Using solid-state nuclear magnetic resonance (ssNMR), cryogenic electron microscopy (cryo-EM), and biophysical methods, we here characterized intermediate amyloid fibrils of αS forming during the aggregation from liquid-like spherical condensates to mature amyloids adopting the structure of pathologically observed aggregates. These transient amyloid intermediates, which induce significant levels of cytotoxicity when incubated with neuronal cells, were found to be stabilized by a small core in an antiparallel β-sheet conformation, with a disordered N-terminal region of the protein remaining available to mediate membrane binding. In contrast, mature amyloids that subsequently appear during the aggregation showed different structural and biological properties, including low levels of cytotoxicity, a rearranged structured core embedding also the N-terminal region, and a reduced propensity to interact with the membrane. The characterization of these two fibrillar forms of αS, and the use of antibodies and designed mutants, enabled us to clarify the role of critical structural elements endowing intermediate amyloid species with the ability to interact with membranes and induce cytotoxicity. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_19184.map.gz emd_19184.map.gz | 28.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-19184-v30.xml emd-19184-v30.xml emd-19184.xml emd-19184.xml | 17.3 KB 17.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_19184_fsc.xml emd_19184_fsc.xml | 7.2 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_19184.png emd_19184.png | 44.8 KB | ||
| Filedesc metadata |  emd-19184.cif.gz emd-19184.cif.gz | 6 KB | ||
| その他 |  emd_19184_half_map_1.map.gz emd_19184_half_map_1.map.gz emd_19184_half_map_2.map.gz emd_19184_half_map_2.map.gz | 23.3 MB 23.3 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-19184 http://ftp.pdbj.org/pub/emdb/structures/EMD-19184 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-19184 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-19184 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8ri9MC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_19184.map.gz / 形式: CCP4 / 大きさ: 30.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_19184.map.gz / 形式: CCP4 / 大きさ: 30.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | helical refinement | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.043 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #2
| ファイル | emd_19184_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
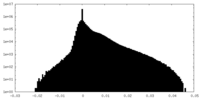
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_19184_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Fibrillar complex of alpha-synuclein
| 全体 | 名称: Fibrillar complex of alpha-synuclein |
|---|---|
| 要素 |
|
-超分子 #1: Fibrillar complex of alpha-synuclein
| 超分子 | 名称: Fibrillar complex of alpha-synuclein / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all 詳細: Late-fibrils of alpha-synuclein produced from long incubation of liquid-liquid phase separations. |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: Alpha-synuclein
| 分子 | 名称: Alpha-synuclein / タイプ: protein_or_peptide / ID: 1 / コピー数: 5 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 14.476108 KDa |
| 組換発現 | 生物種:   Escherichia coli (大腸菌) Escherichia coli (大腸菌) |
| 配列 | 文字列: MDVFMKGLSK AKEGVVAAAE KTKQGVAEAA GKTKEGVLYV GSKTKEGVVH GVATVAEKTK EQVTNVGGAV VTGVTAVAQK TVEGAGSIA AATGFVKKDQ LGKNEEGAPQ EGILEDMPVD PDNEAYEMPS EEGYQDYEPE A UniProtKB:  Α-シヌクレイン Α-シヌクレイン |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | らせん対称体再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 濃度 | 1.45 mg/mL |
|---|---|
| 緩衝液 | pH: 7.4 |
| グリッド | モデル: Quantifoil R2/2 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 60 sec. / 前処理 - 雰囲気: AIR / 前処理 - 気圧: 20.265 kPa |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 294 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 0.9 µm / 倍率(公称値): 120000 Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 0.9 µm / 倍率(公称値): 120000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: COUNTING / デジタル化 - サイズ - 横: 4096 pixel / デジタル化 - サイズ - 縦: 4096 pixel / 撮影したグリッド数: 1 / 実像数: 3262 / 平均電子線量: 43.0 e/Å2 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー




 Z
Z Y
Y X
X