+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-1614 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Globular tetramers of beta-2-microglobulin assemble into elaborate amyloid fibrils | |||||||||
 マップデータ マップデータ | Surface view of an B-type map from beta-2-microglobulin | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード |  protein misfolding (プロテオパチー) / protein misfolding (プロテオパチー) /  amyloid (アミロイド) / amyloid (アミロイド) /  cryo-EM (低温電子顕微鏡法) / cryo-EM (低温電子顕微鏡法) /  3D reconstruction / 3D reconstruction /  STEM (ステム) STEM (ステム) | |||||||||
| 機能・相同性 |  Β2-ミクログロブリン / MHC class I protein complex Β2-ミクログロブリン / MHC class I protein complex 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | らせん対称体再構成法 /  クライオ電子顕微鏡法 / 解像度: 25.0 Å クライオ電子顕微鏡法 / 解像度: 25.0 Å | |||||||||
 データ登録者 データ登録者 | White HE / Hodgkinson JL / Jahn TR / Cohen-Krausz S / Gosal WS / Muller S / Orlova EV / Radford SE / Saibil HR | |||||||||
 引用 引用 |  ジャーナル: J Mol Biol / 年: 2009 ジャーナル: J Mol Biol / 年: 2009タイトル: Globular tetramers of beta(2)-microglobulin assemble into elaborate amyloid fibrils. 著者: Helen E White / Julie L Hodgkinson / Thomas R Jahn / Sara Cohen-Krausz / Walraj S Gosal / Shirley Müller / Elena V Orlova / Sheena E Radford / Helen R Saibil /  要旨: Amyloid fibrils are ordered polymers in which constituent polypeptides adopt a non-native fold. Despite their importance in degenerative human diseases, the overall structure of amyloid fibrils ...Amyloid fibrils are ordered polymers in which constituent polypeptides adopt a non-native fold. Despite their importance in degenerative human diseases, the overall structure of amyloid fibrils remains unknown. High-resolution studies of model peptide assemblies have identified residues forming cross-beta-strands and have revealed some details of local beta-strand packing. However, little is known about the assembly contacts that define the fibril architecture. Here we present a set of three-dimensional structures of amyloid fibrils formed from full-length beta(2)-microglobulin, a 99-residue protein involved in clinical amyloidosis. Our cryo-electron microscopy maps reveal a hierarchical fibril structure built from tetrameric units of globular density, with at least three different subunit interfaces in this homopolymeric assembly. These findings suggest a more complex superstructure for amyloid than hitherto suspected and prompt a re-evaluation of the defining features of the amyloid fold. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_1614.map.gz emd_1614.map.gz | 1.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-1614-v30.xml emd-1614-v30.xml emd-1614.xml emd-1614.xml | 9.9 KB 9.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  1614.tif 1614.tif | 737.6 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-1614 http://ftp.pdbj.org/pub/emdb/structures/EMD-1614 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1614 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1614 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_1614.map.gz / 形式: CCP4 / 大きさ: 1.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_1614.map.gz / 形式: CCP4 / 大きさ: 1.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Surface view of an B-type map from beta-2-microglobulin | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 3.5 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
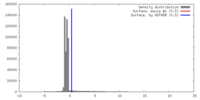
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : beta-2-microglobulin
| 全体 | 名称: beta-2-microglobulin Β2-ミクログロブリン Β2-ミクログロブリン |
|---|---|
| 要素 |
|
-超分子 #1000: beta-2-microglobulin
| 超分子 | 名称: beta-2-microglobulin / タイプ: sample / ID: 1000 / Number unique components: 1 |
|---|---|
| 分子量 | 実験値: 10 KDa |
-分子 #1: beta-2-microglobulin
| 分子 | 名称: beta-2-microglobulin / タイプ: protein_or_peptide / ID: 1 / Name.synonym: beta-2-microglobulin / 集合状態: monomer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) / 別称: Human / 細胞中の位置: plasma Homo sapiens (ヒト) / 別称: Human / 細胞中の位置: plasma |
| 分子量 | 実験値: 10 KDa |
| 組換発現 | 生物種:   Escherichia coli (大腸菌) / 組換プラスミド: pINKWT Escherichia coli (大腸菌) / 組換プラスミド: pINKWT |
| 配列 | GO: MHC class I protein complex / InterPro:  Β2-ミクログロブリン Β2-ミクログロブリン |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | らせん対称体再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 濃度 | 0.3 mg/mL |
|---|---|
| 緩衝液 | pH: 2.5 / 詳細: 25 mM sodium phosphate, 25 mM sodium acetate |
| グリッド | 詳細: holey carbon grids |
| 凍結 | 凍結剤: ETHANE / 装置: HOMEMADE PLUNGER / 詳細: Vitrification instrument: manual plunger |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI F20 |
|---|---|
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 2 mm / 最大 デフォーカス(公称値): 2.6 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 29000 Bright-field microscopy / Cs: 2 mm / 最大 デフォーカス(公称値): 2.6 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 29000 |
| 試料ステージ | 試料ホルダー: side entry / 試料ホルダーモデル: GATAN LIQUID NITROGEN |
| 温度 | 最低: 100 K |
| 詳細 | Low dose |
| 撮影 | カテゴリ: FILM / フィルム・検出器のモデル: KODAK SO-163 FILM / デジタル化 - スキャナー: ZEISS SCAI / デジタル化 - サンプリング間隔: 7 µm / 実像数: 85 / ビット/ピクセル: 8 |
| 実験機器 |  モデル: Tecnai F20 / 画像提供: FEI Company |
- 画像解析
画像解析
| CTF補正 | 詳細: Phase flipping |
|---|---|
| 最終 再構成 | 想定した対称性 - らせんパラメータ - Δz: 52.5 Å 想定した対称性 - らせんパラメータ - ΔΦ: 7.01 ° アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 25.0 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ソフトウェア - 名称: SPIDER 詳細: Maps were calculated for each class as each class had a different pitch. |
 ムービー
ムービー コントローラー
コントローラー










 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)