+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | CryoEM structure of Ku heterodimer bound to DNA | |||||||||
 マップデータ マップデータ | Ku hetero-dimer bound to DNA | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード |  NHEJ (非相同末端結合) / NHEJ (非相同末端結合) /  Ku70 (Ku70) / Ku70 (Ku70) /  Ku80 (Ku80) / Ku80 (Ku80) /  DNA damage (DNA修復) / DNA damage (DNA修復) /  DNA BINDING PROTEIN (DNA結合タンパク質) DNA BINDING PROTEIN (DNA結合タンパク質) | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報Ku70:Ku80 complex / negative regulation of t-circle formation /  DNA end binding / small-subunit processome assembly / positive regulation of lymphocyte differentiation / DNA-dependent protein kinase complex / DNA-dependent protein kinase-DNA ligase 4 complex / cellular response to X-ray / DNA end binding / small-subunit processome assembly / positive regulation of lymphocyte differentiation / DNA-dependent protein kinase complex / DNA-dependent protein kinase-DNA ligase 4 complex / cellular response to X-ray /  nonhomologous end joining complex / nonhomologous end joining complex /  DNA ligation ...Ku70:Ku80 complex / negative regulation of t-circle formation / DNA ligation ...Ku70:Ku80 complex / negative regulation of t-circle formation /  DNA end binding / small-subunit processome assembly / positive regulation of lymphocyte differentiation / DNA-dependent protein kinase complex / DNA-dependent protein kinase-DNA ligase 4 complex / cellular response to X-ray / DNA end binding / small-subunit processome assembly / positive regulation of lymphocyte differentiation / DNA-dependent protein kinase complex / DNA-dependent protein kinase-DNA ligase 4 complex / cellular response to X-ray /  nonhomologous end joining complex / nonhomologous end joining complex /  DNA ligation / nuclear telomere cap complex / regulation of smooth muscle cell proliferation / Cytosolic sensors of pathogen-associated DNA / double-strand break repair via classical nonhomologous end joining / IRF3-mediated induction of type I IFN / DNA ligation / nuclear telomere cap complex / regulation of smooth muscle cell proliferation / Cytosolic sensors of pathogen-associated DNA / double-strand break repair via classical nonhomologous end joining / IRF3-mediated induction of type I IFN /  相同組換え / 相同組換え /  regulation of telomere maintenance / U3 snoRNA binding / positive regulation of neurogenesis / protein localization to chromosome, telomeric region / cellular response to fatty acid / hematopoietic stem cell proliferation / cellular hyperosmotic salinity response / telomeric DNA binding / positive regulation of catalytic activity / 2-LTR circle formation / site of DNA damage / regulation of telomere maintenance / U3 snoRNA binding / positive regulation of neurogenesis / protein localization to chromosome, telomeric region / cellular response to fatty acid / hematopoietic stem cell proliferation / cellular hyperosmotic salinity response / telomeric DNA binding / positive regulation of catalytic activity / 2-LTR circle formation / site of DNA damage /  付加脱離酵素(リアーゼ); 炭素-酸素リアーゼ類; その他の炭素-酸素リアーゼ / 付加脱離酵素(リアーゼ); 炭素-酸素リアーゼ類; その他の炭素-酸素リアーゼ /  enzyme activator activity / 5'-deoxyribose-5-phosphate lyase activity / hematopoietic stem cell differentiation / positive regulation of protein kinase activity / ATP-dependent activity, acting on DNA / positive regulation of telomerase activity / positive regulation of telomere maintenance via telomerase / enzyme activator activity / 5'-deoxyribose-5-phosphate lyase activity / hematopoietic stem cell differentiation / positive regulation of protein kinase activity / ATP-dependent activity, acting on DNA / positive regulation of telomerase activity / positive regulation of telomere maintenance via telomerase /  DNA helicase activity / activation of innate immune response / DNA helicase activity / activation of innate immune response /  telomere maintenance / cellular response to leukemia inhibitory factor / telomere maintenance / cellular response to leukemia inhibitory factor /  神経発生 / 神経発生 /  cyclin binding / small-subunit processome / cyclin binding / small-subunit processome /  デオキシリボ核酸 / Nonhomologous End-Joining (NHEJ) / デオキシリボ核酸 / Nonhomologous End-Joining (NHEJ) /  加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与 / cellular response to gamma radiation / double-strand break repair via nonhomologous end joining / double-strand break repair / 加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与 / cellular response to gamma radiation / double-strand break repair via nonhomologous end joining / double-strand break repair /  double-stranded DNA binding / double-stranded DNA binding /  scaffold protein binding / secretory granule lumen / DNA recombination / ficolin-1-rich granule lumen / scaffold protein binding / secretory granule lumen / DNA recombination / ficolin-1-rich granule lumen /  transcription regulator complex / transcription regulator complex /  chromosome, telomeric region / damaged DNA binding / transcription cis-regulatory region binding / response to xenobiotic stimulus / chromosome, telomeric region / damaged DNA binding / transcription cis-regulatory region binding / response to xenobiotic stimulus /  ribonucleoprotein complex / ribonucleoprotein complex /  自然免疫系 / negative regulation of DNA-templated transcription / DNA damage response / 自然免疫系 / negative regulation of DNA-templated transcription / DNA damage response /  ubiquitin protein ligase binding / Neutrophil degranulation / protein-containing complex binding / ubiquitin protein ligase binding / Neutrophil degranulation / protein-containing complex binding /  核小体 / positive regulation of DNA-templated transcription / 核小体 / positive regulation of DNA-templated transcription /  ATP hydrolysis activity / positive regulation of transcription by RNA polymerase II / protein-containing complex / ATP hydrolysis activity / positive regulation of transcription by RNA polymerase II / protein-containing complex /  DNA binding / DNA binding /  RNA binding / extracellular region / RNA binding / extracellular region /  核質 / 核質 /  ATP binding / ATP binding /  生体膜 / 生体膜 /  細胞核 / 細胞核 /  細胞膜 / 細胞膜 /  細胞質基質 細胞質基質類似検索 - 分子機能 | |||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
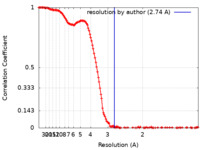
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 2.74 Å クライオ電子顕微鏡法 / 解像度: 2.74 Å | |||||||||
 データ登録者 データ登録者 | Hardwick SW / Kefala-Stavridi A / Chirgadze DY / Blundell TL / Chaplin AK | |||||||||
| 資金援助 |  英国, 1件 英国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nucleic Acids Res / 年: 2023 ジャーナル: Nucleic Acids Res / 年: 2023タイトル: Structural and functional basis of inositol hexaphosphate stimulation of NHEJ through stabilization of Ku-XLF interaction. 著者: Antonia Kefala Stavridi / Amandine Gontier / Vincent Morin / Philippe Frit / Virginie Ropars / Nadia Barboule / Carine Racca / Sagun Jonchhe / Michael J Morten / Jessica Andreani / Alexey Rak ...著者: Antonia Kefala Stavridi / Amandine Gontier / Vincent Morin / Philippe Frit / Virginie Ropars / Nadia Barboule / Carine Racca / Sagun Jonchhe / Michael J Morten / Jessica Andreani / Alexey Rak / Pierre Legrand / Alexa Bourand-Plantefol / Steven W Hardwick / Dimitri Y Chirgadze / Paul Davey / Taiana Maia De Oliveira / Eli Rothenberg / Sebastien Britton / Patrick Calsou / Tom L Blundell / Paloma F Varela / Amanda K Chaplin / Jean-Baptiste Charbonnier /    要旨: The classical Non-Homologous End Joining (c-NHEJ) pathway is the predominant process in mammals for repairing endogenous, accidental or programmed DNA Double-Strand Breaks. c-NHEJ is regulated by ...The classical Non-Homologous End Joining (c-NHEJ) pathway is the predominant process in mammals for repairing endogenous, accidental or programmed DNA Double-Strand Breaks. c-NHEJ is regulated by several accessory factors, post-translational modifications, endogenous chemical agents and metabolites. The metabolite inositol-hexaphosphate (IP6) stimulates c-NHEJ by interacting with the Ku70-Ku80 heterodimer (Ku). We report cryo-EM structures of apo- and DNA-bound Ku in complex with IP6, at 3.5 Å and 2.74 Å resolutions respectively, and an X-ray crystallography structure of a Ku in complex with DNA and IP6 at 3.7 Å. The Ku-IP6 interaction is mediated predominantly via salt bridges at the interface of the Ku70 and Ku80 subunits. This interaction is distant from the DNA, DNA-PKcs, APLF and PAXX binding sites and in close proximity to XLF binding site. Biophysical experiments show that IP6 binding increases the thermal stability of Ku by 2°C in a DNA-dependent manner, stabilizes Ku on DNA and enhances XLF affinity for Ku. In cells, selected mutagenesis of the IP6 binding pocket reduces both Ku accrual at damaged sites and XLF enrolment in the NHEJ complex, which translate into a lower end-joining efficiency. Thus, this study defines the molecular bases of the IP6 metabolite stimulatory effect on the c-NHEJ repair activity. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_14986.map.gz emd_14986.map.gz | 194.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-14986-v30.xml emd-14986-v30.xml emd-14986.xml emd-14986.xml | 20.7 KB 20.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_14986_fsc.xml emd_14986_fsc.xml | 17.4 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_14986.png emd_14986.png | 52.1 KB | ||
| Filedesc metadata |  emd-14986.cif.gz emd-14986.cif.gz | 7.1 KB | ||
| その他 |  emd_14986_half_map_1.map.gz emd_14986_half_map_1.map.gz emd_14986_half_map_2.map.gz emd_14986_half_map_2.map.gz | 194.2 MB 194.2 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-14986 http://ftp.pdbj.org/pub/emdb/structures/EMD-14986 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-14986 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-14986 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_14986.map.gz / 形式: CCP4 / 大きさ: 209.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_14986.map.gz / 形式: CCP4 / 大きさ: 209.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Ku hetero-dimer bound to DNA | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.65 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #2
| ファイル | emd_14986_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_14986_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Ku70/80 heterodimer bound to DNA
| 全体 | 名称: Ku70/80 heterodimer bound to DNA |
|---|---|
| 要素 |
|
-超分子 #1: Ku70/80 heterodimer bound to DNA
| 超分子 | 名称: Ku70/80 heterodimer bound to DNA / タイプ: organelle_or_cellular_component / ID: 1 / 親要素: 0 / 含まれる分子: #1-#4 |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 150 KDa |
-分子 #1: DNA (5'-D(P*TP*CP*CP*CP*TP*CP*TP*AP*GP*AP*TP*AP*TP*C)-3')
| 分子 | 名称: DNA (5'-D(P*TP*CP*CP*CP*TP*CP*TP*AP*GP*AP*TP*AP*TP*C)-3') タイプ: dna / ID: 1 / コピー数: 1 / 分類: DNA |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 4.190741 KDa |
| 配列 | 文字列: (DT)(DC)(DC)(DC)(DT)(DC)(DT)(DA)(DG)(DA) (DT)(DA)(DT)(DC) |
-分子 #2: DNA (5'-D(P*CP*GP*AP*TP*AP*TP*CP*TP*AP*GP*AP*GP*GP*GP*AP*T)-3')
| 分子 | 名称: DNA (5'-D(P*CP*GP*AP*TP*AP*TP*CP*TP*AP*GP*AP*GP*GP*GP*AP*T)-3') タイプ: dna / ID: 2 / コピー数: 1 / 分類: DNA |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 4.96224 KDa |
| 配列 | 文字列: (DC)(DG)(DA)(DT)(DA)(DT)(DC)(DT)(DA)(DG) (DA)(DG)(DG)(DG)(DA)(DT) |
-分子 #3: X-ray repair cross-complementing protein 6
| 分子 | 名称: X-ray repair cross-complementing protein 6 / タイプ: protein_or_peptide / ID: 3 / コピー数: 1 / 光学異性体: LEVO EC番号:  加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与 加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与 |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 69.945039 KDa |
| 組換発現 | 生物種: Insect cell expression vector pTIE1 (その他) |
| 配列 | 文字列: MSGWESYYKT EGDEEAEEEQ EENLEASGDY KYSGRDSLIF LVDASKAMFE SQSEDELTPF DMSIQCIQSV YISKIISSDR DLLAVVFYG TEKDKNSVNF KNIYVLQELD NPGAKRILEL DQFKGQQGQK RFQDMMGHGS DYSLSEVLWV CANLFSDVQF K MSHKRIML ...文字列: MSGWESYYKT EGDEEAEEEQ EENLEASGDY KYSGRDSLIF LVDASKAMFE SQSEDELTPF DMSIQCIQSV YISKIISSDR DLLAVVFYG TEKDKNSVNF KNIYVLQELD NPGAKRILEL DQFKGQQGQK RFQDMMGHGS DYSLSEVLWV CANLFSDVQF K MSHKRIML FTNEDNPHGN DSAKASRART KAGDLRDTGI FLDLMHLKKP GGFDISLFYR DIISIAEDED LRVHFEESSK LE DLLRKVR AKETRKRALS RLKLKLNKDI VISVGIYNLV QKALKPPPIK LYRETNEPVK TKTRTFNTST GGLLLPSDTK RSQ IYGSRQ IILEKEETEE LKRFDDPGLM LMGFKPLVLL KKHHYLRPSL FVYPEESLVI GSSTLFSALL IKCLEKEVAA LCRY TPRRN IPPYFVALVP QEEELDDQKI QVTPPGFQLV FLPFADDKRK MPFTEKIMAT PEQVGKMKAI VEKLRFTYRS DSFEN PVLQ QHFRNLEALA LDLMEPEQAV DLTLPKVEAM NKRLGSLVDE FKELVYPPDY NPEGKVTKRK HDNEGSGSKR PKVEYS EEE LKTHISKGTL GKFTVPMLKE ACRAYGLKSG LKKQELLEAL TKHFQD UniProtKB: X-ray repair cross-complementing protein 6 |
-分子 #4: X-ray repair cross-complementing protein 5
| 分子 | 名称: X-ray repair cross-complementing protein 5 / タイプ: protein_or_peptide / ID: 4 / コピー数: 1 / 光学異性体: LEVO EC番号:  加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与 加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与 |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 82.812438 KDa |
| 組換発現 | 生物種: Insect cell expression vector pTIE1 (その他) |
| 配列 | 文字列: MVRSGNKAAV VLCMDVGFTM SNSIPGIESP FEQAKKVITM FVQRQVFAEN KDEIALVLFG TDGTDNPLSG GDQYQNITVH RHLMLPDFD LLEDIESKIQ PGSQQADFLD ALIVSMDVIQ HETIGKKFEK RHIEIFTDLS SRFSKSQLDI IIHSLKKCDI S LQFFLPFS ...文字列: MVRSGNKAAV VLCMDVGFTM SNSIPGIESP FEQAKKVITM FVQRQVFAEN KDEIALVLFG TDGTDNPLSG GDQYQNITVH RHLMLPDFD LLEDIESKIQ PGSQQADFLD ALIVSMDVIQ HETIGKKFEK RHIEIFTDLS SRFSKSQLDI IIHSLKKCDI S LQFFLPFS LGKEDGSGDR GDGPFRLGGH GPSFPLKGIT EQQKEGLEIV KMVMISLEGE DGLDEIYSFS ESLRKLCVFK KI ERHSIHW PCRLTIGSNL SIRIAAYKSI LQERVKKTWT VVDAKTLKKE DIQKETVYCL NDDDETEVLK EDIIQGFRYG SDI VPFSKV DEEQMKYKSE GKCFSVLGFC KSSQVQRRFF MGNQVLKVFA ARDDEAAAVA LSSLIHALDD LDMVAIVRYA YDKR ANPQV GVAFPHIKHN YECLVYVQLP FMEDLRQYMF SSLKNSKKYA PTEAQLNAVD ALIDSMSLAK KDEKTDTLED LFPTT KIPN PRFQRLFQCL LHRALHPREP LPPIQQHIWN MLNPPAEVTT KSQIPLSKIK TLFPLIEAKK KDQVTAQEIF QDNHED GPT AKKLKTEQGG AHFSVSSLAE GSVTSVGSVN PAENFRVLVK QKKASFEEAS NQLINHIEQF LDTNETPYFM KSIDCIR AF REEAIKFSEE QRFNNFLKAL QEKVEIKQLN HFWEIVVQDG ITLITKEEAS GSSVTAEEAK KFLAPKDKPS GDTAAVFE E GGDVDDLLDM I UniProtKB: X-ray repair cross-complementing protein 5 |
-分子 #5: INOSITOL HEXAKISPHOSPHATE
| 分子 | 名称: INOSITOL HEXAKISPHOSPHATE / タイプ: ligand / ID: 5 / コピー数: 1 / 式: IHP |
|---|---|
| 分子量 | 理論値: 660.035 Da |
| Chemical component information | 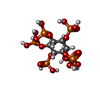 ChemComp-IHP: |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 2 mg/mL |
|---|---|
| 緩衝液 | pH: 8 |
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.6 µm / 最小 デフォーカス(公称値): 0.8 µm / 倍率(公称値): 130000 Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.6 µm / 最小 デフォーカス(公称値): 0.8 µm / 倍率(公称値): 130000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 撮影したグリッド数: 1 / 実像数: 6924 / 平均露光時間: 1.25 sec. / 平均電子線量: 44.39 e/Å2 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー
















 X (Sec.)
X (Sec.) Y (Row.)
Y (Row.) Z (Col.)
Z (Col.)