+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-1438 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Architecture of the yeast Rrp44 exosome complex suggests routes of RNA recruitment for 3' end processing. | |||||||||
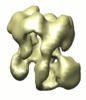
 マップデータ マップデータ | This is the map of yeast Rrp44-associated exosome complex | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |   Saccharomyces cerevisiae (パン酵母) Saccharomyces cerevisiae (パン酵母) | |||||||||
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / クライオ電子顕微鏡法 /  ネガティブ染色法 / 解像度: 19.0 Å ネガティブ染色法 / 解像度: 19.0 Å | |||||||||
 データ登録者 データ登録者 | Wang H-W / Wang J / Ding F / Callahan K / Bratkowski MA / Butler JS / Nogales E / Ke A | |||||||||
 引用 引用 |  ジャーナル: Proc Natl Acad Sci U S A / 年: 2007 ジャーナル: Proc Natl Acad Sci U S A / 年: 2007タイトル: Architecture of the yeast Rrp44 exosome complex suggests routes of RNA recruitment for 3' end processing. 著者: Hong-Wei Wang / Jianjun Wang / Fang Ding / Kevin Callahan / Matthew A Bratkowski / J Scott Butler / Eva Nogales / Ailong Ke /  要旨: The eukaryotic core exosome (CE) is a conserved nine-subunit protein complex important for 3' end trimming and degradation of RNA. In yeast, the Rrp44 protein constitutively associates with the CE ...The eukaryotic core exosome (CE) is a conserved nine-subunit protein complex important for 3' end trimming and degradation of RNA. In yeast, the Rrp44 protein constitutively associates with the CE and provides the sole source of processive 3'-to-5' exoribonuclease activity. Here we present EM reconstructions of the core and Rrp44-bound exosome complexes. The two-lobed Rrp44 protein binds to the RNase PH domain side of the exosome and buttresses the bottom of the exosome-processing chamber. The Rrp44 C-terminal body part containing an RNase II-type active site is anchored to the exosome through a conserved set of interactions mainly to the Rrp45 and Rrp43 subunit, whereas the Rrp44 N-terminal head part is anchored to the Rrp41 subunit and may function as a roadblock to restrict access of RNA to the active site in the body region. The Rrp44-exosome (RE) architecture suggests an active site sequestration mechanism for strict control of 3' exoribonuclease activity in the RE complex. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_1438.map.gz emd_1438.map.gz | 1.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-1438-v30.xml emd-1438-v30.xml emd-1438.xml emd-1438.xml | 17.3 KB 17.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  1438.gif 1438.gif | 62.8 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-1438 http://ftp.pdbj.org/pub/emdb/structures/EMD-1438 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1438 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1438 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_1438.map.gz / 形式: CCP4 / 大きさ: 1.4 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_1438.map.gz / 形式: CCP4 / 大きさ: 1.4 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | This is the map of yeast Rrp44-associated exosome complex | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
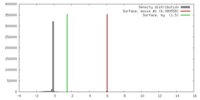
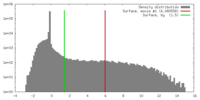
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 5.18 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
+全体 : Rrp44-associated exosome complex
+超分子 #1000: Rrp44-associated exosome complex
+分子 #1: Rrp44
+分子 #2: Rrp43
+分子 #3: Rrp4
+分子 #4: Csl4
+分子 #5: Rrp45
+分子 #6: Rrp46-TAP
+分子 #7: Rrp41
+分子 #8: Rrp42
+分子 #9: Mtr3
+分子 #10: Rrp40
-実験情報
-構造解析
| 手法 |  ネガティブ染色法, ネガティブ染色法,  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.04 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 詳細: 25mM Tris-HCl, 50 mM NaCl, 2 mM DTT, and 10 uM ZnCl2 |
| 染色 | タイプ: NEGATIVE 詳細: Four microliters of the protein solution was negatively stained with 2% uranyl formate solution between two thin layers of carbon on a copper grid by using the sandwich method |
| グリッド | 詳細: 400 mesh copper grid |
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI 12 |
|---|---|
| 電子線 | 加速電圧: 120 kV / 電子線源: LAB6 |
| 電子光学系 | 倍率(補正後): 49000 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 6.6 mm / 最大 デフォーカス(公称値): 0.9 µm / 最小 デフォーカス(公称値): 0.7 µm / 倍率(公称値): 49000 Bright-field microscopy / Cs: 6.6 mm / 最大 デフォーカス(公称値): 0.9 µm / 最小 デフォーカス(公称値): 0.7 µm / 倍率(公称値): 49000 |
| 試料ステージ | 試料ホルダー: normal single-tilt holder / 試料ホルダーモデル: OTHER / Tilt angle max: 55 |
| 温度 | 平均: 300 K |
| アライメント法 | Legacy - 非点収差: objective lens astigmatism was corrected at |
| 詳細 | Low dose mode for taking pictures |
| 日付 | 2006年8月1日 |
| 撮影 | カテゴリ: FILM / フィルム・検出器のモデル: KODAK SO-163 FILM / デジタル化 - スキャナー: OTHER / デジタル化 - サンプリング間隔: 12.7 µm / 実像数: 50 / 平均電子線量: 20 e/Å2 / 詳細: The scanner was Nikon Super Coolscan 8000 / Od range: 1.4 / ビット/ピクセル: 14 |
| Tilt angle min | 0 |
- 画像解析
画像解析
| 最終 2次元分類 | クラス数: 50 |
|---|---|
| 最終 角度割当 | 詳細: SPIDER: theta 90 degrees, phi 90 degrees |
| 最終 再構成 | 想定した対称性 - 点群: C1 (非対称) / アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 19.0 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ソフトウェア - 名称: IMAGIC, SPIDER 詳細: Final map were calculated from all the untilted particles 使用した粒子像数: 3020 |
-原子モデル構築 1
| ソフトウェア | 名称: Situs |
|---|---|
| 詳細 | Protocol: Rigid Body. 2NN6.pdb and 2IX0.pdb were used to dock in the map. The latter one was separated to three domains after the automatic docking and manually adjusted to fit in the map locally in Chimera. |
| 精密化 | プロトコル: RIGID BODY FIT |
 ムービー
ムービー コントローラー
コントローラー












 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)