+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 7fjp | ||||||
|---|---|---|---|---|---|---|---|
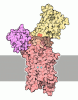
| タイトル | Cryo EM structure of lysosomal ATPase | ||||||
 要素 要素 | Polyamine-transporting ATPase 13A2 | ||||||
 キーワード キーワード |  MEMBRANE PROTEIN (膜タンパク質) / lysosomal ATPase transporter MEMBRANE PROTEIN (膜タンパク質) / lysosomal ATPase transporter | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報polyamine transmembrane transporter activity / ABC-type polyamine transporter activity / polyamine transmembrane transport / spermine transmembrane transport / peptidyl-aspartic acid autophosphorylation / regulation of ubiquitin-specific protease activity / regulation of autophagosome size / extracellular exosome biogenesis /  regulation of chaperone-mediated autophagy / P-type ion transporter activity ...polyamine transmembrane transporter activity / ABC-type polyamine transporter activity / polyamine transmembrane transport / spermine transmembrane transport / peptidyl-aspartic acid autophosphorylation / regulation of ubiquitin-specific protease activity / regulation of autophagosome size / extracellular exosome biogenesis / regulation of chaperone-mediated autophagy / P-type ion transporter activity ...polyamine transmembrane transporter activity / ABC-type polyamine transporter activity / polyamine transmembrane transport / spermine transmembrane transport / peptidyl-aspartic acid autophosphorylation / regulation of ubiquitin-specific protease activity / regulation of autophagosome size / extracellular exosome biogenesis /  regulation of chaperone-mediated autophagy / P-type ion transporter activity / negative regulation of lysosomal protein catabolic process / regulation of chaperone-mediated autophagy / P-type ion transporter activity / negative regulation of lysosomal protein catabolic process /  regulation of lysosomal protein catabolic process / autophagosome-lysosome fusion / intracellular monoatomic cation homeostasis / regulation of autophagy of mitochondrion / autophagosome organization / protein localization to lysosome / regulation of lysosomal protein catabolic process / autophagosome-lysosome fusion / intracellular monoatomic cation homeostasis / regulation of autophagy of mitochondrion / autophagosome organization / protein localization to lysosome /  phosphatidic acid binding / multivesicular body membrane / positive regulation of exosomal secretion / ATPase-coupled monoatomic cation transmembrane transporter activity / intracellular zinc ion homeostasis / トランスロカーゼ; 他の化合物の輸送を触媒; ヌクレオシド三リン酸の加水分解に伴う / regulation of protein localization to nucleus / cupric ion binding / phosphatidylinositol-3,5-bisphosphate binding / regulation of mitochondrion organization / phosphatidic acid binding / multivesicular body membrane / positive regulation of exosomal secretion / ATPase-coupled monoatomic cation transmembrane transporter activity / intracellular zinc ion homeostasis / トランスロカーゼ; 他の化合物の輸送を触媒; ヌクレオシド三リン酸の加水分解に伴う / regulation of protein localization to nucleus / cupric ion binding / phosphatidylinositol-3,5-bisphosphate binding / regulation of mitochondrion organization /  regulation of endopeptidase activity / lysosomal transport / cellular response to zinc ion / regulation of endopeptidase activity / lysosomal transport / cellular response to zinc ion /  regulation of intracellular protein transport / lipid homeostasis / autophagosome membrane / Ion transport by P-type ATPases / regulation of intracellular protein transport / lipid homeostasis / autophagosome membrane / Ion transport by P-type ATPases /  オートファゴソーム / オートファゴソーム /  regulation of macroautophagy / cellular response to manganese ion / regulation of neuron apoptotic process / regulation of macroautophagy / cellular response to manganese ion / regulation of neuron apoptotic process /  小胞 / 小胞 /  エンドソーム / lysosomal lumen / monoatomic ion transmembrane transport / positive regulation of protein secretion / transmembrane transport / intracellular calcium ion homeostasis / エンドソーム / lysosomal lumen / monoatomic ion transmembrane transport / positive regulation of protein secretion / transmembrane transport / intracellular calcium ion homeostasis /  オートファジー / late endosome / cellular response to oxidative stress / late endosome membrane / manganese ion binding / intracellular iron ion homeostasis / vesicle / protein autophosphorylation / オートファジー / late endosome / cellular response to oxidative stress / late endosome membrane / manganese ion binding / intracellular iron ion homeostasis / vesicle / protein autophosphorylation /  リソソーム / neuron projection / lysosomal membrane / neuronal cell body / positive regulation of gene expression / リソソーム / neuron projection / lysosomal membrane / neuronal cell body / positive regulation of gene expression /  ATP hydrolysis activity / zinc ion binding / ATP hydrolysis activity / zinc ion binding /  ATP binding / ATP binding /  生体膜 生体膜類似検索 - 分子機能 | ||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||
| 手法 |  電子顕微鏡法 / 電子顕微鏡法 /  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 3 Å クライオ電子顕微鏡法 / 解像度: 3 Å | ||||||
 データ登録者 データ登録者 | Zhang, S.S. | ||||||
| 資金援助 |  中国, 1件 中国, 1件
| ||||||
 引用 引用 |  ジャーナル: Cell Discov / 年: 2021 ジャーナル: Cell Discov / 年: 2021タイトル: Cryo-EM structures and transport mechanism of human P5B type ATPase ATP13A2. 著者: Xudong Chen / Mingze Zhou / Sensen Zhang / Jian Yin / Ping Zhang / Xujun Xuan / Peiyi Wang / Zhiqiang Liu / Boda Zhou / Maojun Yang /  要旨: Polyamines are important polycations that play critical roles in mammalian cells. ATP13A2 belongs to the orphan P5B adenosine triphosphatases (ATPase) family and has been established as a lysosomal ...Polyamines are important polycations that play critical roles in mammalian cells. ATP13A2 belongs to the orphan P5B adenosine triphosphatases (ATPase) family and has been established as a lysosomal polyamine exporter to maintain the normal function of lysosomes and mitochondria. Previous studies have reported that several human neurodegenerative disorders are related to mutations in the ATP13A2 gene. However, the transport mechanism of ATP13A2 in the lysosome remains unclear. Here, we report the cryo-electron microscopy (cryo-EM) structures of three distinct intermediates of the human ATP13A2, revealing key insights into the spermine (SPM) transport cycle in the lysosome. The transmembrane domain serves as a substrate binding site and the C-terminal domain is essential for protein stability and may play a regulatory role. These findings advance our understanding of the polyamine transport mechanism, the lipid-associated regulation, and the disease-associated mutants of ATP13A2. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  7fjp.cif.gz 7fjp.cif.gz | 175.7 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb7fjp.ent.gz pdb7fjp.ent.gz | 135.7 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  7fjp.json.gz 7fjp.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/fj/7fjp https://data.pdbj.org/pub/pdb/validation_reports/fj/7fjp ftp://data.pdbj.org/pub/pdb/validation_reports/fj/7fjp ftp://data.pdbj.org/pub/pdb/validation_reports/fj/7fjp | HTTPS FTP |
|---|
-関連構造データ
| 関連構造データ |  31626MC  7fjmC  7fjqC M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 125239.844 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   Homo sapiens (ヒト) / 遺伝子: ATP13A2 / 細胞株 (発現宿主): HEK293 / 発現宿主: Homo sapiens (ヒト) / 遺伝子: ATP13A2 / 細胞株 (発現宿主): HEK293 / 発現宿主:   Homo sapiens (ヒト) Homo sapiens (ヒト)参照: UniProt: Q9NQ11, トランスロカーゼ; 他の化合物の輸送を触媒; ヌクレオシド三リン酸の加水分解に伴う | ||
|---|---|---|---|
| #2: 化合物 | ChemComp-PO4 /  リン酸塩 リン酸塩 | ||
| #3: 化合物 | ChemComp-ADP /  アデノシン二リン酸 アデノシン二リン酸 | ||
| #4: 化合物 | | 研究の焦点であるリガンドがあるか | N | |
-実験情報
-実験
| 実験 | 手法:  電子顕微鏡法 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法:  単粒子再構成法 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: lysosomal ATPase E1p_ADP / タイプ: ORGANELLE OR CELLULAR COMPONENT / Entity ID: #1 / 由来: RECOMBINANT |
|---|---|
| 分子量 | 実験値: NO |
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 由来(組換発現) | 生物種:   Homo sapiens (ヒト) / 細胞: HEK293 Homo sapiens (ヒト) / 細胞: HEK293 |
| 緩衝液 | pH: 7.2 |
| 試料 | 包埋: NO / シャドウイング: NO / 染色 : NO / 凍結 : NO / 凍結 : YES : YES |
急速凍結 | 凍結剤: ETHANE |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源 : :  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD Bright-field microscopy Bright-field microscopy |
| 撮影 | 電子線照射量: 50 e/Å2 フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) |
- 解析
解析
CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION |
|---|---|
3次元再構成 | 解像度: 3 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 317000 / 対称性のタイプ: POINT |
 ムービー
ムービー コントローラー
コントローラー





 PDBj
PDBj