| 登録情報 | データベース: PDB / ID: 6a9e
|
|---|
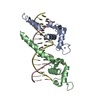
| タイトル | Crystal structure of the N-terminal domain of Atg2 |
|---|
 要素 要素 | Endolysin,Autophagy-related protein 2 |
|---|
 キーワード キーワード | LIPID TRANSPORT |
|---|
| 機能・相同性 |  機能・相同性情報 機能・相同性情報
: / lipid transfer activity / intermembrane lipid transfer / autophagy of mitochondrion / phagophore assembly site membrane / piecemeal microautophagy of the nucleus /  phosphatidylinositol-3-phosphate binding / phagophore assembly site / reticulophagy / phosphatidylinositol-3-phosphate binding / phagophore assembly site / reticulophagy /  extrinsic component of membrane ...: / lipid transfer activity / intermembrane lipid transfer / autophagy of mitochondrion / phagophore assembly site membrane / piecemeal microautophagy of the nucleus / extrinsic component of membrane ...: / lipid transfer activity / intermembrane lipid transfer / autophagy of mitochondrion / phagophore assembly site membrane / piecemeal microautophagy of the nucleus /  phosphatidylinositol-3-phosphate binding / phagophore assembly site / reticulophagy / phosphatidylinositol-3-phosphate binding / phagophore assembly site / reticulophagy /  extrinsic component of membrane / sporulation resulting in formation of a cellular spore / extrinsic component of membrane / sporulation resulting in formation of a cellular spore /  autophagosome assembly / viral release from host cell by cytolysis / peptidoglycan catabolic process / meiotic cell cycle / autophagosome assembly / viral release from host cell by cytolysis / peptidoglycan catabolic process / meiotic cell cycle /  オートファジー / オートファジー /  オートファジー / cell wall macromolecule catabolic process / オートファジー / cell wall macromolecule catabolic process /  リゾチーム / リゾチーム /  lysozyme activity / host cell cytoplasm / defense response to bacterium / endoplasmic reticulum membrane類似検索 - 分子機能 lysozyme activity / host cell cytoplasm / defense response to bacterium / endoplasmic reticulum membrane類似検索 - 分子機能 Autophagy-related protein 2, CAD motif / Autophagy-related protein 2, middle RBG modules / Autophagy-related protein 2/VPS13, C-terminal / Autophagy-related protein 2 / ATG2/VPS13, C terminal domain /  Vacuolar protein sorting-associated protein 13-like, N-terminal domain / VPS13-like, N-terminal / Endolysin T4 type / T4-type lysozyme / Vacuolar protein sorting-associated protein 13-like, N-terminal domain / VPS13-like, N-terminal / Endolysin T4 type / T4-type lysozyme /  Glycoside hydrolase, family 24 ...Autophagy-related protein 2, CAD motif / Autophagy-related protein 2, middle RBG modules / Autophagy-related protein 2/VPS13, C-terminal / Autophagy-related protein 2 / ATG2/VPS13, C terminal domain / Glycoside hydrolase, family 24 ...Autophagy-related protein 2, CAD motif / Autophagy-related protein 2, middle RBG modules / Autophagy-related protein 2/VPS13, C-terminal / Autophagy-related protein 2 / ATG2/VPS13, C terminal domain /  Vacuolar protein sorting-associated protein 13-like, N-terminal domain / VPS13-like, N-terminal / Endolysin T4 type / T4-type lysozyme / Vacuolar protein sorting-associated protein 13-like, N-terminal domain / VPS13-like, N-terminal / Endolysin T4 type / T4-type lysozyme /  Glycoside hydrolase, family 24 / Lysozyme domain superfamily / Phage lysozyme / Lysozyme-like domain superfamily類似検索 - ドメイン・相同性 Glycoside hydrolase, family 24 / Lysozyme domain superfamily / Phage lysozyme / Lysozyme-like domain superfamily類似検索 - ドメイン・相同性  Endolysin / Autophagy-related protein 2 / Endolysin / Autophagy-related protein 2 /  Endolysin類似検索 - 構成要素 Endolysin類似検索 - 構成要素 |
|---|
| 生物種 |  Enterobacteria phage RB59 (ファージ) Enterobacteria phage RB59 (ファージ)
   Schizosaccharomyces pombe (分裂酵母) Schizosaccharomyces pombe (分裂酵母) |
|---|
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  単波長異常分散 / 解像度: 3.205 Å 単波長異常分散 / 解像度: 3.205 Å |
|---|
 データ登録者 データ登録者 | Osawa, T. / Noda, N.N. |
|---|
 引用 引用 |  ジャーナル: Nat. Struct. Mol. Biol. / 年: 2019 ジャーナル: Nat. Struct. Mol. Biol. / 年: 2019
タイトル: Atg2 mediates direct lipid transfer between membranes for autophagosome formation.
著者: Osawa, T. / Kotani, T. / Kawaoka, T. / Hirata, E. / Suzuki, K. / Nakatogawa, H. / Ohsumi, Y. / Noda, N.N. |
|---|
| 履歴 | | 登録 | 2018年7月13日 | 登録サイト: PDBJ / 処理サイト: PDBJ |
|---|
| 改定 1.0 | 2019年3月20日 | Provider: repository / タイプ: Initial release |
|---|
| 改定 1.1 | 2019年3月27日 | Group: Data collection / Database references / カテゴリ: citation / citation_author
Item: _citation.country / _citation.journal_abbrev ..._citation.country / _citation.journal_abbrev / _citation.journal_id_CSD / _citation.journal_id_ISSN / _citation.title |
|---|
| 改定 1.2 | 2019年4月10日 | Group: Data collection / Database references / カテゴリ: citation / citation_author
Item: _citation.journal_abbrev / _citation.pdbx_database_id_PubMed / _citation.title |
|---|
| 改定 1.3 | 2019年4月17日 | Group: Data collection / Database references / カテゴリ: citation
Item: _citation.journal_volume / _citation.page_first / _citation.page_last |
|---|
|
|---|
 データを開く
データを開く 基本情報
基本情報 要素
要素 キーワード
キーワード 機能・相同性情報
機能・相同性情報 phosphatidylinositol-3-phosphate binding / phagophore assembly site / reticulophagy /
phosphatidylinositol-3-phosphate binding / phagophore assembly site / reticulophagy /  extrinsic component of membrane ...: / lipid transfer activity / intermembrane lipid transfer / autophagy of mitochondrion / phagophore assembly site membrane / piecemeal microautophagy of the nucleus /
extrinsic component of membrane ...: / lipid transfer activity / intermembrane lipid transfer / autophagy of mitochondrion / phagophore assembly site membrane / piecemeal microautophagy of the nucleus /  phosphatidylinositol-3-phosphate binding / phagophore assembly site / reticulophagy /
phosphatidylinositol-3-phosphate binding / phagophore assembly site / reticulophagy /  extrinsic component of membrane / sporulation resulting in formation of a cellular spore /
extrinsic component of membrane / sporulation resulting in formation of a cellular spore /  autophagosome assembly / viral release from host cell by cytolysis / peptidoglycan catabolic process / meiotic cell cycle /
autophagosome assembly / viral release from host cell by cytolysis / peptidoglycan catabolic process / meiotic cell cycle /  オートファジー /
オートファジー /  オートファジー / cell wall macromolecule catabolic process /
オートファジー / cell wall macromolecule catabolic process /  リゾチーム /
リゾチーム /  lysozyme activity / host cell cytoplasm / defense response to bacterium / endoplasmic reticulum membrane
lysozyme activity / host cell cytoplasm / defense response to bacterium / endoplasmic reticulum membrane Enterobacteria phage RB59 (ファージ)
Enterobacteria phage RB59 (ファージ)
 Schizosaccharomyces pombe (分裂酵母)
Schizosaccharomyces pombe (分裂酵母) X線回折 /
X線回折 /  シンクロトロン /
シンクロトロン /  単波長異常分散 / 解像度: 3.205 Å
単波長異常分散 / 解像度: 3.205 Å  データ登録者
データ登録者 引用
引用 ジャーナル: Nat. Struct. Mol. Biol. / 年: 2019
ジャーナル: Nat. Struct. Mol. Biol. / 年: 2019 構造の表示
構造の表示 Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク ダウンロード
ダウンロード 6a9e.cif.gz
6a9e.cif.gz PDBx/mmCIF形式
PDBx/mmCIF形式 pdb6a9e.ent.gz
pdb6a9e.ent.gz PDB形式
PDB形式 6a9e.json.gz
6a9e.json.gz PDBx/mmJSON形式
PDBx/mmJSON形式 その他のダウンロード
その他のダウンロード https://data.pdbj.org/pub/pdb/validation_reports/a9/6a9e
https://data.pdbj.org/pub/pdb/validation_reports/a9/6a9e ftp://data.pdbj.org/pub/pdb/validation_reports/a9/6a9e
ftp://data.pdbj.org/pub/pdb/validation_reports/a9/6a9e リンク
リンク 集合体
集合体


 要素
要素 Enterobacteria phage RB59 (ファージ), (組換発現)
Enterobacteria phage RB59 (ファージ), (組換発現) 
 Schizosaccharomyces pombe (strain 972 / ATCC 24843) (分裂酵母)
Schizosaccharomyces pombe (strain 972 / ATCC 24843) (分裂酵母)
 Escherichia coli (大腸菌)
Escherichia coli (大腸菌) リゾチーム
リゾチーム X線回折 / 使用した結晶の数: 1
X線回折 / 使用した結晶の数: 1  試料調製
試料調製
 シンクロトロン / サイト:
シンクロトロン / サイト:  Photon Factory
Photon Factory  / ビームライン: BL-1A / 波長: 0.9692 Å
/ ビームライン: BL-1A / 波長: 0.9692 Å : 0.9692 Å / 相対比: 1
: 0.9692 Å / 相対比: 1  解析
解析 :
:  単波長異常分散 / 解像度: 3.205→44.103 Å / 交差検証法: FREE R-VALUE / σ(F): 0.65 / 位相誤差: 26.34
単波長異常分散 / 解像度: 3.205→44.103 Å / 交差検証法: FREE R-VALUE / σ(F): 0.65 / 位相誤差: 26.34  ムービー
ムービー コントローラー
コントローラー













 PDBj
PDBj




