[English] 日本語
 Yorodumi
Yorodumi- PDB-5eqr: Crystal structure of a genotype 1a/3a chimeric HCV NS3/4A proteas... -
+ Open data
Open data
- Basic information
Basic information
| Entry | Database: PDB / ID: 5eqr | ||||||
|---|---|---|---|---|---|---|---|
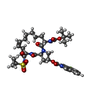
| Title | Crystal structure of a genotype 1a/3a chimeric HCV NS3/4A protease in complex with danoprevir | ||||||
 Components Components | NS3 protease | ||||||
 Keywords Keywords | HYDROLASE/HYDROLASE Inhibitor /  danoprevir / danoprevir /  drug resistance / drug resistance /  HCV protease inhibitor / HCV protease inhibitor /  genotype 3 / genotype 3 /  HYDROLASE / HYDROLASE-HYDROLASE Inhibitor complex HYDROLASE / HYDROLASE-HYDROLASE Inhibitor complex | ||||||
| Function / homology |  Function and homology information Function and homology informationtransformation of host cell by virus / host cell membrane / serine-type peptidase activity /  virion component / symbiont entry into host cell / virion attachment to host cell / virion component / symbiont entry into host cell / virion attachment to host cell /  proteolysis / proteolysis /  membrane / membrane /  metal ion binding metal ion bindingSimilarity search - Function | ||||||
| Biological species |  Hepatitis C virus Hepatitis C virus | ||||||
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  MOLECULAR REPLACEMENT / MOLECULAR REPLACEMENT /  molecular replacement / Resolution: 1.96 Å molecular replacement / Resolution: 1.96 Å | ||||||
 Authors Authors | Soumana, D. / Yilmaz, N.K. / Ali, A. / Prachanronarong, K.L. / Schiffer, C.A. | ||||||
| Funding support |  United States, 1items United States, 1items
| ||||||
 Citation Citation |  Journal: J.Am.Chem.Soc. / Year: 2016 Journal: J.Am.Chem.Soc. / Year: 2016Title: Molecular and Dynamic Mechanism Underlying Drug Resistance in Genotype 3 Hepatitis C NS3/4A Protease. Authors: Soumana, D.I. / Kurt Yilmaz, N. / Ali, A. / Prachanronarong, K.L. / Schiffer, C.A. #1:  Journal: PLoS Pathog. / Year: 2012 Journal: PLoS Pathog. / Year: 2012Title: The molecular basis of drug resistance against hepatitis C virus NS3/4A protease inhibitors. Authors: Romano, K.P. / Ali, A. / Aydin, C. / Soumana, D. / Ozen, A. / Deveau, L.M. / Silver, C. / Cao, H. / Newton, A. / Petropoulos, C.J. / Huang, W. / Schiffer, C.A. | ||||||
| History |
|
- Structure visualization
Structure visualization
| Structure viewer | Molecule:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- Downloads & links
Downloads & links
- Download
Download
| PDBx/mmCIF format |  5eqr.cif.gz 5eqr.cif.gz | 124.8 KB | Display |  PDBx/mmCIF format PDBx/mmCIF format |
|---|---|---|---|---|
| PDB format |  pdb5eqr.ent.gz pdb5eqr.ent.gz | 96.2 KB | Display |  PDB format PDB format |
| PDBx/mmJSON format |  5eqr.json.gz 5eqr.json.gz | Tree view |  PDBx/mmJSON format PDBx/mmJSON format | |
| Others |  Other downloads Other downloads |
-Validation report
| Arichive directory |  https://data.pdbj.org/pub/pdb/validation_reports/eq/5eqr https://data.pdbj.org/pub/pdb/validation_reports/eq/5eqr ftp://data.pdbj.org/pub/pdb/validation_reports/eq/5eqr ftp://data.pdbj.org/pub/pdb/validation_reports/eq/5eqr | HTTPS FTP |
|---|
-Related structure data
- Links
Links
- Assembly
Assembly
| Deposited unit | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||
| Unit cell |
|
- Components
Components
| #1: Protein | Mass: 20974.764 Da / Num. of mol.: 1 Source method: isolated from a genetically manipulated source Source: (gene. exp.)  Hepatitis C virus / Plasmid: pET28-a / Production host: Hepatitis C virus / Plasmid: pET28-a / Production host:   Escherichia coli (E. coli) / Strain (production host): BL21-DE3 / References: UniProt: C1KIK8, UniProt: A0A0B4WYC6*PLUS Escherichia coli (E. coli) / Strain (production host): BL21-DE3 / References: UniProt: C1KIK8, UniProt: A0A0B4WYC6*PLUS |
|---|---|
| #2: Chemical | ChemComp-TSV / ( Danoprevir Danoprevir |
| #3: Chemical | ChemComp-ZN / |
| #4: Chemical | ChemComp-SO4 /  Sulfate Sulfate |
| #5: Water | ChemComp-HOH /  Water Water |
-Experimental details
-Experiment
| Experiment | Method:  X-RAY DIFFRACTION / Number of used crystals: 1 X-RAY DIFFRACTION / Number of used crystals: 1 |
|---|
- Sample preparation
Sample preparation
| Crystal | Density Matthews: 2.3 Å3/Da / Density % sol: 46.5 % |
|---|---|
Crystal grow | Temperature: 298 K / Method: vapor diffusion, hanging drop / pH: 6.5 Details: 100mM MES buffer pH 6.5, 4% (w/v) ammonium sulfate, 20-26% PEG 3350 |
-Data collection
| Diffraction | Mean temperature: 100 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Diffraction source | Source:  ROTATING ANODE / Type: RIGAKU / Wavelength: 1.5 Å ROTATING ANODE / Type: RIGAKU / Wavelength: 1.5 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Detector | Type: RIGAKU SATURN 944 / Detector: CCD / Date: Feb 13, 2014 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radiation | Protocol: SINGLE WAVELENGTH / Monochromatic (M) / Laue (L): M / Scattering type: x-ray | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radiation wavelength | Wavelength : 1.5 Å / Relative weight: 1 : 1.5 Å / Relative weight: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection | Resolution: 1.96→50 Å / Num. obs: 14041 / % possible obs: 96.8 % / Redundancy: 4.3 % / Rmerge(I) obs: 0.09 / Χ2: 1.071 / Net I/av σ(I): 15.779 / Net I/σ(I): 7.7 / Num. measured all: 60292 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection shell | Diffraction-ID: 1 / Rejects: 0
|
-Phasing
Phasing | Method:  molecular replacement molecular replacement | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Phasing MR |
|
- Processing
Processing
| Software |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Refinement | Method to determine structure : :  MOLECULAR REPLACEMENT / Resolution: 1.96→26.328 Å / FOM work R set: 0.8627 / SU ML: 0.19 / Cross valid method: FREE R-VALUE / σ(F): 0 / Phase error: 19.38 / Stereochemistry target values: ML MOLECULAR REPLACEMENT / Resolution: 1.96→26.328 Å / FOM work R set: 0.8627 / SU ML: 0.19 / Cross valid method: FREE R-VALUE / σ(F): 0 / Phase error: 19.38 / Stereochemistry target values: ML
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solvent computation | Shrinkage radii: 0.9 Å / VDW probe radii: 1.11 Å / Solvent model: FLAT BULK SOLVENT MODEL | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Displacement parameters | Biso max: 162.06 Å2 / Biso mean: 24.97 Å2 / Biso min: 7.74 Å2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement step | Cycle: final / Resolution: 1.96→26.328 Å
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS refinement shell | Refine-ID: X-RAY DIFFRACTION
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS params. | Method: refined / Refine-ID: X-RAY DIFFRACTION
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS group |
|
 Movie
Movie Controller
Controller















 PDBj
PDBj