+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1y16 | ||||||
|---|---|---|---|---|---|---|---|
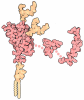
| タイトル | mouse prion protein with mutations S170N and N174T | ||||||
 要素 要素 | Major prion protein | ||||||
 キーワード キーワード | UNKNOWN FUNCTION /  prion protein / PrP / prion protein / PrP /  PrnP / TSE / CWD PrnP / TSE / CWD | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報Insertion of tail-anchored proteins into the endoplasmic reticulum membrane / negative regulation of amyloid precursor protein catabolic process /  lamin binding / regulation of glutamate receptor signaling pathway / regulation of calcium ion import across plasma membrane / aspartic-type endopeptidase inhibitor activity / lamin binding / regulation of glutamate receptor signaling pathway / regulation of calcium ion import across plasma membrane / aspartic-type endopeptidase inhibitor activity /  glycosaminoglycan binding / ATP-dependent protein binding / regulation of potassium ion transmembrane transport / negative regulation of interleukin-17 production ...Insertion of tail-anchored proteins into the endoplasmic reticulum membrane / negative regulation of amyloid precursor protein catabolic process / glycosaminoglycan binding / ATP-dependent protein binding / regulation of potassium ion transmembrane transport / negative regulation of interleukin-17 production ...Insertion of tail-anchored proteins into the endoplasmic reticulum membrane / negative regulation of amyloid precursor protein catabolic process /  lamin binding / regulation of glutamate receptor signaling pathway / regulation of calcium ion import across plasma membrane / aspartic-type endopeptidase inhibitor activity / lamin binding / regulation of glutamate receptor signaling pathway / regulation of calcium ion import across plasma membrane / aspartic-type endopeptidase inhibitor activity /  glycosaminoglycan binding / ATP-dependent protein binding / regulation of potassium ion transmembrane transport / negative regulation of interleukin-17 production / negative regulation of dendritic spine maintenance / type 5 metabotropic glutamate receptor binding / cupric ion binding / nucleobase-containing compound metabolic process / response to copper ion / negative regulation of calcineurin-NFAT signaling cascade / negative regulation of interleukin-2 production / negative regulation of T cell receptor signaling pathway / activation of protein kinase activity / cuprous ion binding / negative regulation of amyloid-beta formation / negative regulation of activated T cell proliferation / response to amyloid-beta / : / negative regulation of type II interferon production / intracellular copper ion homeostasis / negative regulation of long-term synaptic potentiation / positive regulation of protein targeting to membrane / side of membrane / response to cadmium ion / regulation of peptidyl-tyrosine phosphorylation / glycosaminoglycan binding / ATP-dependent protein binding / regulation of potassium ion transmembrane transport / negative regulation of interleukin-17 production / negative regulation of dendritic spine maintenance / type 5 metabotropic glutamate receptor binding / cupric ion binding / nucleobase-containing compound metabolic process / response to copper ion / negative regulation of calcineurin-NFAT signaling cascade / negative regulation of interleukin-2 production / negative regulation of T cell receptor signaling pathway / activation of protein kinase activity / cuprous ion binding / negative regulation of amyloid-beta formation / negative regulation of activated T cell proliferation / response to amyloid-beta / : / negative regulation of type II interferon production / intracellular copper ion homeostasis / negative regulation of long-term synaptic potentiation / positive regulation of protein targeting to membrane / side of membrane / response to cadmium ion / regulation of peptidyl-tyrosine phosphorylation /  封入体 / cellular response to copper ion / neuron projection maintenance / protein sequestering activity / 封入体 / cellular response to copper ion / neuron projection maintenance / protein sequestering activity /  tubulin binding / negative regulation of protein phosphorylation / molecular condensate scaffold activity / molecular function activator activity / positive regulation of protein localization to plasma membrane / protein destabilization / protein homooligomerization / negative regulation of DNA-binding transcription factor activity / tubulin binding / negative regulation of protein phosphorylation / molecular condensate scaffold activity / molecular function activator activity / positive regulation of protein localization to plasma membrane / protein destabilization / protein homooligomerization / negative regulation of DNA-binding transcription factor activity /  terminal bouton / cellular response to amyloid-beta / terminal bouton / cellular response to amyloid-beta /  regulation of protein localization / positive regulation of peptidyl-tyrosine phosphorylation / positive regulation of neuron apoptotic process / cellular response to xenobiotic stimulus / regulation of protein localization / positive regulation of peptidyl-tyrosine phosphorylation / positive regulation of neuron apoptotic process / cellular response to xenobiotic stimulus /  signaling receptor activity / signaling receptor activity /  amyloid-beta binding / protein-folding chaperone binding / amyloid-beta binding / protein-folding chaperone binding /  microtubule binding / microtubule binding /  核膜 / 核膜 /  protease binding / response to oxidative stress / mitochondrial outer membrane / transmembrane transporter binding / protease binding / response to oxidative stress / mitochondrial outer membrane / transmembrane transporter binding /  postsynaptic density / molecular adaptor activity / learning or memory / postsynaptic density / molecular adaptor activity / learning or memory /  脂質ラフト / copper ion binding / intracellular membrane-bounded organelle / 脂質ラフト / copper ion binding / intracellular membrane-bounded organelle /  樹状突起 / protein-containing complex binding / negative regulation of apoptotic process / 樹状突起 / protein-containing complex binding / negative regulation of apoptotic process /  ゴルジ体 / ゴルジ体 /  細胞膜 / 細胞膜 /  小胞体 / 小胞体 /  生体膜 / identical protein binding / 生体膜 / identical protein binding /  metal ion binding / metal ion binding /  細胞膜 / 細胞膜 /  細胞質基質 細胞質基質類似検索 - 分子機能 | ||||||
| 生物種 |   Mus musculus (ハツカネズミ) Mus musculus (ハツカネズミ) | ||||||
| 手法 |  溶液NMR / torsion angle dynamics 溶液NMR / torsion angle dynamics | ||||||
 データ登録者 データ登録者 | Gossert, A.D. / Bonjour, S. / Lysek, D.A. / Fiorito, F. / Wuthrich, K. | ||||||
 引用 引用 |  ジャーナル: Proc.Natl.Acad.Sci.Usa / 年: 2005 ジャーナル: Proc.Natl.Acad.Sci.Usa / 年: 2005タイトル: Prion protein NMR structures of elk and of mouse/elk hybrids 著者: Gossert, A.D. / Bonjour, S. / Lysek, D.A. / Fiorito, F. / Wuthrich, K. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1y16.cif.gz 1y16.cif.gz | 690.8 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1y16.ent.gz pdb1y16.ent.gz | 602.1 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1y16.json.gz 1y16.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/y1/1y16 https://data.pdbj.org/pub/pdb/validation_reports/y1/1y16 ftp://data.pdbj.org/pub/pdb/validation_reports/y1/1y16 ftp://data.pdbj.org/pub/pdb/validation_reports/y1/1y16 | HTTPS FTP |
|---|
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 1 |
| |||||||||
| NMR アンサンブル |
|
- 要素
要素
| #1: タンパク質 | 分子量: 13278.773 Da / 分子数: 1 / 断片: C-terminal domain / 変異: S170N, N174T / 由来タイプ: 組換発現 / 由来: (組換発現)   Mus musculus (ハツカネズミ) / 遺伝子: Prnp / 生物種 (発現宿主): Escherichia coli / 発現宿主: Mus musculus (ハツカネズミ) / 遺伝子: Prnp / 生物種 (発現宿主): Escherichia coli / 発現宿主:   Escherichia coli BL21 (大腸菌) / 株 (発現宿主): BL21 / 参照: UniProt: P04925 Escherichia coli BL21 (大腸菌) / 株 (発現宿主): BL21 / 参照: UniProt: P04925 |
|---|
-実験情報
-実験
| 実験 | 手法:  溶液NMR 溶液NMR | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| NMR実験 |
| ||||||||||||
| NMR実験の詳細 | Text: This structure was determined using standard 3D heteronuclear techniques. |
- 試料調製
試料調製
| 詳細 | 内容: 1mM mprp(121-213) S170N,N174T U-15N,13C;10mM acetate 溶媒系: 90% H2O/10% D2O |
|---|---|
| 試料状態 | イオン強度: 10 / pH: 4.5 / 圧: ambient / 温度: 293 K |
-NMR測定
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 放射波長 | 相対比: 1 | |||||||||||||||
| NMRスペクトロメーター |
|
- 解析
解析
| NMR software |
| ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 手法: torsion angle dynamics / ソフトェア番号: 1 詳細: The structure was also refined with ATNOS version 1.0 (author: Herrmann) | ||||||||||||
| 代表構造 | 選択基準: fewest violations | ||||||||||||
| NMRアンサンブル | コンフォーマー選択の基準: target function / 計算したコンフォーマーの数: 100 / 登録したコンフォーマーの数: 20 |
 ムービー
ムービー コントローラー
コントローラー
















 PDBj
PDBj