+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1ml6 | ||||||
|---|---|---|---|---|---|---|---|
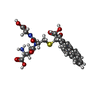
| タイトル | Crystal Structure of mGSTA2-2 in Complex with the Glutathione Conjugate of Benzo[a]pyrene-7(R),8(S)-Diol-9(S),10(R)-Epoxide | ||||||
 要素 要素 | Glutathione S-Transferase GT41A | ||||||
 キーワード キーワード |  TRANSFERASE (転移酵素) / GST detoxification / mGSTA2-2 TRANSFERASE (転移酵素) / GST detoxification / mGSTA2-2 | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報response to stilbenoid /  glutathione binding / glutathione binding /  グルタチオン-S-トランスフェラーゼ / グルタチオン-S-トランスフェラーゼ /  glutathione transferase activity / glutathione metabolic process / xenobiotic metabolic process / response to bacterium / glutathione transferase activity / glutathione metabolic process / xenobiotic metabolic process / response to bacterium /  細胞質基質 細胞質基質類似検索 - 分子機能 | ||||||
| 生物種 |   Mus musculus (ハツカネズミ) Mus musculus (ハツカネズミ) | ||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 1.9 Å 分子置換 / 解像度: 1.9 Å | ||||||
 データ登録者 データ登録者 | Gu, Y. / Xiao, B. / Wargo, H.L. / Bucher, M.H. / Singh, S.V. / Ji, X. | ||||||
 引用 引用 |  ジャーナル: Biochemistry / 年: 2003 ジャーナル: Biochemistry / 年: 2003タイトル: Residues 207, 216, and 221 and the catalytic activity of mGSTA1-1 and mGSTA2-2 toward benzo[a]pyrene-(7R,8S)-diol-(9S,10R)-epoxide 著者: Gu, Y. / Xiao, B. / Wargo, H.L. / Bucher, M.H. / Singh, S.V. / Ji, X. #1:  ジャーナル: Biochemistry / 年: 2000 ジャーナル: Biochemistry / 年: 2000タイトル: Residue R216 and Catalytic Efficiency of a Murine Class Alpha Glutathione S-Transferase toward Benzo[a]pyrene 7(R),8(S)-Diol-9(S),10(R)-Epoxide 著者: Gu, Y. / Singh, S.V. / Ji, X. #2:  ジャーナル: Biochemistry / 年: 1999 ジャーナル: Biochemistry / 年: 1999タイトル: Amino Acid Substitutions at Positions 207 and 221 Contribute to Catalytic Differences between Murine Glutathione S-Transferase A1-1 and A2-2 toward (+)-anti-7,8-Dihydroxy-9,10-epoxy- ...タイトル: Amino Acid Substitutions at Positions 207 and 221 Contribute to Catalytic Differences between Murine Glutathione S-Transferase A1-1 and A2-2 toward (+)-anti-7,8-Dihydroxy-9,10-epoxy-7,8,9,10-tetrahydrobenzo[a]pyrene 著者: Xia, H. / Gu, Y. / Pan, S.-S. / Ji, X. / Singh, S.V. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1ml6.cif.gz 1ml6.cif.gz | 112.9 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1ml6.ent.gz pdb1ml6.ent.gz | 85.3 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1ml6.json.gz 1ml6.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/ml/1ml6 https://data.pdbj.org/pub/pdb/validation_reports/ml/1ml6 ftp://data.pdbj.org/pub/pdb/validation_reports/ml/1ml6 ftp://data.pdbj.org/pub/pdb/validation_reports/ml/1ml6 | HTTPS FTP |
|---|
-関連構造データ
| 関連構造データ |  1f3aS S: 精密化の開始モデル |
|---|---|
| 類似構造データ |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||||||
| 単位格子 |
| ||||||||||||
| Components on special symmetry positions |
|
- 要素
要素
| #1: タンパク質 | 分子量: 25455.799 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)   Mus musculus (ハツカネズミ) / 遺伝子: GST / プラスミド: pET-11d / 発現宿主: Mus musculus (ハツカネズミ) / 遺伝子: GST / プラスミド: pET-11d / 発現宿主:   Escherichia coli (大腸菌) Escherichia coli (大腸菌)参照: UniProt: P10648,  グルタチオン-S-トランスフェラーゼ グルタチオン-S-トランスフェラーゼ#2: 化合物 | #3: 化合物 |  2-プロパノール 2-プロパノール#4: 水 | ChemComp-HOH / |  水 水 |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2.4 Å3/Da / 溶媒含有率: 48.74 % | ||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
結晶化 | 温度: 288 K / 手法: 蒸気拡散法, ハンギングドロップ法 / pH: 7.5 詳細: PEG 4000, isopropanol, NaHepes, pH 7.5, VAPOR DIFFUSION, HANGING DROP, temperature 288K | ||||||||||||||||||||||||||||||||||||||||||||||||
| 結晶化 | *PLUS 温度: 15 ℃ | ||||||||||||||||||||||||||||||||||||||||||||||||
| 溶液の組成 | *PLUS
|
-データ収集
| 回折 | 平均測定温度: 100 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  NSLS NSLS  / ビームライン: X9B / 波長: 0.92 Å / ビームライン: X9B / 波長: 0.92 Å |
| 検出器 | タイプ: ADSC QUANTUM 4 / 検出器: CCD / 日付: 1999年7月23日 / 詳細: mirrors |
| 放射 | モノクロメーター: Si 111 / プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長 : 0.92 Å / 相対比: 1 : 0.92 Å / 相対比: 1 |
| 反射 | 解像度: 1.9→30 Å / Num. all: 37794 / Num. obs: 37794 / % possible obs: 99.7 % / Observed criterion σ(I): 0 / 冗長度: 3.56 % / Biso Wilson estimate: 19.9 Å2 / Rmerge(I) obs: 0.062 / Rsym value: 0.038 / Net I/σ(I): 18.68 |
| 反射 シェル | 解像度: 1.9→1.97 Å / 冗長度: 3.31 % / Rmerge(I) obs: 0.513 / Mean I/σ(I) obs: 2.44 / Rsym value: 0.448 / % possible all: 99.2 |
| 反射 | *PLUS 最高解像度: 1.9 Å / 最低解像度: 30 Å / 冗長度: 4.59 % |
| 反射 シェル | *PLUS % possible obs: 99.2 % |
- 解析
解析
| ソフトウェア |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法 : :  分子置換 分子置換開始モデル: PDB ENTRY 1F3A 解像度: 1.9→26.28 Å / Rfactor Rfree error: 0.006 / Data cutoff high absF: 1753798.71 / Data cutoff high rms absF: 1753798.71 / Data cutoff low absF: 0 / Isotropic thermal model: RESTRAINED / 交差検証法: THROUGHOUT / σ(F): 0 / σ(I): 0 / 立体化学のターゲット値: Engh & Huber
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | 溶媒モデル: FLAT MODEL / Bsol: 44.9908 Å2 / ksol: 0.335569 e/Å3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 33.6 Å2
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine analyze |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 1.9→26.28 Å
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS精密化 シェル | Refine-ID: X-RAY DIFFRACTION / Total num. of bins used: 6
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Xplor file |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化 | *PLUS 最高解像度: 1.9 Å / 最低解像度: 30 Å / Num. reflection obs: 35892 / Rfactor Rfree : 0.249 / Rfactor Rwork : 0.249 / Rfactor Rwork : 0.2 : 0.2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | *PLUS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | *PLUS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 | *PLUS
|
 ムービー
ムービー コントローラー
コントローラー














 PDBj
PDBj