+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1i8k | ||||||
|---|---|---|---|---|---|---|---|
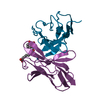
| タイトル | CRYSTAL STRUCTURE OF DSFV MR1 IN COMPLEX WITH THE PEPTIDE ANTIGEN OF THE MUTANT EPIDERMAL GROWTH FACTOR RECEPTOR, EGFRVIII, AT LIQUID NITROGEN TEMPERATURE | ||||||
 要素 要素 |
| ||||||
 キーワード キーワード |  IMMUNE SYSTEM (免疫系) / antibody-peptide complex / immunoglobulin fold / peptide antigen / type II' beta turn. IMMUNE SYSTEM (免疫系) / antibody-peptide complex / immunoglobulin fold / peptide antigen / type II' beta turn. | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 immunoglobulin complex / immunoglobulin mediated immune response / immunoglobulin complex / immunoglobulin mediated immune response /  antigen binding / antigen binding /  獲得免疫系 / blood microparticle / 獲得免疫系 / blood microparticle /  免疫応答 / 免疫応答 /  extracellular space extracellular space類似検索 - 分子機能 | ||||||
| 生物種 |   Mus musculus (ハツカネズミ) Mus musculus (ハツカネズミ) | ||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 1.8 Å 分子置換 / 解像度: 1.8 Å | ||||||
 データ登録者 データ登録者 | Landry, R.C. / Klimowicz, A.C. / Lavictoire, S.J. / Borisova, S. / Kottachchi, D.T. / Lorimer, I.A. / Evans, S.V. | ||||||
 引用 引用 |  ジャーナル: J.Mol.Biol. / 年: 2001 ジャーナル: J.Mol.Biol. / 年: 2001タイトル: Antibody recognition of a conformational epitope in a peptide antigen: Fv-peptide complex of an antibody fragment specific for the mutant EGF receptor, EGFRvIII. 著者: Landry, R.C. / Klimowicz, A.C. / Lavictoire, S.J. / Borisova, S. / Kottachchi, D.T. / Lorimer, I.A. / Evans, S.V. | ||||||
| 履歴 |
| ||||||
| Remark 999 | SEQUENCE Residues 100 of chain A and 344 of chain B have been mutated to Cys residues to introduce ...SEQUENCE Residues 100 of chain A and 344 of chain B have been mutated to Cys residues to introduce a disulfide bridge between chains A and B. There is no sequence database match for chain C because the sequence of EGFRvIII has not yet been deposited in any database. The DNA sequence of the normal EGF receptor has been deposited (NM_005228). |
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1i8k.cif.gz 1i8k.cif.gz | 60.8 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1i8k.ent.gz pdb1i8k.ent.gz | 47.2 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1i8k.json.gz 1i8k.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/i8/1i8k https://data.pdbj.org/pub/pdb/validation_reports/i8/1i8k ftp://data.pdbj.org/pub/pdb/validation_reports/i8/1i8k ftp://data.pdbj.org/pub/pdb/validation_reports/i8/1i8k | HTTPS FTP |
|---|
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||
| 単位格子 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 11745.038 Da / 分子数: 1 / 変異: D100C / 由来タイプ: 組換発現 / 由来: (組換発現)   Mus musculus (ハツカネズミ) / 発現宿主: Mus musculus (ハツカネズミ) / 発現宿主:   Escherichia coli (大腸菌) / 株 (発現宿主): TG1 / 参照: UniProt: Q8R028, UniProt: P01660*PLUS Escherichia coli (大腸菌) / 株 (発現宿主): TG1 / 参照: UniProt: Q8R028, UniProt: P01660*PLUS |
|---|---|
| #2: タンパク質 | 分子量: 13712.354 Da / 分子数: 1 / 変異: R344C / 由来タイプ: 組換発現 / 由来: (組換発現)   Mus musculus (ハツカネズミ) / 発現宿主: Mus musculus (ハツカネズミ) / 発現宿主:   Escherichia coli (大腸菌) / 株 (発現宿主): TG1 / 参照: UniProt: P18529 Escherichia coli (大腸菌) / 株 (発現宿主): TG1 / 参照: UniProt: P18529 |
| #3: タンパク質・ペプチド |  上皮成長因子受容体 / EPIDERMAL GROWTH FACTOR RECEPTOR / EGFRVIII PEPTIDE ANTIGEN 上皮成長因子受容体 / EPIDERMAL GROWTH FACTOR RECEPTOR / EGFRVIII PEPTIDE ANTIGEN分子量: 1421.531 Da / 分子数: 1 / Fragment: N-TERMINAL FRAGMENT / 由来タイプ: 合成 詳細: The peptide sequence is from the N-terminal of the mutant epidermal growth factor receptor, EGFRvIII |
| #4: 水 | ChemComp-HOH /  水 水 |
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2.5 Å3/Da / 溶媒含有率: 50.8 % | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
結晶化 | 温度: 293 K / 手法: 蒸気拡散法, ハンギングドロップ法 / pH: 7 詳細: sodium chloride, MPD, PEG 10K, pH 7.0, VAPOR DIFFUSION, HANGING DROP, temperature 293K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 結晶化 | *PLUS 温度: 18 ℃ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶液の組成 | *PLUS
|
-データ収集
| 回折 | 平均測定温度: 100 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  NSLS NSLS  / ビームライン: X8C / 波長: 0.9789 Å / ビームライン: X8C / 波長: 0.9789 Å |
| 検出器 | タイプ: ADSC QUANTUM 4 / 検出器: CCD / 日付: 1999年6月28日 |
| 放射 | モノクロメーター: collimating mirror optics / プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長 : 0.9789 Å / 相対比: 1 : 0.9789 Å / 相対比: 1 |
| 反射 | 解像度: 1.8→6 Å / Num. all: 25057 / Num. obs: 24309 / % possible obs: 99.8 % / Observed criterion σ(F): 3 / Observed criterion σ(I): 3 / 冗長度: 7.26 % / Biso Wilson estimate: 13.94 Å2 / Rmerge(I) obs: 0.052 / Net I/σ(I): 18.6 |
| 反射 シェル | 解像度: 1.8→1.86 Å / 冗長度: 6.94 % / Rmerge(I) obs: 0.143 / % possible all: 99.4 |
| 反射 | *PLUS 最高解像度: 1.8 Å / Num. obs: 24641 / % possible obs: 98.5 % / Num. measured all: 25654 |
| 反射 シェル | *PLUS % possible obs: 95.7 % |
- 解析
解析
| ソフトウェア |
| ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法 : :  分子置換 / 解像度: 1.8→6 Å / σ(F): 3 / σ(I): 3 / 立体化学のターゲット値: CHARMm 分子置換 / 解像度: 1.8→6 Å / σ(F): 3 / σ(I): 3 / 立体化学のターゲット値: CHARMm
| ||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 13 Å2 | ||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 1.8→6 Å
| ||||||||||||||||||||
| 拘束条件 |
| ||||||||||||||||||||
| LS精密化 シェル | 解像度: 1.8→1.88 Å
| ||||||||||||||||||||
| 精密化 | *PLUS 最高解像度: 1.8 Å / 最低解像度: 6 Å / σ(F): 3 / Rfactor Rfree : 0.225 : 0.225 | ||||||||||||||||||||
| 溶媒の処理 | *PLUS | ||||||||||||||||||||
| 原子変位パラメータ | *PLUS Biso mean: 13 Å2 | ||||||||||||||||||||
| LS精密化 シェル | *PLUS Rfactor Rfree: 0.276 / Rfactor Rwork: 0.216 |
 ムービー
ムービー コントローラー
コントローラー













 PDBj
PDBj
