+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of human Elp123 in complex with tRNA, S-ethyl-CoA, 5'-deoxyadenosine and methionine | |||||||||
 マップデータ マップデータ | deepEMhancer sharpened map | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Elongator / tRNA modification / acetyl-CoA hydrolysis /  TRANSLATION (翻訳 (生物学)) TRANSLATION (翻訳 (生物学)) | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報phosphorylase kinase regulator activity / tRNA uridine(34) acetyltransferase activity / elongator holoenzyme complex / tRNA wobble base 5-methoxycarbonylmethyl-2-thiouridinylation / tRNA wobble uridine modification / regulation of receptor signaling pathway via JAK-STAT /  acetyltransferase activity / acetyltransferase activity /  転移酵素; アシル基を移すもの; アミノアシル基以外のアシル基を移すもの / transcription elongation factor complex / 転移酵素; アシル基を移すもの; アミノアシル基以外のアシル基を移すもの / transcription elongation factor complex /  central nervous system development ...phosphorylase kinase regulator activity / tRNA uridine(34) acetyltransferase activity / elongator holoenzyme complex / tRNA wobble base 5-methoxycarbonylmethyl-2-thiouridinylation / tRNA wobble uridine modification / regulation of receptor signaling pathway via JAK-STAT / central nervous system development ...phosphorylase kinase regulator activity / tRNA uridine(34) acetyltransferase activity / elongator holoenzyme complex / tRNA wobble base 5-methoxycarbonylmethyl-2-thiouridinylation / tRNA wobble uridine modification / regulation of receptor signaling pathway via JAK-STAT /  acetyltransferase activity / acetyltransferase activity /  転移酵素; アシル基を移すもの; アミノアシル基以外のアシル基を移すもの / transcription elongation factor complex / 転移酵素; アシル基を移すもの; アミノアシル基以外のアシル基を移すもの / transcription elongation factor complex /  central nervous system development / transcription elongation by RNA polymerase II / central nervous system development / transcription elongation by RNA polymerase II /  neuron migration / neuron migration /  : / : /  regulation of translation / 4 iron, 4 sulfur cluster binding / HATs acetylate histones / regulation of translation / 4 iron, 4 sulfur cluster binding / HATs acetylate histones /  tRNA binding / positive regulation of cell migration / tRNA binding / positive regulation of cell migration /  核小体 / regulation of transcription by RNA polymerase II / 核小体 / regulation of transcription by RNA polymerase II /  protein kinase binding / protein kinase binding /  核質 / 核質 /  metal ion binding / metal ion binding /  細胞核 / 細胞核 /  細胞質基質 / 細胞質基質 /  細胞質 細胞質類似検索 - 分子機能 | |||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.35 Å クライオ電子顕微鏡法 / 解像度: 3.35 Å | |||||||||
 データ登録者 データ登録者 | Abbassi N / Jaciuk M / Lin T-Y / Glatt S | |||||||||
| 資金援助 | European Union, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2024 ジャーナル: Nat Commun / 年: 2024タイトル: Cryo-EM structures of the human Elongator complex at work. 著者: Nour-El-Hana Abbassi / Marcin Jaciuk / David Scherf / Pauline Böhnert / Alexander Rau / Alexander Hammermeister / Michał Rawski / Paulina Indyka / Grzegorz Wazny / Andrzej Chramiec-Głąbik ...著者: Nour-El-Hana Abbassi / Marcin Jaciuk / David Scherf / Pauline Böhnert / Alexander Rau / Alexander Hammermeister / Michał Rawski / Paulina Indyka / Grzegorz Wazny / Andrzej Chramiec-Głąbik / Dominika Dobosz / Bozena Skupien-Rabian / Urszula Jankowska / Juri Rappsilber / Raffael Schaffrath / Ting-Yu Lin / Sebastian Glatt /    要旨: tRNA modifications affect ribosomal elongation speed and co-translational folding dynamics. The Elongator complex is responsible for introducing 5-carboxymethyl at wobble uridine bases (cmU) in ...tRNA modifications affect ribosomal elongation speed and co-translational folding dynamics. The Elongator complex is responsible for introducing 5-carboxymethyl at wobble uridine bases (cmU) in eukaryotic tRNAs. However, the structure and function of human Elongator remain poorly understood. In this study, we present a series of cryo-EM structures of human ELP123 in complex with tRNA and cofactors at four different stages of the reaction. The structures at resolutions of up to 2.9 Å together with complementary functional analyses reveal the molecular mechanism of the modification reaction. Our results show that tRNA binding exposes a universally conserved uridine at position 33 (U), which triggers acetyl-CoA hydrolysis. We identify a series of conserved residues that are crucial for the radical-based acetylation of U and profile the molecular effects of patient-derived mutations. Together, we provide the high-resolution view of human Elongator and reveal its detailed mechanism of action. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_17926.map.gz emd_17926.map.gz | 313.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-17926-v30.xml emd-17926-v30.xml emd-17926.xml emd-17926.xml | 25 KB 25 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
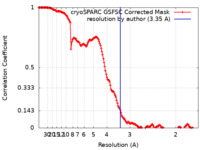
| FSC (解像度算出) |  emd_17926_fsc.xml emd_17926_fsc.xml | 15.2 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_17926.png emd_17926.png | 77.8 KB | ||
| マスクデータ |  emd_17926_msk_1.map emd_17926_msk_1.map | 371.3 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-17926.cif.gz emd-17926.cif.gz | 8.8 KB | ||
| その他 |  emd_17926_half_map_1.map.gz emd_17926_half_map_1.map.gz emd_17926_half_map_2.map.gz emd_17926_half_map_2.map.gz | 344.1 MB 344.1 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-17926 http://ftp.pdbj.org/pub/emdb/structures/EMD-17926 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-17926 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-17926 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_17926.map.gz / 形式: CCP4 / 大きさ: 371.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_17926.map.gz / 形式: CCP4 / 大きさ: 371.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | deepEMhancer sharpened map | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.85 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_17926_msk_1.map emd_17926_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
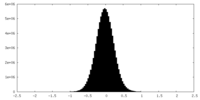
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_17926_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
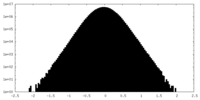
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_17926_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
+全体 : Human Elp123 in complex with glutamine tRNA, S-ethyl-CoA, 5'-deox...
+超分子 #1: Human Elp123 in complex with glutamine tRNA, S-ethyl-CoA, 5'-deox...
+分子 #1: Elongator complex protein 1
+分子 #2: Elongator complex protein 2
+分子 #3: Elongator complex protein 3
+分子 #4: tRNA Gln
+分子 #5: IRON/SULFUR CLUSTER
+分子 #6: 5'-DEOXYADENOSINE
+分子 #7: S-Ethyl-CoA
+分子 #8: METHIONINE
+分子 #9: MAGNESIUM ION
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.6 mg/mL | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
| |||||||||||||||
| グリッド | モデル: Quantifoil R2/1 / 材質: COPPER / メッシュ: 200 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 60 sec. / 前処理 - 雰囲気: AIR / 詳細: 8 mA | |||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV / 詳細: 15 s wait time, blot force 5, 5 s blot time. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.7 µm / 最小 デフォーカス(公称値): 0.9 µm / 倍率(公称値): 96000 Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.7 µm / 最小 デフォーカス(公称値): 0.9 µm / 倍率(公称値): 96000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) デジタル化 - サイズ - 横: 4096 pixel / デジタル化 - サイズ - 縦: 4096 pixel / 実像数: 3192 / 平均電子線量: 40.0 e/Å2 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | Chain - Source name: Other / Chain - Initial model type: experimental model / 詳細: HsElp123-tRNA-ACO-5AD-MET from the same study |
|---|---|
| 得られたモデル |  PDB-8ptz: |
 ムービー
ムービー コントローラー
コントローラー












 Z
Z Y
Y X
X