+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 5nco | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
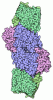
| タイトル | Quaternary complex between SRP, SR, and SecYEG bound to the translating ribosome | |||||||||
 要素 要素 |
| |||||||||
 キーワード キーワード |  RIBOSOME (リボソーム) / SRP / Sec translocon / RIBOSOME (リボソーム) / SRP / Sec translocon /  SRP receptor / SRP receptor /  quaternary complex (第四紀) quaternary complex (第四紀) | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報protein insertion into membrane from inner side / cell envelope Sec protein transport complex /  signal recognition particle binding / protein transport by the Sec complex / signal recognition particle binding / protein transport by the Sec complex /  intracellular protein transmembrane transport / intracellular protein transmembrane transport /  シグナル認識粒子 / シグナル認識粒子 /  signal-recognition-particle GTPase / protein-transporting ATPase activity / 7S RNA binding / SRP-dependent cotranslational protein targeting to membrane, translocation ...protein insertion into membrane from inner side / cell envelope Sec protein transport complex / signal-recognition-particle GTPase / protein-transporting ATPase activity / 7S RNA binding / SRP-dependent cotranslational protein targeting to membrane, translocation ...protein insertion into membrane from inner side / cell envelope Sec protein transport complex /  signal recognition particle binding / protein transport by the Sec complex / signal recognition particle binding / protein transport by the Sec complex /  intracellular protein transmembrane transport / intracellular protein transmembrane transport /  シグナル認識粒子 / シグナル認識粒子 /  signal-recognition-particle GTPase / protein-transporting ATPase activity / 7S RNA binding / SRP-dependent cotranslational protein targeting to membrane, translocation / signal-recognition-particle GTPase / protein-transporting ATPase activity / 7S RNA binding / SRP-dependent cotranslational protein targeting to membrane, translocation /  signal sequence binding / SRP-dependent cotranslational protein targeting to membrane / protein targeting to membrane / signal sequence binding / SRP-dependent cotranslational protein targeting to membrane / protein targeting to membrane /  stringent response / stringent response /  protein secretion / protein transmembrane transporter activity / protein secretion / protein transmembrane transporter activity /  transcriptional attenuation / endoribonuclease inhibitor activity / RNA-binding transcription regulator activity / positive regulation of ribosome biogenesis / transcriptional attenuation / endoribonuclease inhibitor activity / RNA-binding transcription regulator activity / positive regulation of ribosome biogenesis /  protein targeting / negative regulation of cytoplasmic translation / translational termination / DnaA-L2 complex / translation repressor activity / negative regulation of DNA-templated DNA replication initiation / protein targeting / negative regulation of cytoplasmic translation / translational termination / DnaA-L2 complex / translation repressor activity / negative regulation of DNA-templated DNA replication initiation /  ribosome assembly / mRNA regulatory element binding translation repressor activity / assembly of large subunit precursor of preribosome / cytosolic ribosome assembly / response to reactive oxygen species / ribosome assembly / mRNA regulatory element binding translation repressor activity / assembly of large subunit precursor of preribosome / cytosolic ribosome assembly / response to reactive oxygen species /  regulation of cell growth / DNA-templated transcription termination / regulation of cell growth / DNA-templated transcription termination /  intracellular protein transport / response to radiation / intracellular protein transport / response to radiation /  ribosomal large subunit assembly / cytoplasmic side of plasma membrane / mRNA 5'-UTR binding / large ribosomal subunit / ribosomal large subunit assembly / cytoplasmic side of plasma membrane / mRNA 5'-UTR binding / large ribosomal subunit /  ribosome binding / ribosome binding /  5S rRNA binding / large ribosomal subunit rRNA binding / 5S rRNA binding / large ribosomal subunit rRNA binding /  transferase activity / cytosolic large ribosomal subunit / cytoplasmic translation / transferase activity / cytosolic large ribosomal subunit / cytoplasmic translation /  tRNA binding / negative regulation of translation / tRNA binding / negative regulation of translation /  rRNA binding / rRNA binding /  リボソーム / structural constituent of ribosome / リボソーム / structural constituent of ribosome /  ribonucleoprotein complex / ribonucleoprotein complex /  翻訳 (生物学) / response to antibiotic / 翻訳 (生物学) / response to antibiotic /  GTPase activity / negative regulation of DNA-templated transcription / GTPase activity / negative regulation of DNA-templated transcription /  mRNA binding / GTP binding / protein homodimerization activity / mRNA binding / GTP binding / protein homodimerization activity /  ATP hydrolysis activity / ATP hydrolysis activity /  DNA binding / DNA binding /  RNA binding / zinc ion binding / RNA binding / zinc ion binding /  生体膜 / 生体膜 /  細胞膜 / 細胞膜 /  細胞質基質 / 細胞質基質 /  細胞質 細胞質類似検索 - 分子機能 | |||||||||
| 生物種 |   Escherichia coli (大腸菌) Escherichia coli (大腸菌) | |||||||||
| 手法 |  電子顕微鏡法 / 電子顕微鏡法 /  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 4.8 Å クライオ電子顕微鏡法 / 解像度: 4.8 Å | |||||||||
 データ登録者 データ登録者 | Jomaa, A. / Hwang Fu, Y. / Boerhinger, D. / Leibundgut, M. / Shan, S.O. / Ban, N. | |||||||||
| 資金援助 |  スイス, 2件 スイス, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2017 ジャーナル: Nat Commun / 年: 2017タイトル: Structure of the quaternary complex between SRP, SR, and translocon bound to the translating ribosome. 著者: Ahmad Jomaa / Yu-Hsien Hwang Fu / Daniel Boehringer / Marc Leibundgut / Shu-Ou Shan / Nenad Ban /   要旨: During co-translational protein targeting, the signal recognition particle (SRP) binds to the translating ribosome displaying the signal sequence to deliver it to the SRP receptor (SR) on the ...During co-translational protein targeting, the signal recognition particle (SRP) binds to the translating ribosome displaying the signal sequence to deliver it to the SRP receptor (SR) on the membrane, where the signal peptide is transferred to the translocon. Using electron cryo-microscopy, we have determined the structure of a quaternary complex of the translating Escherichia coli ribosome, the SRP-SR in the 'activated' state and the translocon. Our structure, supported by biochemical experiments, reveals that the SRP RNA adopts a kinked and untwisted conformation to allow repositioning of the 'activated' SRP-SR complex on the ribosome. In addition, we observe the translocon positioned through interactions with the SR in the vicinity of the ribosome exit tunnel where the signal sequence is extending beyond its hydrophobic binding groove of the SRP M domain towards the translocon. Our study provides new insights into the mechanism of signal sequence transfer from the SRP to the translocon. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  5nco.cif.gz 5nco.cif.gz | 2.5 MB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb5nco.ent.gz pdb5nco.ent.gz | 表示 |  PDB形式 PDB形式 | |
| PDBx/mmJSON形式 |  5nco.json.gz 5nco.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/nc/5nco https://data.pdbj.org/pub/pdb/validation_reports/nc/5nco ftp://data.pdbj.org/pub/pdb/validation_reports/nc/5nco ftp://data.pdbj.org/pub/pdb/validation_reports/nc/5nco | HTTPS FTP |
|---|
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
-RNA鎖 , 4種, 4分子 12AB
| #1: RNA鎖 | 分子量: 33611.926 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)   Escherichia coli (大腸菌) / 参照: GenBank: 1126835766 Escherichia coli (大腸菌) / 参照: GenBank: 1126835766 |
|---|---|
| #2: RNA鎖 | 分子量: 894.612 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)   Escherichia coli (大腸菌) Escherichia coli (大腸菌) |
| #3: RNA鎖 |  23SリボソームRNA 23SリボソームRNA分子量: 941306.188 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)   Escherichia coli (大腸菌) / 参照: Escherichia coli (大腸菌) / 参照:  GenBank: 2073407 GenBank: 2073407 |
| #4: RNA鎖 |  5SリボソームRNA 5SリボソームRNA分子量: 38790.090 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)   Escherichia coli (大腸菌) / 参照: Escherichia coli (大腸菌) / 参照:  GenBank: 1114321404 GenBank: 1114321404 |
+50S ribosomal protein ... , 30種, 30分子 CDEFGHIJKLMNOPQRSTUVWXYZabcdef
-Protein translocase subunit ... , 2種, 2分子 gh
| #35: タンパク質 | 分子量: 45627.977 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   Escherichia coli (大腸菌) / 遺伝子: secY, prlA, b3300, JW3262 / 発現宿主: Escherichia coli (大腸菌) / 遺伝子: secY, prlA, b3300, JW3262 / 発現宿主:   Escherichia coli BL21 (大腸菌) / 参照: UniProt: P0AGA2 Escherichia coli BL21 (大腸菌) / 参照: UniProt: P0AGA2 |
|---|---|
| #36: タンパク質 | 分子量: 6241.415 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   Escherichia coli (大腸菌) / 遺伝子: secE, prlG, b3981, JW3944 / 発現宿主: Escherichia coli (大腸菌) / 遺伝子: secE, prlG, b3981, JW3944 / 発現宿主:   Escherichia coli BL21 (大腸菌) / 参照: UniProt: P0AG96 Escherichia coli BL21 (大腸菌) / 参照: UniProt: P0AG96 |
-Signal recognition particle ... , 2種, 2分子 il
| #37: タンパク質 |  シグナル認識粒子 / Fifty-four homolog / Ffh / p48 シグナル認識粒子 / Fifty-four homolog / Ffh / p48分子量: 48514.723 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   Escherichia coli (大腸菌) / 遺伝子: ffh, b2610, JW5414 / 発現宿主: Escherichia coli (大腸菌) / 遺伝子: ffh, b2610, JW5414 / 発現宿主:   Escherichia coli BL21 (大腸菌) / 参照: UniProt: P0AGD7 Escherichia coli BL21 (大腸菌) / 参照: UniProt: P0AGD7 |
|---|---|
| #40: タンパク質 | 分子量: 29443.721 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   Escherichia coli (大腸菌) / 遺伝子: ftsY, b3464, JW3429 / 発現宿主: Escherichia coli (大腸菌) / 遺伝子: ftsY, b3464, JW3429 / 発現宿主:   Escherichia coli BL21 (大腸菌) / 参照: UniProt: P10121 Escherichia coli BL21 (大腸菌) / 参照: UniProt: P10121 |
-タンパク質 / タンパク質・ペプチド , 2種, 2分子 jk
| #38: タンパク質 | 分子量: 7234.632 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   Escherichia coli (大腸菌) / 遺伝子: secG, b3175, JW3142 / 発現宿主: Escherichia coli (大腸菌) / 遺伝子: secG, b3175, JW3142 / 発現宿主:   Escherichia coli BL21 (大腸菌) / 参照: UniProt: P0AG99 Escherichia coli BL21 (大腸菌) / 参照: UniProt: P0AG99 |
|---|---|
| #39: タンパク質・ペプチド | 分子量: 2276.820 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   Escherichia coli (大腸菌) / 発現宿主: Escherichia coli (大腸菌) / 発現宿主:   Escherichia coli BL21 (大腸菌) Escherichia coli BL21 (大腸菌) |
-非ポリマー , 4種, 7分子 




| #41: 化合物 | ChemComp-ZN / | ||||
|---|---|---|---|---|---|
| #42: 化合物 | | #43: 化合物 | #44: 化合物 |  グアノシン二リン酸 グアノシン二リン酸 |
-実験情報
-実験
| 実験 | 手法:  電子顕微鏡法 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法:  単粒子再構成法 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 |
| ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 分子量 | 値: 2.7 MDa / 実験値: NO | ||||||||||||||||||||||||
| 由来(天然) |
| ||||||||||||||||||||||||
| 由来(組換発現) | 生物種:   Escherichia coli BL21 (大腸菌) Escherichia coli BL21 (大腸菌) | ||||||||||||||||||||||||
| 緩衝液 | pH: 7.5 | ||||||||||||||||||||||||
| 試料 | 濃度: 0.1 mg/ml / 包埋: NO / シャドウイング: NO / 染色 : NO / 凍結 : NO / 凍結 : YES : YES | ||||||||||||||||||||||||
| 試料支持 | グリッドの材料: COPPER / グリッドのサイズ: 200 divisions/in. / グリッドのタイプ: Quantifoil R2/2 | ||||||||||||||||||||||||
急速凍結 | 装置: FEI VITROBOT MARK I / 凍結剤: ETHANE / 湿度: 100 % / 凍結前の試料温度: 277 K |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源 : :  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD Bright-field microscopy / 倍率(補正後): 100719 X / Cs Bright-field microscopy / 倍率(補正後): 100719 X / Cs : 2.7 mm / アライメント法: COMA FREE : 2.7 mm / アライメント法: COMA FREE |
| 試料ホルダ | 凍結剤: NITROGEN 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER 最高温度: 85 K / 最低温度: 78 K |
| 撮影 | 電子線照射量: 20 e/Å2 / 検出モード: その他 フィルム・検出器のモデル: FEI FALCON II (4k x 4k) |
- 解析
解析
| EMソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
CTF補正 | 詳細: After 3D reconstruction 3D maps were sharpened / タイプ: PHASE FLIPPING ONLY | ||||||||||||||||||||||||||||||||||||||||||||
| 粒子像の選択 | 選択した粒子像数: 1029950 | ||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 点対称性 : C1 (非対称) : C1 (非対称) | ||||||||||||||||||||||||||||||||||||||||||||
3次元再構成 | 解像度: 4.8 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 13926 / 対称性のタイプ: POINT | ||||||||||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | プロトコル: RIGID BODY FIT / 空間: RECIPROCAL / Target criteria: Cross-correlation coefficient | ||||||||||||||||||||||||||||||||||||||||||||
| 精密化 | 最高解像度: 4.8 Å |
 ムービー
ムービー コントローラー
コントローラー












 PDBj
PDBj