+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Human Membrane-bound O-acyltransferase 7 | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | lipid metabolism membrane remodeling /  MEMBRANE PROTEIN (膜タンパク質) MEMBRANE PROTEIN (膜タンパク質) | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 2-acylglycerol-3-phosphate O-acyltransferase activity / 2-acylglycerol-3-phosphate O-acyltransferase activity /  1-acylglycerol-3-phosphate O-acyltransferase activity / phosphatidylinositol acyl-chain remodeling / lysophospholipid acyltransferase activity / regulation of triglyceride metabolic process / lipid modification / 1-acylglycerol-3-phosphate O-acyltransferase activity / phosphatidylinositol acyl-chain remodeling / lysophospholipid acyltransferase activity / regulation of triglyceride metabolic process / lipid modification /  O-acyltransferase activity / phosphatidylcholine acyl-chain remodeling / Acyl chain remodelling of PI / mitochondria-associated endoplasmic reticulum membrane contact site ... O-acyltransferase activity / phosphatidylcholine acyl-chain remodeling / Acyl chain remodelling of PI / mitochondria-associated endoplasmic reticulum membrane contact site ... 2-acylglycerol-3-phosphate O-acyltransferase activity / 2-acylglycerol-3-phosphate O-acyltransferase activity /  1-acylglycerol-3-phosphate O-acyltransferase activity / phosphatidylinositol acyl-chain remodeling / lysophospholipid acyltransferase activity / regulation of triglyceride metabolic process / lipid modification / 1-acylglycerol-3-phosphate O-acyltransferase activity / phosphatidylinositol acyl-chain remodeling / lysophospholipid acyltransferase activity / regulation of triglyceride metabolic process / lipid modification /  O-acyltransferase activity / phosphatidylcholine acyl-chain remodeling / Acyl chain remodelling of PI / mitochondria-associated endoplasmic reticulum membrane contact site / layer formation in cerebral cortex / O-acyltransferase activity / phosphatidylcholine acyl-chain remodeling / Acyl chain remodelling of PI / mitochondria-associated endoplasmic reticulum membrane contact site / layer formation in cerebral cortex /  ventricular system development / phosphatidylinositol biosynthetic process / ventricular system development / phosphatidylinositol biosynthetic process /  転移酵素; アシル基を移すもの; アミノアシル基以外のアシル基を移すもの / endoplasmic reticulum membrane / 転移酵素; アシル基を移すもの; アミノアシル基以外のアシル基を移すもの / endoplasmic reticulum membrane /  小胞体 / 小胞体 /  生体膜 生体膜類似検索 - 分子機能 | |||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.7 Å クライオ電子顕微鏡法 / 解像度: 3.7 Å | |||||||||
 データ登録者 データ登録者 | Wang K / Liao M / Farese RV / Walther TC | |||||||||
| 資金援助 |  米国, 2件 米国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2023 ジャーナル: Nat Commun / 年: 2023タイトル: The structure of phosphatidylinositol remodeling MBOAT7 reveals its catalytic mechanism and enables inhibitor identification. 著者: Kun Wang / Chia-Wei Lee / Xuewu Sui / Siyoung Kim / Shuhui Wang / Aidan B Higgs / Aaron J Baublis / Gregory A Voth / Maofu Liao / Tobias C Walther / Robert V Farese /   要旨: Cells remodel glycerophospholipid acyl chains via the Lands cycle to adjust membrane properties. Membrane-bound O-acyltransferase (MBOAT) 7 acylates lyso-phosphatidylinositol (lyso-PI) with ...Cells remodel glycerophospholipid acyl chains via the Lands cycle to adjust membrane properties. Membrane-bound O-acyltransferase (MBOAT) 7 acylates lyso-phosphatidylinositol (lyso-PI) with arachidonyl-CoA. MBOAT7 mutations cause brain developmental disorders, and reduced expression is linked to fatty liver disease. In contrast, increased MBOAT7 expression is linked to hepatocellular and renal cancers. The mechanistic basis of MBOAT7 catalysis and substrate selectivity are unknown. Here, we report the structure and a model for the catalytic mechanism of human MBOAT7. Arachidonyl-CoA and lyso-PI access the catalytic center through a twisted tunnel from the cytosol and lumenal sides, respectively. N-terminal residues on the ER lumenal side determine phospholipid headgroup selectivity: swapping them between MBOATs 1, 5, and 7 converts enzyme specificity for different lyso-phospholipids. Finally, the MBOAT7 structure and virtual screening enabled identification of small-molecule inhibitors that may serve as lead compounds for pharmacologic development. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_28552.map.gz emd_28552.map.gz | 49.3 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-28552-v30.xml emd-28552-v30.xml emd-28552.xml emd-28552.xml | 14.3 KB 14.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_28552.png emd_28552.png | 115.1 KB | ||
| その他 |  emd_28552_half_map_1.map.gz emd_28552_half_map_1.map.gz emd_28552_half_map_2.map.gz emd_28552_half_map_2.map.gz | 49.5 MB 49.5 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-28552 http://ftp.pdbj.org/pub/emdb/structures/EMD-28552 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-28552 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-28552 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8ercMC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_28552.map.gz / 形式: CCP4 / 大きさ: 52.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_28552.map.gz / 形式: CCP4 / 大きさ: 52.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 0.825 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #2
| ファイル | emd_28552_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
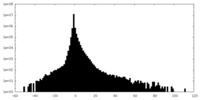
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_28552_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Membrane-bound O-acyltransferase 7
| 全体 | 名称: Membrane-bound O-acyltransferase 7 |
|---|---|
| 要素 |
|
-超分子 #1: Membrane-bound O-acyltransferase 7
| 超分子 | 名称: Membrane-bound O-acyltransferase 7 / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all / 詳細: Purified protein |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 55 kDa/nm |
-分子 #1: Lysophospholipid acyltransferase 7
| 分子 | 名称: Lysophospholipid acyltransferase 7 / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO EC番号:  転移酵素; アシル基を移すもの; アミノアシル基以外のアシル基を移すもの 転移酵素; アシル基を移すもの; アミノアシル基以外のアシル基を移すもの |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 54.196277 KDa |
| 組換発現 | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: MSPEEWTYLV VLLISIPIGF LFKKAGPGLK RWGAAAVGLG LTLFTCGPHT LHSLVTILGT WALIQAQPCS CHALALAWTF SYLLFFRAL SLLGLPTPTP FTNAVQLLLT LKLVSLASEV QDLHLAQRKE MASGFSKGPT LGLLPDVPSL METLSYSYCY V GIMTGPFF ...文字列: MSPEEWTYLV VLLISIPIGF LFKKAGPGLK RWGAAAVGLG LTLFTCGPHT LHSLVTILGT WALIQAQPCS CHALALAWTF SYLLFFRAL SLLGLPTPTP FTNAVQLLLT LKLVSLASEV QDLHLAQRKE MASGFSKGPT LGLLPDVPSL METLSYSYCY V GIMTGPFF RYRTYLDWLE QPFPGAVPSL RPLLRRAWPA PLFGLLFLLS SHLFPLEAVR EDAFYARPLP ARLFYMIPVF FA FRMRFYV AWIAAECGCI AAGFGAYPVA AKARAGGGPT LQCPPPSSPE KAASLEYDYE TIRNIDCYST DFCVRVRDGM RYW NMTVQW WLAQYIYKSA PARSYVLRSA WTMLLSAYWH GLHPGYYLSF LTIPLCLAAE GRLESALRGR LSPGGQKAWD WVHW FLKMR AYDYMCMGFV LLSLADTLRY WASIYFCIHF LALAALGLGL ALGGGSPSRR KAASQPTSLA PEKLREELEA CGIEN LYFQ UniProtKB: Lysophospholipid acyltransferase 7 |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | 2D array |
- 試料調製
試料調製
| 濃度 | 6 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 |
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: OTHER / 最大 デフォーカス(公称値): 2.2 µm / 最小 デフォーカス(公称値): 0.8 µm |
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 55.5 e/Å2 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期モデル | モデルのタイプ: OTHER 詳細: Initial model were generated using ab initio construction in cryoSPARC |
|---|---|
| 初期 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
| 最終 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 3.7 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 206418 |
 ムービー
ムービー コントローラー
コントローラー





 Z
Z Y
Y X
X